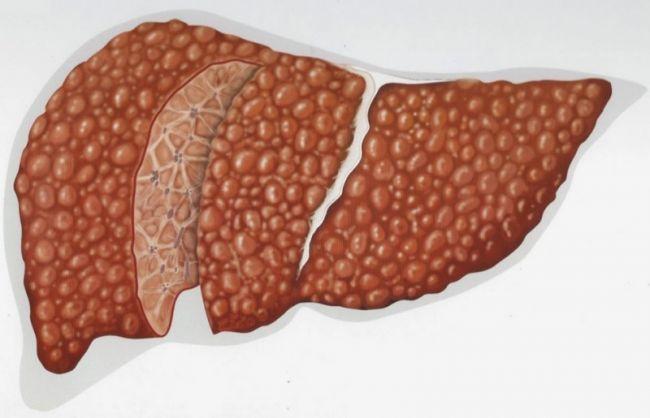
Фокальная липодистрофия 4 сегмента печени — это редкое заболевание, характеризующееся накоплением жировой ткани в определенных участках печени, что приводит к нарушению ее функций. Чаще всего это происходит в результате местного метаболического дисбаланса, воспалительных процессов или новообразований. Заболевание может быть ассоциировано с различными системными нарушениями и имеет важные клинические проявления.
Признаки фокальной липодистрофии включают увеличение печени, а также возможное ухудшение ее функций, что может проявляться желтухой, утомляемостью и другими симптомами. Диагностика требует проведения визуализационных исследований, таких как УЗИ или МРТ, а также лабораторных анализов для определения уровня ферментов и других показателей функционального состояния печени.
- Определение: Фокальная липодистрофия 4 сегмента печени – это заболевание, характеризующееся потерей жировой ткани в определенных зонах печени.
- Причины: Может быть связано с нарушениями метаболизма, наследственными факторами или воздействием лекарств.
- Симптомы: Чаще всего заболевание протекает бессимптомно, но могут возникать нарушения функции печени.
- Диагностика: Определяется с помощью визуализационных методов, таких как УЗИ или МРТ, и биопсии печени.
- Лечение: Основное внимание уделяется устранению причин болезни и контролю состояния печени.
- Прогноз: При своевременной диагностике и адекватном лечении заболевание может иметь благоприятный исход.
Что такое неалкогольная жировая болезнь печени (НАЖБП), как она определяется и какими методами ее лечат?
Неалкогольная жировая болезнь печени (НАЖБП) представляет собой хроническое заболевание, связанное с обменными процессами, при котором происходит накопление жира в тканях печени. Это состояние может привести к гепатиту, фиброзу, циррозу, а в отдельных случаях — к гепатоцеллюлярной карциноме.
Наиболее частыми формами патологии являются неалкогольный стеатогепатоз, который характеризуется стеатозом печени, затрагивающим более 5% печеночной паренхимы, без признаков повреждения гепатоцитов, и неалкогольный стеатогепатит — воспалительный процесс, протекающий с повреждением гепатоцитов на фоне стеатоза.
Исследования DIREG 1 и DIREG 2, в которых участвовали более 50 тысяч людей, показали, что неалкогольная жировая болезнь печени встречается у каждого третьего пациента, который обращается к врачу общей практики. Возраст оказывает значительное влияние на распространенность НАЖБП: среди подростков 12-17 лет болезнь выявляется лишь у 2,9%, тогда как среди людей в возрасте 60-69 лет этот показатель достигает 42,96%. Максимальная распространенность неалкогольного стеатоза наблюдается у пожилых людей 70-80 лет (34,26%), а неалкогольного стеатогепатита — у тех, кому от 50 до 59 лет (10,95%). Увеличение числа случаев среди молодежи до 18 лет вызывает особую тревогу, так как это связано с ростом заболеваемости ожирением у детей.

Этиология и патогенез НАЖБП
- возраст старше 45 лет;
- долгосрочное использование лекарств с гепатотоксическим действием (глюкокортикоидов, НПВП, синтетических эстрогенов, тетрациклинов и других препаратов);
- синдром мальабсорбции;
- резкое снижение веса;
- липодистрофия;
- болезнь Вильсона–Коновалова.
Многочисленные исследования подчеркивают, что инсулинорезистентность является важным фактором, вызывающим развитие и обострение этого заболевания. В настоящее время имеется значительное количество научной информации, подтверждающей взаимосвязь между НАЖБП и инсулинорезистентностью.
Фокальная липодистрофия 4 сегмента печени — это редкое заболевание, характеризующееся избыточным накоплением жировой ткани в печени. Обычно это состояние возникает в определенных областях органа и может быть связано с различными метаболическими нарушениями. Важно отметить, что этот вид липодистрофии не всегда проявляется яркими симптомами, что делает диагностику сложной задачей. Однако выявить наличие жировой инфильтрации можно с помощью современных методов визуализации, таких как УЗИ или МРТ.
Признаки фокальной липодистрофии часто включают увеличение размеров печени, что может быть выявлено при пальпации или в результате обследований. Пациенты могут также испытывать общие симптомы, такие как усталость, дискомфорт в правом подреберье и нарушения пищеварения. Поскольку жировая ткань может оказывать давление на соседние органы, возможны и другие проявления, такие как боли в животе или расстройства пищеварительной системы.
Лечение фокальной липодистрофии 4 сегмента печени зависит от причин заболевания и его тяжести. В некоторых случаях достаточным может быть изменение образа жизни, включая диету и физическую активность, в то время как в более тяжелых случаях может потребоваться медикаментозная терапия или даже хирургическое вмешательство. Важно понимать, что ранняя диагностика и правильное лечение могут существенно улучшить состояние пациента и предотвратить возможные осложнения.
Факторы роста, способствующие воспалительным процессам и образованию фиброза, также играют роль в прогрессировании заболевания. В частности, трансформирующий фактор роста-β (TGF-β), инсулиноподобный фактор роста (IGF-1) и тромбоцитарный фактор роста (PDGF) способствуют увеличению образования коллагена и соединительной ткани в печени. Экспериментальные исследования предположили, что генетические вариации, относящиеся к обмену глюкозы, липидов и воспалению, могут повышать риск развития НАЖБП независимо от ожирения и диабета.
В последнее время активно обсуждается влияние микробиоты кишечника на возникновение неалкогольного стеатогепатита. Данные некоторых экспериментальных исследований показали, что увеличение нормальной микрофлоры или появление патогенной флоры в тонком кишечнике может привести к синдрому избыточного бактериального роста и эндотоксемии. Присутствие эндотоксинов может вызвать нарушение целостности кишечного барьера и оксидативный стресс в печени, что в свою очередь, может инициировать развитие неалкогольного стеатогепатита.
Таким образом, патогенез неалкогольной жировой болезни печени достаточно сложен и включает различные механизмы. В нем участвуют инсулинорезистентность, уровень адипоцитокинов, медиаторов воспаления, состояние кишечной микрофлоры и многие другие факторы, поэтому исследования механизмов патогенеза НАЖБП в настоящее время продолжаются.
Симптомы жировой дистрофии
Клиническая картина врожденной генерализованной липодистрофии включает отсутствие подкожно-жировой клетчатки и чрезмерное накопление жира в печени, сердечной мышце, почках и скелетных мышцах, что приводит к нарушению их функционирования. Проблемы с обменом веществ и углеводов порождают инсулинорезистентность и могут привести к диабету второго типа, как правило, к 20 годам. Из-за затрудненного усвоения жиров в крови увеличивается уровень липидов и возрастает нагрузка на органы, участвующие в их метаболизме.
Пациенты с этой формой липодистрофии зачастую имеют стройное телосложение и худое лицо, у них четко выражены подкожные вены, наблюдается увеличение кистей и стоп, а также гиперпигментация в складках кожи.
При семейной парциальной жировой дистрофии потеря подкожно-жировой клетчатки в основном происходит в области ног, реже — на руках и туловище. У таких пациентов отмечается избыток жировых отложений в области живота, шеи и лица. Для этой формы болезни характерна инсулинорезистентность, повышение уровня триглицеридов и жирных кислот в крови, скопление жира в гепатоцитах и скелетных мышцах, а также нарушения секреции лептина, что увеличивает вероятность сахарного диабета.
При приобретенной генерализованной липодистрофии изначально наблюдается нормальное распределение жира в организме. Однако с течением времени, чаще всего в детском или подростковом возрасте, наблюдается потеря жировой ткани на лице и конечностях. У каждого четвертого пациента в начале болезни возникает панникулит с локальными липодистрофиями. Накопление жира в печени может спровоцировать развитие цирроза и диабета, а также привести к повышению уровня триглицеридов.
При приобретенной парциальной жировой дистрофии отмечается потеря жировых клеток в верхней части туловища, тогда как ноги чаще всего остаются непораженными, а ягодицы и бедра затрагиваются лишь в редких случаях. Эта форма заболевания наиболее часто связана с ВИЧ-инфекцией.
При липодистрофии, обусловленной инъекциями инсулина в области введения препарата наблюдается отечность подкожно-жировой клетчатки и ее уплотнение. Редко в местах проведения инъекций наблюдается гиперпигментация.
Методы лечения жировой дистрофии
Лечение липодистрофии зависит от специфики заболевания, клинической картины и имеющихся нарушений обмена. В настоящее время не существует специфической терапии. Обычно назначаемые гиполипидемические препараты могут не давать ожидаемого эффекта. Применяется в основном симптоматическое лечение, направленное на облегчение симптомов и предотвращение осложнений.
Так как жировые клетки отвечают за выработку гормонов, включая лептин, при врожденных липодистрофиях наблюдается его дефицит. В таких ситуациях рекомендуется принимать препараты-аналоги лептина для нормализации обменных процессов.
При значительных нарушениях обмена показаны фармакологические средства, которые корректируют уровень липидов и сахара в крови. Если липодистрофия вызывается инсулиновыми инъекциями, необходимо проводить профилактические мероприятия для предотвращения дальнейшего повреждения жировых клеток.
В схему лечения могут включаться гепатопротекторы, препараты против аритмии. При умственной отсталости ребенку показаны занятия по специальной программе и работа с квалифицированным психологом. Во взрослом возрасте больные врожденной генерализованной жировой дистрофией для коррекции слишком худого лица прибегают к помощи косметологических процедур, а также проводят пластические операции.
Пациентам с установленной приобретенной парциальной жировой дистрофией для коррекции выраженных изменений может быть выполнена аутотрансплантация жировых тканей, при которой используется собственная жировая ткань организма, что показывает высокую эффективность.
Клинические проявления жировой дистрофии печени
Ранние симптомы
Ранние стадии неалкогольной жировой болезни печени часто протекают без симптомов. Большинство пациентов не жалуются на состояния, хотя иногда может наблюдаться слабость, усталость и дискомфорт в правом подреберье. При осмотре у 50–75% больных выявляется увеличение печени, а у 25% — увеличение селезенки.
Симптомы острого заболевания
Острая жировая дегенерация печени является редким патологическим состоянием, возникающим в результате отравления ядовитыми грибами, антибиотиками, либо фосфоросодержащими и мышьяковистыми соединениями. Эта форма жировой дистрофии также является одним из наиболее тяжёлых осложнений беременности, возникающим из-за нехватки клеточных ферментов. Она проявляется ярко выраженной симптоматикой:
- боль в области подложечной;
- изжога;
- тошнота;
- рвота, в тяжелых случаях с примесью крови;
- желтуха кожи, слизистых и склер;
- вялая реакция;
- мышечная слабость;
- спутанность сознания.
При этом печень имеет нормальные или уменьшенные размеры. Подобное состояние может повлечь за собой развитие острой печеночно-почечной недостаточности и нарушение свертываемости крови (ДВС-синдром), иногда приводящие к смерти пациента. При более благоприятном исходе происходит трансформация острой жировой дистрофии печени в хроническую форму.
Симптомы хронической формы
Хроническая форма неалкогольной жировой болезни печени характеризуется малозаметной симптоматикой:
- ощущение тяжести в правом подреберье;
- проблемы с аппетитом;
- тошнота после еды;
- метеоризм;
- периодические нарушения стула.
К менее характерным признакам жировой дистрофии печени относятся:
- снижение остроты зрения;
- тусклость, пастозность и сухость кожи;
- появление сосудистых звездочек;
- астеновегетативные расстройства (усталость, слабость, головные боли).
В ходе диагностического осмотра обнаруживается незначительная болезненность и увеличение нижнего края печени.
Несвоевременное и адекватное лечение может привести к серьезным осложнениям, таким как фиброз, цирроз печени, инфаркт или инсульт.
Диагностика НАЖБП
Для диагностики неалкогольной жировой болезни печени необходимо собрать анамнез, провести физикальный осмотр, измерить индекс массы тела, а также провести лабораторное и инструментальное обследование.
Лабораторные методы диагностики:
- биохимическое исследование крови (определение уровня билирубина, АлТ, АсТ, гамма-глутамилтранспептидазы, протромбина, показателей обмена железа, щелочной фосфатазы и белковых фракций, уровень глюкозы);
- анализ на вирусные гепатиты;
- генетическое тестирование (для исключения гемохроматоза и болезни Вильсона);
- фибротест (для определения степени фиброза печени).
Инструментальная диагностика:
- ультразвуковое обследование;
- КТ или МРТ (для определения степени жировой инфильтрации печени);
- протонная магниторезонансная спектроскопия (для оценки количества жира в печени);
- Целевая биопсия печени осуществляется для проведения различия между неалкогольным стеатозом и прочими заболеваниями печени, а также чтобы оценить, как эффективно проходит лечение неалкогольной жировой болезни печени (НАЖБП).
Узнайте свой индекс массы тела прямо сейчас!
Липодистрофия печени
Жировая дистрофия печени (жировой гепатоз) возникает вследствие замещения гепатоцитов жировыми клетками. При гепатозе скапливаются жировые отложения, которые выглядят как капли на печени.
Основными причинами жировой дистрофии считаются заболевания желчного пузыря, его протоков, а также расстройства в кишечнике. Жировая дистрофия печени (ЖДП) может быть вызвана следующими заболеваниями:
- Серьезное ожирение.
- Сахарный диабет второго типа, мальабсорбционный и мальдигестивный синдром.
- Чрезмерное потребление алкоголя.
- Употребление кортикостероидов, тетрациклинов, эстрогенов и НПВС.
Липодистрофия часто развивается на фоне хронических гепатитов, особенно гепатита типа С.
Характерные признаки, наблюдаемые на макропрепарате при ЖДП: увеличенная печень (гепатомегалия), гладкая поверхность, плотная или рыхлая консистенция, округлый передний край органа, который имеет глинистый, желтый или желто-коричневый цвет.
Токсическая ДП
Токсическая дистрофия печени (ТДП) проявляется обширными быстро развивающимися некротическими процессами, которые затрагивают структуру печени. Обычно патология имеет острое течение, но иногда переходит в хроническую форму, провоцируя дисфункцию печени.
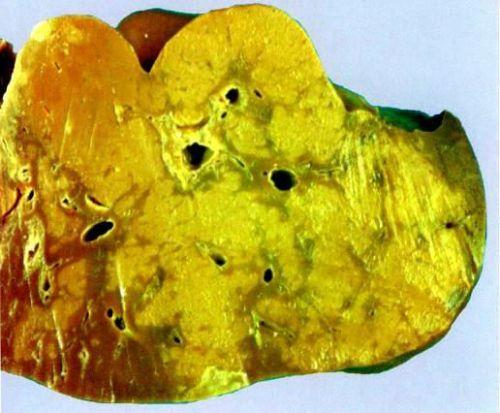
При токсической дистрофии печени (ТДП) происходят некротические изменения.
Массированные некрозы могут возникать в результате воздействия токсинов, содержащихся в продуктах питания, например, в грибах. Подобные отравления могут быть вызваны внешними факторами. Токсическая дистрофия печени также может развиваться из-за эндотоксикоза. К таким состояниям относятся токсикозы у беременных женщин и гипертиреоз, при котором наблюдается избыток гормонов щитовидной железы. Часто ТДП развивается на фоне гепатита, при этом дистрофия становится симптомом острого течения болезни.
Токсическая дистрофия печени сопровождается увеличением размеров печени, изменениями в тканевой плотности — орган может быть как дряблым, так и плотным, и приобретает желтоватый оттенок. Если не проводить лечение, печень постепенно уменьшается, капсульная оболочка покрывается морщинами, а орган может принять серый цвет, что напоминает глинистую массу.
В течение трех недель печень продолжает уменьшаться и приобретать красноватую окраску. Со временем начинает обнажаться ретикулярная строма печени, в которой отчетливо видны расширенные и переполненные кровью капилляры. Гепатоциты остаются лишь в редких участках долек, что свидетельствует о красной дистрофии.
Хроническая токсическая дистрофия печени – редкое состояние, которое может привести к серьезным последствиям, включая быстрое ухудшение функции печени и угрозу жизни пациента.
Жировая дистрофия печени

Жировая дистрофия печени // Источник: Unsplash
Общие сведения о заболевании
Причины возникновения заболевания:
- Злоупотребление алкоголем является самой распространенной причиной жирового гепатоза. Этиловый спирт и его метаболические продукты влияют на все стадии обмена жиров в печени, и степень жировой дистрофии зависит от количества выпитого алкоголя.
- Сахарный диабет.
- Ожирение и избыточное поступление жира с пищей.
- Недостаток белка, синдром Квашиоркор (накопление жира в печени связано с дефицитом белка и нарушением транспорта жиров из печени к тканям).
- Отравление гепатотропными токсинами (такими как четыреххлористый углерод, ДДТ, желтый фосфор и некоторые другие).
- Применение определенных лекарств.
Симптоматика
Пациенты с жировым гепатозом жалоб обычно не предъявляют. Течение болезни стертое, медленно прогрессирующее. Со времени появляются постоянные тупые боли в правом подреберье, могут быть тошнота, рвота, нарушения стула.
Жировая дистрофия печени редко проявляется выраженной клинической картиной: сильными болями в животе, желтухой, потерей веса, кожным зудом.
Диагностика
Врач-терапевт может заподозрить жировую дистрофию печени уже на этапе клинического осмотра, почувствовав увеличение печени при пальпации живота. Это увеличение органа можно подтвердить с помощью УЗИ брюшной полости. В биохимических анализах крови выявляется повышенный уровень печеночных ферментов (АсАТ, АлАТ, щелочная фосфатаза). В некоторых случаях для уточнения диагноза проводят компьютерную томографию, магнитно-резонансную томографию и биопсию печени.
Лечение
Плотность печени на КТ при жировом гепатозе

При жировой инфильтрации плотность паренхимы печени (L) на КТ оказывается ниже, чем у селезенки (S), по крайней мере, на 10 HU.
В норме денситометрические показатели главной пищеварительной железы составляют 50-75 HU, сосудов — 35-50 единиц. Внутрипеченочные желчевыводящие протоки у здорового человека не визуализируются. Ослабление КТ ниже — 40 HU на постконтрастной томограмме является убедительным доказательством стеатоза печени. При диффузной жировой инфильтрации плотность органа равномерно снижена, чаще присутствует гепатомегалия.
КТ, МРТ и УЗИ при стеатозе печени

Изображение жирового гепатоза на сонограмме.
Ультразвуковое исследование — это основной метод визуализации, основанный на принципах эхолокации. Высокочастотные акустические волны абсолютно безопасны для человека. УЗИ органов брюшной полости почти не имеет противопоказаний и может быть выполнено даже у постели пациента с использованием портативного оборудования. Сонограммы помогают выявить стеатоз печени при изменении тканей более чем на 30%.
К разновидности УЗИ относится эластография, позволяющая оценить плотность печени, диагностировать стеатоз, фиброз или цирроз. Однако эластография имеет ограниченную информативность на поздних сроках беременности или при асците (скоплении жидкости в брюшной полости).
Если результатов ультрасонографии при жировом гепатозе недостаточно, используют экспертные способы визуализации — КТ или МРТ.
Магнитно-резонансная томография с контрастированием предпочтительнее для оценки подозрительных участков фокального стеатоза и исключения опухолевых образований. Это исследование можно провести пациентам без металлических имплантов в теле. Качество изображений сильно зависит от характеристик оборудования, и оптимальным вариантом считается МРТ на аппарате мощностью от 1,5 Тесла.

Определение доли липидной инфильтрации гепатоцитов с помощью магнитно-резонансного сканирования (PDFF) позволяет количественно оценить степень поражения печени при неалкогольной жировой болезни.
Учитывая отсутствие ионизирующего облучения во время процедуры, МРТ может быть назначена для контроля изменений в динамике на фоне проводимого лечения.
Компьютерная томография при жировом гепатозе предоставляет достаточно информации для оценки вероятности прогрессирования заболевания и начала терапии.
В самых сложных случаях может потребоваться осуществление биопсии и патоморфологическое исследование.
В диагностическом центре “Магнит” в Санкт-Петербурге КТ, МРТ и УЗИ печени проводят на современном высококачественном оборудовании. Для получения любой услуги требуется предварительная запись по телефону: 8 (812) 407-32-31 . Для описания изменений в динамике в клинику необходимо предоставить результаты ранее выполненной диагностики.
Для проведения КТ с контрастом необходимы направление от врача и результаты анализа крови на креатинин.