При повреждении мениска коленного сустава использование противовоспалительных препаратов, таких как Кетонал, может помочь в alleviation (облегчении) боли и снижении воспаления. Кетоновая кислота обладает хорошими анальгезирующими и противовоспалительными свойствами, что делает ее подходящей для лечения травм колена.
Однако перед началом приема любого из этих препаратов стоит проконсультироваться с врачом, чтобы определить наиболее подходящее лечение и избегать возможных побочных эффектов. Корректная диагностика и индивидуальный подход помогут ускорить процесс восстановления.
- Мениск коленного сустава играет важную роль в стабилизации и амортизации суставов.
- Повреждения мениска могут вызывать боль, снижение подвижности и другие симптомы.
- Кетонов и Кетонал — нестероидные противовоспалительные препараты (НПВП), используемые для облегчения боли и воспаления.
- Выбор между Кетонов и Кетонал зависит от индивидуальных особенностей пациента и рекомендаций врача.
- Обе препараты имеют схожие показания, но могут различаться по побочным эффектам и дозировке.
- Важно проконсультироваться с врачом перед началом лечения для определения оптимального подхода.
Кетопрофен — это один из сильнейших ингибиторов циклооксигеназы (ЦОГ), оказывающий влияние и на активность липоксигеназы, а также брадикинина. Он способствует стабилизации мембран лизосом, что защитит от высвобождения ферментов, участвующих в воспалительных явлениях.
К ключевым особенностям кетопрофена относятся его анальгетические, противовоспалительные и противоотечные свойства. К тому же, он не оказывает вредного воздействия на суставной хрящ.
Абсорбция. Способность местных НПВП проникающей через дерму во многом зависит от физических и химических характеристик составляющих геля. Скорость выделения и усвоения кетопрофена в форме геля для наружного применения определяется вспомогательными веществами, входящими в состав препарата. В отличие от оральной формы, биодоступность кетопрофена в виде геля составляет около 5%. Препарат действует преимущественно на местном уровне, не имея системного эффекта.
Распределение. Кетопрофен преимущественно связывается с белками плазмы (99%). Проникает в ткани суставов, в т.ч. синовиальную жидкость, и достигает там терапевтических концентраций. При этом концентрация кетопрофена в крови остается незначительной. При местном нанесении в виде геля Cmax кетопрофена в плазме отмечается через 6 ч. Значимые концентрации присутствуют в подкожно-жировой клетчатке, околосуставных тканях и синовиальной жидкости. Действие препарата в тканях сохраняется до 12 ч.
Метаболизм и выведение. В печени происходит метаболизм кетопрофена с образованием конъюгатов, экретируемых в основном через почки. Этот процесс не зависит от возраста и наличия печеночной или почечной недостаточности. Кетопрофен выводится из организма постепенно почками.
Показания
Симптоматическая терапия направлена на ослабление боли и воспалительных симптомов при следующих состояниях (не влияя на прогрессирование основной болезни):
При повреждении мениска коленного сустава мне часто задают вопрос о том, какую противовоспалительную терапию выбрать: кетонов или кетонал. Оба эти препарата относятся к группе нестероидных противовоспалительных средств (НПВС) и обладают схожими механизмами действия. Однако между ними есть ряд отличий, которые важно учитывать при выборе лечения.
Кетонов, в частности, обладает более высокой селективностью к циклооксигеназе-2 (ЦОГ-2), что делает его предпочтительным вариантом для длительного использования. Это может привести к меньшему числу побочных эффектов, связанных с желудочно-кишечным трактом, что является особенно важным для пациентов с предрасположенностью к гастриту или язвам. С другой стороны, кетонал, хоть и менее селективен, может быть более эффективен при выраженных болях, связанных с острыми повреждениями.
Выбор между кетонов и кетоналом должен основываться на индивидуальных особенностях пациента, наличии сопутствующих заболеваний и степени выраженности болевого синдрома. Важно также учитывать, что оба препарата имеют разные способы применения и формы выпуска, что может влиять на удобство для пациента. Я всегда рекомендую провести полноценную оценку состояния и согласовать выбор средства с лечащим врачом, чтобы избежать возможных осложнений и добиться наилучшего результата в лечении.
- реактивный артрит (синдром Рейтера);
- остеоартроз разных локализаций;
- периартрит, тендинит, бурсит, миалгия, невралгия, радикулит;
- травмы опорно-двигательного аппарата (в том числе спортивные), ушибы мышц и связок, растяжения и разрывы связок и сухожилий.
Виды повреждений
Разрыв или надрыв мениска — это частая травма колена, встречающаяся не только у спортсменов, но и у обычных людей. Ее можно классифицировать как:
- травматический разрыв, возникающий в результате прямого удара (например, по колену) или происшествия (падение, скручивание колена);
- дегенеративный разрыв, вызванный истощением мениска в процессе старения.
Ортопедические хирурги делят разрывы мениска на разные категории в зависимости от их тяжести и сложности.
Выделяют поражение медиального или латерального мениска коленного сустава. Возможно поражение сразу двух хрящевых элементов, что утяжеляет состояние.
Причины повреждений, разрывов мениска
Любые действия, которые связаны с поворотами или скручиваниями колена, могут привести к повреждению медиального или латерального мениска. Например, подобные травмы часто происходят у спортсменов, которые резко останавливаются или разворачиваются на месте, оставляя ногу неподвижной. Другие действия потенциально вызывающие разрыв включают:
- длительное пребывание на коленях;
- приседания, особенно глубокие и с дополнительным весом;
- подъем тяжестей с согнутыми коленями.
При приседаниях чувствуется боль в коленях
Если мениск дегенерировал, изношен и хрупок, возможно, не будет какого-либо конкретного действия или движения, которое приведет к его разрыву. Боль и отек могут пройти сами по себе через несколько недель; однако симптомы разрыва мениска часто возвращаются, если человек возобновляет деятельность, которая оказывает давление или напряжение на колено.
Диагностика
Для диагностики разрыва мениска применяются несколько методов исследования, позволяющих установить наличие повреждений и их степень.
Физическое обследование
Врач осматривает колено, оценивая симптомы, проверяя диапазон движений и осуществляя специальные тесты (например, тест МакМюррея, направленный на выявление болевых ощущений), чтобы установить стабильность колена и признаки разрыва мениска. [5]
Магнитно-резонансная томография (МРТ)
МРТ является одним из наиболее точных методов диагностики разрыва мениска. Он позволяет получить детальные изображения мягких тканей колена, к которым относится мениск, и выявить наличие разрывов, их размер, форму и местоположение. [4]
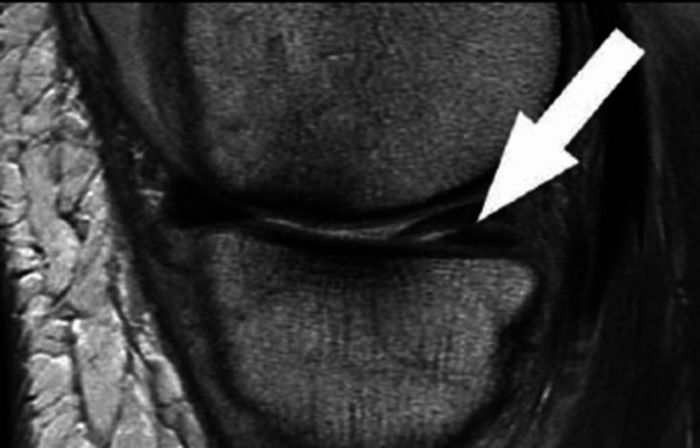
Рис. 3 МРТ-снимок с горизонтальным разрывом медиального мениска заднего рога
УЗИ (ультразвуковое исследование)
Ультразвуковое исследование является быстрым и доступным способом выявления грубых разрывов мениска, однако его точность ниже, чем у МРТ.
Артроскопия
Диагностическая артроскопия — это хирургическая процедура, при которой врач вводит специальный инструмент (артроскоп) через маленький разрез в колене. Артроскоп оснащен камерой и освещением, что позволяет врачу визуально осмотреть внутренние структуры коленного сустава, включая мениски, и определить наличие и характер разрыва.
Артроскопия также используется для выполнения хирургического лечения разрыва мениска, такого как его сшивание или удаление. [4]
Степени повреждения мениска по данным МРТ
В медицинской практике наиболее часто используется классификация по Stoller, которая позволяет оценить степень повреждения мениска по результатам МРТ (этот метод также помогает оценить состояние костей, хрящей, связок и капсулы коленного сустава). [6]
Согласно классификации Stoller, повреждения мениска делятся на четыре степени:
- Нулевая степень (0): соответствует нормальному состоянию мениска без патологий.
- Первая степень (1): наблюдается очаговый сигнал повышенной интенсивности в толще мениска.
- Вторая степень (2): определяется линейный сигнал повышенной интенсивности.
- Третья степень (3a и 3b): сигнал значительно усиливается, достигая края мениска (3a – до одного края, 3b – до обоих), что указывает на разрыв.
Следует отметить, что классификация Stoller имеет свои недостатки: она не учитывает характер разрыва, его протяженность и перспективы восстановления. Врачи-ортопеды обычно сопровождают снимки МРТ более подробными описаниями при оценке и планировании лечения заболевания. Например, разрывы мениска могут классифицироваться по типу повреждения: вертикальные, горизонтальные, косой, радиальный и т.п.

Рис.4 Различные типы повреждений мениска
Фармакокинетика
При пероральном приеме кетопрофен быстро всасывается из желудочно-кишечного тракта. Его биодоступность составляет 90%. При назначении дозы 100 мг в обычной лекарственной форме, максимальная концентрация (C max) в плазме крови достигает 10.4 мкг/мл через 1 час и 22 минуты.
Связывание кетопрофена с белками плазмы крови составляет 99%, в основном с альбуминовой фракцией. V d составляет 0.1 л/кг. Кетопрофен проникает в синовиальную жидкость и после приема внутрь достигает там концентрации, равной 30% концентрации в плазме крови. C ss кетопрофена в плазме крови определяются даже через 24 ч после его приема.
Кетопрофен подвергается значительному метаболизму посредством микросомальных ферментов печени. Период полураспада (T 1/2) составляет менее двух часов. Кетопрофен связывается с глюкуроновой кислотой и выводится из организма в виде глюкуронида. Активных метаболитов кетопрофена не существует. До 80% кетопрофена выводится почками в течение 24 часов, в основном в форме глюкуронида.
Показания активных веществ препарата Кетонал ®
Симптоматическая терапия боли, в том числе воспалительного происхождения: ревматоидный артрит; серонегативные артриты: анкилозирующий спондилит (болезнь Бехтерева), псориатический артрит, реактивный артрит (синдром Рейтера); подагра, псевдоподагра; дегенеративные заболевания опорно-двигательного аппарата, включая остеоартроз; различные по степени интенсивности болевые синдромы: головная боль, мигрень, тендинит, бурсит, миалгия, невралгия, радикулит; посттравматические и послеоперационные боли, в том числе с воспалением и повышенной температурой; боли при онкологических заболеваниях; альгодисменорея.
| Код МКБ-10 | Показание |
| G43 | Мигрень |
| M02.3 | Болезнь Рейтера |
| M05 | Серопозитивный ревматоидный артрит |
| M07 | Псориатические и энтеропатические артропатии |
| M10 | Подагра |
| M13.9 | Артрит неуточненный |
| M15 | Полиартроз |
| M19.9 | Артроз неуточненный |
| M25.5 | Боль в суставе |
| M42 | Остеохондроз позвоночника |
| M45 | Анкилозирующий спондилит |
| M47 | Спондилез |
| M54.1 | Радикулопатия |
| M54.3 | Ишиас |
| M54.4 | Люмбаго с ишиасом |
| M65 | Синовиты и теносиновиты |
| M70 | Болезни мягких тканей, связанные с нагрузкой, перегрузкой и давлением |
| M71 | Другие бурсопатии |
| M79.1 | Миалгия |
| M79.2 | Невралгия и неврит неуточненные |
| N94.4 | Первичная дисменорея |
| N94.5 | Вторичная дисменорея |
| R51 | Головная боль |
| R52.0 | Острая боль |
| R52.2 | Другая постоянная боль (хроническая) |
| T14.3 | Вывих, растяжение и перенапряжение капсульно-связочного аппарата сустава неуточненной области тела |
| T14.9 | Травма неуточненная |
Если обезболивающие гели не помогают и боль умеренная или средней интенсивности
В таких случаях назначаются обезболивающие и противовоспалительные средства:
- Таблетки Кеторол по 1 таблетке, внутрь в дозе 10 мг — 2-3 раза в день на протяжении 7 дней (можно до 4 раз в сутки в зависимости от степени боли, но не более).
- Или Капсулы Кетонал Дуо по 1 капсуле (150 мг) не более 2 раз в сутки.
- Или Таблетки Дексалгин по 1 таблетке (25 мг) 1-3 раза в день через каждые 8 часов.
Внимание, прием анальгетиков по продолжительности не должен превышать 5-7 дн., и обязательно сочетается с приемом препаратов которые понижают кислотность желудка (Омез, Нольпаза).

Если обезболивающие гели не помогают и боль сильная
В таких случаях могут понадобиться инъекции:
- Розчин Кетопрофен 2 мл внутримышечно 2 раза в день (+ Гастропротекция, принимайте Омез по 1 капсуле 2 раза в день на весь период лечения).
- Или Розчин Кеторол по 1 мл внутримышечно 2 раза в день (+ Гастропротекция, принимайте Омез по 1 капсуле 2 раза в день на весь период лечения).
- Или Дексалгин по 2 мл внутримышечно 2 раза в день (+ Гастропротекция, принимайте Омез по 1 капсуле 2 раза в день на весь период лечения).

Здесь представлены самые популярные препараты для обезболивания, однако на аптечном рынке имеется значительно большее количество вариантов.
ММА имени И.М. Сеченова
Заболевания суставов — одна из наиболее частых причин визита пациентов к врачу (см. рис. 1). Болевой синдром, возникающий при повреждении суставов и окружающих тканей, зачастую носит хронический характер и значительно снижает качество жизни людей.
Причины болевых ощущений в различных структурах опорно–двигательного аппарата могут быть разнообразными: они могут быть связаны с поражением сосудов или нервов, увеличением внутримедуллярного давления или спазмом мышц. Однако наиболее часто это обусловлено хроническим воспалением синовиальной оболочки. Пациенты, страдающие от ревматоидного артрита, болезни Бехтерева, псориатической артропатии, обычно вынуждены длительное время принимать обезболивающие лекарства, которые обладают и противовоспалительным действием. Повышение распространенности деформирующего остеоартроза влияет на растущее число людей, нуждающихся в обезболивающих. Поэтому к препаратам, способствующим снижению воспаления и боли, выдвигаются определенные требования: они должны быть как эффективными, так и переносимыми для краткосрочного и длительного применения.
Рис. 1. Частота развития различных заболеваний в популяции (US National Health Interview Survey, 1999)
НПВП обладают тремя основными свойствами: анальгезирующим, противовоспалительным и жаропонижающим. Эти препараты широко используют в медицинской практике, прежде всего, для облегчения острой и хронической боли различного происхождения.
Основная часть медикаментов данной группы действует как неселективные ингибиторы циклооксигеназы (ЦОГ), которая играет ключевую роль в расщеплении фосфолипидов клеточных мембран при их повреждении [1]. Это воздействие обуславливает как их терапевтическую эффективность (антиоксидантный эффект ЦОГ–2), так и вероятность возникновения побочных эффектов (антиоксидантный эффект ЦОГ–1). Эти наблюдения стали шансом для разработки нового класса НПВП с селективным воздействием на ЦОГ–2 (к таким относятся мелоксикам, нимесулид и целекоксиб), которые зарекомендовали себя как эффективные средства при хронических воспалительных процессах в опорно-двигательном аппарате. Также стоит отметить, что переносимость этих препаратов по отношению к слизистой ЖКТ сопоставима с эффектом плацебо [2,3]. Ранее предполагалось, что более сильное обезболивание или противовоспалительный эффект сопряжены с увеличением частоты нежелательных эффектов. Тем не менее, в последнее время стали поступать новые данные о ЦОГ-независимых механизмах как действия, так и побочных эффектов НПВП [4]. Были зафиксированы случаи, когда неселективные НПВП обладали центральным механизмом анальгезии, который, как правило, заметно сильнее, чем у селективных ЦОГ–2 ингибиторов [5,6].
Кетопрофен (Кетонал) представляет собой производное пропионовой кислоты, как и такие известные препараты, как ибупрофен и флюрбипрофен. Среди всех неселективных НПВП именно производные пропионовой кислоты отличаются наилучшей переносимостью.
Хорошо известен его выраженный анальгетический эффект, превышающий таковой при применении производных фенилуксусной кислоты (диклофенака), индолуксусной кислоты (индометацина). В этой связи «a priori» считалось, что у кетопрофена должна быть и плохая переносимость.
Возможно, поэтому Кетонал широко используется специалистами, занимающимися острыми болями, такими как хирурги, травматологи, стоматологи, гинекологи и онкологи, но реже — ревматологами. По данным П.С. Векшева и соавт. [7], для достижения оптимального обезболивания при минимально инвазивных операциях в 94,3% случаев достаточно использования Кетонала в дозе 100 мг 2–3 раза в день. В ходе более травматических операций применение Кетонала позволило значительно уменьшить нужную дозу наркотических анальгетиков [8]. В сравнительном исследовании различных НПВП в послеоперационном периоде Кетонал (300 мг/сутки, в/м) показал себя лучше по сравнению с диклофенаком (150–200 мг/сутки, в/м) и кеторолаком (90 мг/сутки, в/м), причем Кетонал также отличался лучшей переносимостью: частота побочных эффектов составила 4%, 31% и 14% соответственно [9,10]. Высокая эффективность и лучшая переносимость Кетонала отмечены при лечении болевого синдрома у пациентов с злокачественными заболеваниями [11]. При использовании Кетонала в гинекологии для обезболивания после эндоскопических операций наиболее эффективной формой являются таблетки форте по сравнению с суппозиториями и капсулами [12].
Врач–ревматолог в большинстве случаев имеет дело с хроническими заболеваниями суставов (артрит, артроз), когда пациенты вынуждены многие месяцы и годы непрерывно применять НПВП. Необходимая длительность приема НПВП и известный факт, что частота побочных реакций со стороны ЖКТ (язв слизистой желудка и 12–перстной кишки, кровотечений) на фоне приема НПВП выше у больных с поражением опорно–двигательного аппарата, чем у страдающих иными видами хронической боли [13], заставляют врача искать наиболее безопасные препараты. Однако селективные ингибиторы ЦОГ–2 при некоторых формах воспаления оказывают противовоспалительный эффект только в очень высоких дозах, когда происходит подавление синтеза и ЦОГ–1.
Кетонал, являющийся производным пропионовой кислоты и относящимся к категории наиболее безопасных НПВП, имеет короткий период полураспада (Т1/2=1–2 часа) и быстро абсорбируется и выводится [14]. Благодаря своей высокой липофильности, Кетонал легко проникает через гемато-энцефалический барьер и влияет на сигнальную передачу болевых stimuli на уровне задних рогов спинного мозга, что и обуславливает его центральное анальгезирующее воздействие.
Эти фармакодинамические свойства кетопрофена стали основой для его более широкого применения в ревматологической практике. Мы провели клинические и клинико-эндоскопические исследования, направленные на оценку эффективности и переносимости Кетонала у пациентов с высокой активностью ревматоидного артрита и болезнью Бехтерева при длительном использовании, а также у больных с артрозами. В рамках ряда специализированных клинических исследований было показано, что фармакокинетика Кетонала у молодежи и пожилых людей не имеет значительных отличий [15,16]. Кроме того, кетопрофен не оказывает заметного влияния на синтез протеогликанов хондроцитами в in vitro и in vivo исследованиях [17], что подтверждает его безопасность для суставного хряща.
По нашим данным, при назначении различных форм Кетонала частота развития положительного эффекта составила 87% при использовании таблетированной формы, 79% при использовании в/м инъекций и 100% при использовании Кетонала в виде 5% крема. Интересны данные J.S. Walker и соавт. [18], показавших, что у больных РА, «отвечающих» на кетопрофен, до назначения препарата отмечено достоверное увеличение концентрации фактора некроза опухоли–a и тенденция к увеличению уровня других провоспалительных цитокинов по сравнению с больными, «не отвечающими» на кетопрофен. Эти данные подтверждают, что выраженный противовоспалительный и анальгетический эффекты кетопрофена связаны не только с ЦОГ– опосредованной ингибицией синтеза простагландинов. Препарат оказывает быстрое и достоверное уменьшение боли и параметров, отражающих уровень воспаления в суставах.
В процессе клинико-эндоскопического исследования о результативности и переносимости Кетонала в различных формах у пациентов с активным ревматоидным артритом, принимающих Кетонал в форме суппозиториев (50 мг), таблеток форте (100 мг) или таблеток-ретард (150 мг) на протяжении трех месяцев, было выявлено, что Кетонал демонстрирует высокую анальгезирующую и противовоспалительную эффективность при отличной переносимости [19]. Частота эрозивных и язвенных поражений слизистой ЖКТ при применении различных НПВП была продемонстрирована на рисунке 2. Как видно, частота повреждений слизистой ЖКТ при использовании Кетонала сопоставима с таковой для селективных ЦОГ–2 ингибиторов.
Рис. 2. Частота повреждения слизистой ЖКТ на фоне использования НПВП
Таким образом, Кетонал продемонстрировал высокую эффективность в управлении суставной болью и воспалением у пациентов с хроническими заболеваниями суставов, а также хорошую переносимость. Этот препарат может успешно использоваться для длительного лечения, в том числе у пожилых пациентов.
1. Vane J.R. Inhibition of prostaglandin synthesis as a mechanism of action for the aspiei–like drugs. Nature, 1971; 231; 235–239.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты (перспективы применения в медицине). М., «Анко», 2000, 143 стр.
3. Crofford L.J., Lipsky P.E., Brooks P. и др. Основные биологические и клинические аспекты специфических ингибиторов циклооксигеназы-2. Arthr.Rheum., 2000; 43; 4–13.
4. Fitzgarald G.A., Partono C. The coxibs, selective inhibitors of cyclooxigenase–2. N.Engl.J.Med., 2001; 345;433–442.
5. Bannwarth B., Demotes–Mainard F., Schaeverbeke T. и др. Центральные анальгезирующие эффекты препаратов, подобных аспирину. Fund.Clin.Pharm., 1995; 9; 1–7.
6. McCormack K., Urguhat E. Корреляция между эффективностью нестероидных противовоспалительных препаратов в клинической модели боли и расслоением их противовоспалительных и анальгезирующих свойств в результатах на животных. Clin.Drug Invest., 1995; 9; 88–97.
7. Ветшев П.С., Чилингариди К.Е., Ипполитов Л.И. и др. Хирургический стресс при различных вариантах холецистэктомии. Хирургия, 2002, №3, стр. 4–10.
8. Ветшев П.С., Ветшева М.С. Принципы обезболивания в раннем послеоперационном периоде. Хирургия, 2002, №12, 49–52.
9. Кириенко П.А., Гельфанд Б.Р., Леванович Д.А. и др. Сравнительная оценка эффективности нестероидных противовоспалительных препаратов, применяемых для послеоперационного обезболивания. Consillium medicum, Хирургия №2, 2002.
10. Гельфанд Б.Р., Кириенко П.А., Леванович Д.А., Борзенко А.Г. Сравнительная оценка эффективности нестероидных противовоспалительных препаратов, использующихся для послеоперационного обезболивания. Вестник интенсивной терапии, 2002, №4, Послеоперационный период, стр. 83–88.
11. Новиков Г.А., Вайсман М.А., Прохоров Б.М. и др. Кетонал в лечении болевого синдрома у пациентов с распространенными формами злокачественных новообразований. Паллиативная медицина и реабилитация, №3, 2002, 48–51.
12. Айламазян Э.К., Ниаури Д.А., Зиятдинова Г.М. Экономическое обоснование применения Кетонала для обезболивания после эндоскопических вмешательств в гинекологии. Российский вестник акушера-гинеколога, №6, 2002, 51–53.
13. Janssen M., Dijkmans B., van der Sluijs F.A. «Проблемы верхних отделов ЖКТ и осложнения у пациентов с хроническими ревматическими заболеваниями по сравнению с другими хроническими патологиями». Br.J.Rheum., 1992., Vol.31: 747–752.
14. Williams R.L., Upton R.A. The clinical pharmacology of ketoprofen. J.Clin.Pharm., 1988; 28: 13–22.
15. Schattenkirchen M. Долговременная безопасность кетопрофена у пожилых пациентов с артритом. Scand.J.Rheum., 1991; 91 (Suppl.): 27–36.
16. Le Loet X. Безопасность кетопрофена у пожилых: проспективное исследование 20000 пациентов. Scand.J.Rheum., 1989; 83: 21–27.
17. Huber–Brunning O., Willbrinck B., Vanroy J., Vanderveen M.J. Potential influences of ketoprofan on human healthy and osteoarthritic cartilage in vitro. Scand. J.Rheum., 1989;18:29–32.
18. Walker J.S., Sheater-Rhode R.B. Carmody J.J. и др. Нестероидные противовоспалительные препараты при ревматоидном артрите и остеоартрите. Поддержка концепции «ответчик» и «неответчик». Arthr.Rheum., 1987; 11: 1944–1954.
19. Чичасова Н.В., Имаметдинова Г.Р., Каратеев А.Е. и др. Эффективность и безопасность кетопрофена (Кетонала) при ревматоидном артрите (клинико-эндоскопическое исследование). Научно-практическая ревматология, 2001; 1: 47–52.