При обострении подагры на пальце ноги внутримышечный обезболивающий укол может оказать значительное облегчение. Чаще всего используют препараты на основе нестероидных противовоспалительных средств, которые уменьшают боль и воспаление, позволяя пациенту вернуться к привычной активности.
Тем не менее, важно помнить, что такие уколы не устраняют основную проблему — повышение уровня мочевой кислоты в организме. Для эффективного контроля подагры требуется комплексный подход, включая изменение диеты и, при необходимости, применение препаратов для снижения уровня мочевой кислоты.
- Обострение подагры сопровождается сильной болью и воспалением в суставе, чаще всего в большом пальце ноги.
- Внутримышечные уколы обезболивающих средств, таких как нестероидные противовоспалительные препараты (НПВП), могут быстро облегчить состояние пациента.
- Процедура должна проводиться квалифицированным медицинским работником для минимизации риска осложнений.
- Важно учитывать противопоказания к использованию определённых препаратов, особенно при наличии сопутствующих заболеваний.
- После снятия остроты симптомов рекомендуется продолжение лечения для предотвращения дальнейших обострений подагры.
1. М.С. Елисеев. Новые подходы к диагностике и терапии подагры / М.С. Елисеев // Научно-практическая ревматология. – 2014. – № 2. – С.141-146.
2. F. Sivera, M. Anders, L. Carmona и др. Многонациональные рутинные рекомендации по диагностике и управлению подагрой: объединение систематического литературного анализа и мнений экспертной группы лечащих ревматологов в инициативе 3e // Ann. Rheum. Dis. 2014.
Том 2. № 73. С. 328-335.
3. Каратеев А.Е. Оценка риска желудочно-кишечных и сердечно-сосудистых осложнений, ассоциированных с применением нестероидных противовоспалительных препаратов в популяции СНГ / А.Е. Каратеев, Т.В. Попкова, Д.С. Новикова // Научно-практическая ревматология. – 2014. – № 6. – С. 600-606.
4. Ревматология. Российские клинические рекомендации / Под редакцией академика РАН Е.Л. Насонова. – М.: ГЕОТАР-Медиа, 2017. – 456 с.
5. Neogi T., Jansen T., Dalbeth N. et al. 2015 Gout classification criteria: an American College of Rheumatology / European League Against Rheumatism collaborative initiative. Ann. Rheum. Dis.
2015.
Том.
74 (10). С. 1789-1798.
6. Ф.М. Кудаева. Эффективность и безопасность кокстрала при лечении острого подагрического артрита / Ф.М. Кудаева, И.А. Якунина, В.Г. Барскова, В.А.
Насонова // Современная ревматология. – 2007. – № 1. – С. 55-58.
7. М.С. Елисеев. Нимесулид в терапии острой боли / М.С. Елисеев // Медицинский совет. – 2016. – №17. – С. 110-112.
8. Н.В. Чичасова. Использование кетопрофена (кетонал) в практике медицины / Н.В. Чичасова, Е.Л. Насонов, Г.Р. Имаметдинова // Фарматека. – 2003. – № 5. – С.16-21.
9. Bhala N., Emberson J., Merhi A. et al. Vascular and upper gastrointestinal effects of NSAIDs: meta-analysis of individual participant data from randomized trials // Lancet. 2013. Vol. 382. №. 9894.
С. 769-779.
Когда речь идет о лечении обострений подагры, особенно в области пальцев ног, важно понимать, что обезболивающие внутримышечные уколы могут оказать значительное влияние на качество жизни пациента. В таких случаях боль может быть интенсивной и изнуряющей, что затрудняет даже простые повседневные действия. Внутримышечные инъекции, такие как декстраксон или НПВП, позволяют быстро достичь обезболивающего эффекта, что особенно ценно при острых приступах.
Однако стоит заметить, что применение обезболивающих средств не является универсальным решением. Важно учитывать индивидуальные особенности пациента, а также стадию заболевания. Например, у некоторых людей могут возникать побочные эффекты от НПВП, такие как гастрит или почечные проблемы, что требует осторожности и предварительной оценки врачом. Поэтому перед применением данного метода важно проконсультироваться со специалистом, чтобы выбрать наиболее безопасный и эффективный подход.
Кроме того, следует помнить, что временное снятие боли при помощи уколов не устраняет основную проблему — уровень мочевой кислоты в организме. Поэтому наряду с обезболиванием необходимо оперативно работать над изменением образа жизни и назначением соответствующих медикаментов для контроля подагры. Имея комплексный подход к лечению, можно не только облегчить состояние пациента в момент обострения, но и предотвратить будущие приступы.
В начале XXI века подагра стала привлекать внимание врачей из-за роста распространенности заболевания и необходимости разработки адекватных мер по лечению и профилактике этого тяжелого заболевания. Подагра представляет собой метаболическое заболевание, проявляющееся нарушенным обменом пуринов и накоплением мочевой кислоты (МК), формированием кристаллов моноурата натрия и отложением их в органах мишенях.
Основное клиническое проявление подагры, с которым часто сталкиваются врачи в первичном звене здравоохранения, — острый подагрический артрит. Этот тип артрита является одним из наиболее серьезных видов ревматических заболеваний суставов.
Обычно болевой приступ начинается в ночное время или ранним утром сразу после вставания, чаще затрагивая первый плюснефаланговый сустав, с сопутствующей отечностью и покраснением кожи в области сустава, откуда и происходит название подагра, которое можно перевести как «нога в ловушке». Сильная боль ограничивает движения в воспаленном суставе, любое легкое прикосновение усугубляет болезненные ощущения. Первичные приступы могут длиться от 1–2 дней до 7–10 дней, и при отсутствии своевременного лечения они могут становиться гораздо продолжительнее, превращаясь в частые рецидивы. Характерно сокращение бессимптомного интервала, приступы становятся более выраженными, вовлекаются новые суставы, формируются тофусы в различных тканях — сначала единичные, затем множественные, развивается хронический артрит [1].
В недавно опубликованных международных рекомендациях по диагностике и лечению подагры [1,2], по мнению экспертов, основу терапии острого подагрического артрита составляют НПВП, которые являются препаратами первой линии, особенно в условиях поликлиники [3]. Однако четкой концепции, определяющей выбор конкретного нестероидного противовоспалительного препарата (НПВП) для купирования острой подагрической атаки, на сегодняшний день не существует.
На практике терапевт и ревматолог в поликлинике при острых подагрических артритах вынуждены назначать нестероидные противовоспалительные препараты (НПВП) с максимально быстрым эффектом для снятия боли и воспаления, обращая внимание на безопасность этих медикаментов с точки зрения побочных эффектов. Проблемы, связанные с сочетанием подагры с гипертонией, диабетом, ожирением и сосудистыми заболеваниями, усугубляют выбор НПВП. Таким пациентам эти лекарства предписываются на короткие курсы для быстрого купирования боли при остром подагрическом артрите [3].
В этой связи представляет интерес применение препарата кетопрофен (кетонал), который отличается наиболее быстрым началом анальгетического действия. Через 1–2 часа после введения концентрация препарата в плазме составляет 90 % и быстро нарастает в синовиальной жидкости, что позволяет применять кетонал для купирования приступа острой боли у больных подагрой. Наличие парентеральной лекарственных форм облегчает подбор для больного индивидуальной дозы и позволяет оптимизировать лечение больных в амбулаторных условиях.
Цель исследования заключается в оценке клинической эффективности терапии острого артрита у пациентов с подагрой на основе применения кетопрофена (кетонала).
В материалы исследования вошли 21 пациент (15 мужчин и 6 женщин) с установленным диагнозом подагры, обратившиеся в поликлинику с остропротекающим артритом, которые дали информированное согласие на участие в лечении. Диагноз подагры был основан на классификационных критериях, разработанных Американской ассоциацией ревматологов и утвержденных ВОЗ [4]. Гиперурикемия определялась согласно критериям EULAR (2006) [5]. Отбор пациентов проводился по следующим критериям: возраст старше 18 лет, острый подагрический артрит продолжительностью не более 3 недель, не более 4 пораженных суставов.
Критерии исключения из исследования: тяжелая тофусная подагра, сердечно-сосудистые осложнения в анамнезе, нарушения ритма, тяжелые сопутствующие заболевания желудочно-кишечного тракта, печени, почек, сердечная недостаточность, онкологический анамнез, а также больные, принимающие антикоагулянты, глюкокортикоиды, колхицин. На момент исследования пациенты не принимали другие НПВП. Кетопрофен (кетонал) назначали в дозе 2 мл (50мг/мл) внутримышечно 1 раз в день в течение 10 дней. Эффективность препарата оценивали до начала исследования, через 5 дней и по окончании терапии – через 10 дней.
Каждому пациенту проводилось полное клиническое обследование, включая антропометрические измерения (вес, рост, индекс массы тела (ИМТ)), общеклинические анализы крови и мочи, биохимическое исследование липидного профиля крови, уровень глюкозы, креатинина, мочевины, трансаминаз, ревматоидного фактора, С-реактивного белка, ультразвуковое исследование (УЗИ) почек и пораженных суставов. Вместе с клиническими данными оценивались артрологические тесты: интенсивность болевого синдрома в суставах при движении и в состоянии покоя с использованием 100-мм визуально-аналоговой шкалы (ВАШ), количество припухших суставов, оценка общего состояния пациента (ОСП) по шкале ВАШ.
Больному предлагалось оценить динамику боли по следующей шкале, которые применяются в ФГБНУ «НИИР им. В.А. Насоновой» [6]: 0 баллов – боль не уменьшилась; 1 балл – немного уменьшилась; 2 балла – уменьшилась; 3 балла – значительно уменьшилась; 4 балла – исчезла полностью.
Перед началом и после завершения курса терапии определялись следующие параметры [6]:
1) индекс припухлости суставов в баллах (0 – отсутствует припухлость, 1 – пальпируемая припухлость, 2 – видимая припухлость, 3 – выраженная припухлость);
2) гиперемия кожных покровов над суставом в баллах (0 – нет, 1 – есть);
3) суставной индекс в баллах (0 – отсутствие боли, 1 – боль при пальпации, о которой сообщает пациент, 2 – боль при пальпации, при которой пациент ощущает дискомфорт, 3 – боль при пальпации, заставляющая пациента отдернуть конечность).
Статистическую обработку данных осуществляли с помощью программного обеспечения Statistica 10.0 (StatSoft, USA). Оценивали размер выборки, среднюю, медиану, стандартное отклонение, процентили (25-й и 75-й процентили). Достоверность показателей определялась с помощью t-критерия Стьюдента, основанного на предположении, что сравниваемые выборки принадлежат к нормальным распределениям.
При наличии непараметрического распределения данных для сравнения двух независимых групп применялся U-критерий Манна — Уитни, для двух зависимых групп — критерий Вилкоксона. Различия считались статистически значимыми при уровне р.
Результаты. В выборке пациентов с подагрой преобладали мужчины (71,4 %) (См. Таблица 1).
Возраст больных колебался с 39 до 64 лет, средний возраст больных подагрой составил 57,2±11,07 года. Продолжительность заболевания подагрой у большинства больных колебалась от 1 года до 6 лет, медиана и интерквартильный размах длительности болезни – 4,2 [1;6,5], число атак в год – 2,23±0,75. Длительность последнего обострения составила 1,25±0,79 недели, количество поражённых суставов 3 [1;4].
В основном И плюснефаланговый сустав был поражен в 82 % случаев, суставы предплюсны — в 12 %, голеностопные — в 50 %, коленные суставы — в 30 %. Артрит локтевых и проксимальных межфаланговых суставов кистей наблюдался в 4 (19 %) случаях. У пациентов преобладало рецидивирующее течение болезни — 12 человек (57 %), хроническое — у 9 человек (43 %). У 5 (24 %) пациентов были обнаружены подкожные и внутрикожные тофусы.
У большинства пациентов выявлялась сопутствующая патология. Так, у 14 (67 %) больных была отмечена артериальная гипертензия, у 2 (10 %) – сахарный диабет 2-го типа. Анализ антропометрических данных показал, что 11(52 %) пациентов имели избыточную массу тела и 6 (28,5 %) – абдоминальное ожирение I и II степени. Более чем у половины больных выявлялся остеоартроз.
Уровень мочевой кислоты в сыворотке крови варьировался от 383 до 564, среднее значение составило 469,18 ± 58,27 ммоль/л. На момент исследования пациенты не принимали других НПВП, и лишь половина из них регулярно использовала аллопуринол.
Клиническая характеристика пациентов с подагрой до начала терапии.
Артрозилен капсулы
Артрозилен капсулы (кетопрофен): Нестероидный противовоспалительный. капсулы.04 мая 2016 г..
Эторикоксиб: нестероидные противовоспалительные препараты (НПВП). Таблетки с пленочной оболочкой.
07 сент. 2019 г..
Эторикоксиб: нестероидный противовоспалительный препарат (НПВП). Пленочные таблетки.
г.
Дексаметазон таблетки — ФК Обновление
Дексаметазон таблетки (дексаметазон): Кортикостероид, глюкокортикоид.23 марта 2017 г..Диклак раствор (диклофенак): Нестероидный противовоспалительный. Раствор для инъекций.01 марта 2016 г..Дикловит гель (диклофенак): Нестероидный противовоспалительный. Гель.04 сент.
2017 г. Дикловит (диклофенак) суппозитории: Нестероидный противовоспалительный. Ректальные суппозитории. 21 сент.
2016 г..Диклоген таблетки (диклофенак): Нестероидный противовоспалительный. Таблетки.01 окт. 2011 г..
Диклофенак: нестероидный противовоспалительный препарат (НПВП). Раствор для внутримышечного введения.
г.
Медикаментозное купирование острого приступа подагры
В статье рассмотрены механизмы развития подагры, критерии ее диагностики и способы лечения. Для локальной терапии острого подагрического артрита часто используют периартикулярное или внутрисуставное (при обязательном исключении септического артрита) введение глюкокортикостероидов, в частности Дипроспана. Применение Дипроспана имеет большие преимущества перед другими глюкокортикоидами из-за надежного, быстрого и длительного действия, хорошей переносимости, а также более низкой стоимости лечения.
- КЛЮЧЕВЫЕ СЛОВА: подагра, диагностика, терапия, внутрисуставные инъекции пролонгированных глюкокортикостероидов, Дипроспан
В статье анализируются механизмы развития подагры, ее диагностические критерии и методы лечения. Для местной терапии острого подагрического артрита часто применяются периартикулярные или внутрисуставные инъекции глюкокортикостероидов, в частности Дипроспана. Использование Дипроспана предоставляет много преимуществ перед другими глюкокортикоидами благодаря его надежному, быстрому и длительному действию, хорошей переносимости и более низкой цене лечения.
Таблица 1. Характеристика ГКС, применяемых для локальной инъекционной терапии острого подагрического артрита
Таблица 2. Дозировка и процедура введения ГКС в суставы.
Подагра — это заболевание, связанное с нарушениями пуринового обмена, которое проявляется повышением уровня мочевой кислоты в крови (гиперурикемией) и отложением уратов в суставах и/или околосуставных тканях, почках и других органах [1–3].
Подагрой страдают около 0,1% населения. Это преимущественно лица среднего или старшего возраста (80–90%) с предшествующей в течение 20–30 лет бессимптомной гиперурикемией. Установлено, что мужчины болеют подагрой в 20 раз чаще.
Европейская лига по борьбе с ревматизмом (EULAR) определяет гиперурикемию как уровень мочевой кислоты (МК) выше 360 мкмоль/л (6 мг/дл). Гиперурикемия может быть вызвана ожирением, артериальной гипертензией, приемом медикаментов (диуретиков, низких доз аспирина, аминофиллина, диазепама, дифенгидрамина, допамина, препаратов с кофеином, витаминов B12 и C, свинца), генетическими аномалиями и употреблением алкоголя.
Накопление МК в крови может быть обусловлено либо ее высокой продукцией (повышен синтез эндогенных пуринов), либо низкой экскрецией, либо сочетанием этих механизмов. Первичная гиперпродукция связана с дефектами ферментативной системы синтеза МК (недостаточность гипоксантин-гуанинфосфорибозилтрансферазы и повышение активности рибозофосфатпирофосфокиназы). Вторичная гиперпродукция – с повышенным распадом клеток при гемобластозах, парапротеинемиях, хроническом гемолизе, проведении химиотерапии. Гиперурикемия часто сопутствует псориазу [4].
При кристаллизации мочевой кислоты образуются микротофусы (агрегации кристаллов) в синовиальной оболочке и хряще. Порой из-за травмы, повышения температуры в суставе или изменения концентрации мочевой кислоты в крови или синовиальной жидкости микротофусы подвергаются разрушению, и кристаллы попадают в суставную полость. Синовиальные клетки вырабатывают цитокины (интерлейкины 1, 6, 8 и фактор некроза опухоли альфа), которые привлекают нейтрофилы. Иммуноглобулины и компоненты комплемента опсонизируют ураты, усиливая фагоцитарную активность нейтрофилов.
Снижение экскреции мочевой кислоты может быть связано с образованием кристаллов уратов в почках на фоне высокого уровня их выделения (больше 800 мг/сут) при первичном гиперпродуцировании мочевой кислоты. Вследствие этого развивается уратный тубулоинтерстициальный нефрит [5].
Клиническая картина подагры – наличие тофусов, поражение суставов и почек (интерстициального нефрита и нефролитиаза). Известно, что подагра оказывает существенное влияние на развитие атеросклеротического процесса и, следовательно, сердечно-сосудистых заболеваний, что определяет прогноз данного заболевания [6, 7].
Дебют подагры обычно определяется как первый приступ острого подагрического артрита; однако до его начала может наблюдаться длительное время гиперурикемия, которая способствует образованию почечнокаменной болезни [8, 9].
Острый подагрический артрит провоцируется травмой, физической нагрузкой, посещением сауны, эмоциональным стрессом, изменением диеты (как перееданием, так и голоданием), употреблением алкогольных напитков, инфекцией, хирургическими вмешательствами, применением лекарств (наиболее часто тиазидных диуретиков, химиотерапевтических противоопухолевых средств). В дебюте заболевания нередко наблюдается поражение одного сустава нижних конечностей, причем у 50% больных поражен первый плюснефаланговый сустав (ПФС).
Атаки подагры чаще всего возникают в ночное время, проявляясь стремительным увеличением покраснения и температуры в суставе, а также отеком и болевыми ощущениями. Воспалительный процесс может затрагивать мягкие ткани, создавая признаки воспаления подкожной клетчатки или флебита. Телесная температура может подниматься до фебрильных значений. Обычно приступ длится от нескольких дней до нескольких недель, при этом сустав остается без деформаций.
Чтобы изучить экскрецию мочевой кислоты, нужно провести трехдневную диету, исключающую продукты с высоким содержанием пуринов (мясо, бульоны, рыба, птица, бобовые, кофе, чай, алкоголь, пиво). Затем измеряют объем суточной мочи, pH, а также уровень мочевой кислоты и креатинина как в моче, так и в сыворотке крови. В норме за сутки выделяется от 300 до 600 мг (1,8–3,6 ммоль/л) мочевой кислоты.
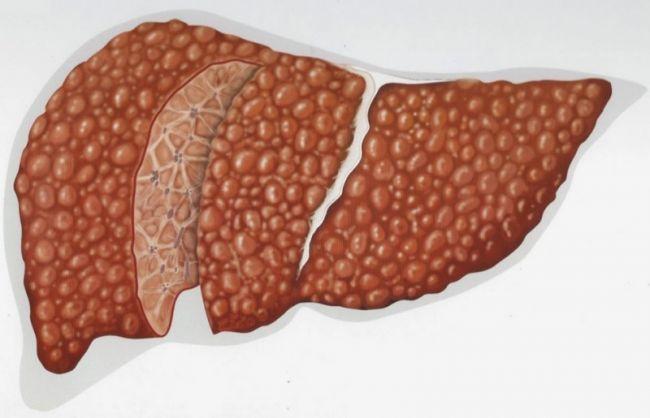
При рентгенологическом исследовании суставов стоп в случае хронического подагрического артрита наблюдаются краевые костные или кистовидные образования правильной формы с четкими, иногда склерозированными контурами (симптом пробойника). С течением времени выраженная деструкция отмечается не только на субхондральном участке кости, но и в эпифизе и даже в диафизе, развивается внутрисуставной остеолиз. Обычно данные изменения наиболее выражены в суставах стоп (в первую очередь в суставах большого пальца) [10].
На сегодняшний день чаще всего применяются критерии подагрического артрита, разработанные S. Wallace и коллегами, одобренные Всемирной организацией здравоохранения в 2000 году [11]:
А. Наличие характерных мононатриевых уратных кристаллов в синовиальной жидкости.
B. Подтвержденный тофус (по результатам химического анализа или поляризационной микроскопии).
C. Наличие 6 из 12 клинических, лабораторных и рентгенологических признаков:
- максимальная степень воспаления сустава в первый день;
- более одного эпизода артрита;
- моноартрит;
- покраснение суставов;
- боль и воспаление первого плюснефалангового сустава;
- асимметричное воспаление плюснефаланговых суставов;
- одностороннее поражение тарзальных суставов;
- подозрение на наличие тофусов;
- гиперурикемия;
- асимметричное воспаление суставов;
- субкортикальные кисты без эрозий по рентгенографическим данным;
- отсутствие микроорганизмов в культуре синовиальной жидкости.
Необходимо отметить, что у 95,5% больных подагрой пять и более признаков отмечаются уже на ранней стадии заболевания.
Комплексное лечение подагры включает сочетание немедикаментозных и медикаментозных подходов, целью которых является снижение уровня мочевой кислоты в крови и предотвращение повреждения разнообразных органов и систем. При подагрическом артрите назначается специализированная диета (стол № 6), исключающая продукты, богатые пуринами, с ограничением натрия и жиров. В рацион добавляют щелочные минеральные воды и цитрусовые для улучшения выведения уратов. Суточное количество свободной жидкости увеличивается до 2,5 литров, если нет противопоказаний со стороны сердечно-сосудистой системы.
При отсутствии противопоказаний средствами выбора являются нестероидные противовоспалительные препараты (НПВП) в полных терапевтических дозах: индометацин (25–50 мг четыре раза в день), напроксен (500 мг два раза в день), диклофенак (25–50 мг четыре раза в день), нимесулид (100 мг два раза в день), эторикоксиб (Аркоксиа) (120 мг в день). При неэффективности НПВП или наличии противопоказаний (например, лечение варфарином) применяют колхицин (0,5–0,6 мг внутрь каждый час до купирования острого артрита). Этот препарат не следует назначать пациентам с тяжелым поражением почек, при заболеваниях ЖКТ, сердечно-сосудистой системы, поскольку увеличивается риск тяжелых побочных эффектов. Абсолютным противопоказанием для назначения колхицина является сочетание почечной и печеночной недостаточности, выраженное снижение скорости клубочковой фильтрации и внепеченочная билиарная обструкция.
Если применение нестероидных противовоспалительных препаратов (НПВП) или колхицина невозможно, назначаются глюкокортикостероиды (ГКС) в следующих дозах: преднизолон в первый день в дозе 40-60 мг (в таблетках) с последующим уменьшением дозы на 5 мг через день; триамцинолон – 60 мг внутримышечно, введение при необходимости повторяют через 24 часа; метилпреднизолон – 50-150 мг внутривенно капельно с учетом применения малой пульс-терапии: однократно 250-500 мг, с возможностью повторной инъекции через 24 часа.
Важно отметить, что использование ГКС (внутривенно или внутримышечно) может спровоцировать синдром рикошета и различные побочные эффекты, что может потребовать наблюдения пациента в стационаре. В связи с этим рассматривается оправданность одновременного применения небольших доз колхицина (1–2 мг в сутки) [9].
Для локальной инъекционной терапии острого подагрического артрита используют периартикулярное или внутрисуставное (при обязательном исключении септического артрита) введение ГКС.
Характеристика глюкокортикостероидов, применяемых для локальной инъекционной терапии острого подагрического артрита, приведена в табл. 1. Гидрокортизона ацетат (короткодействующий ГКС) выпускается в виде микрокристаллической суспензии в флаконах по 5 мл с содержанием 125 мг препарата. Из-за короткого действия его применение стало уменьшаться, и сейчас он в основном используется для инфильтрации периартикулярных тканей или при минимальных проявлениях синовита.
Кеналог 40 – водная кристал- лическая суспензия синтетического фторированного ГКС (триамцинолона ацетонида). Выпускается в ампулах по 1 и 5 мл в концентрации 40 мг/мл. Противовоспалительное действие наступает через один – три дня после внутрисуставной инъекции и продолжается в среднем до одного месяца. Следует отметить, что препарат чаще других ГКС вызывает атрофию кожи и подкожной жировой клетчатки, некроз сухожилий, связок, мышц.
Дипроспан& является пролонгированной формой бетаметазона, фторированного аналога метилпреднизолона. Выпускается в ампулах по 1 мл, содержащих 2 мг бетаметазона динатрия фосфата и 5 мг бетаметазона дипропионата.
Первая составляющая (хорошо растворимый и быстро всасывающийся эфир) обеспечивает оперативный эффект, в то время как вторая (медленно абсорбирующаяся депо-фракция) – продленный. Поэтому действие Дипроспана начинается в течение 2–4 часов после внутрисуставного введения и продолжается до трех недель.
Еще одно достоинство препарата заключается в том, что кристаллы суспензии микронизированы. Так, концентрация кристаллов в 1 мл Дипроспана равна 6,4 мг/мл, в то время как в 1 мл Кеналога – 40 мг/мл. Кроме того, средний размер кристаллов Дипроспана составляет от 2 до 6 мкм, тогда как величина кристаллов Кеналога 40 – около 12 мкм. Как следствие, внесуставные инъекции практически безболезненны и не сопровождаются осложнениями. Это позволяет применять Дипроспан без анестетика.
Опыт применения Дипроспана и Кеналога 40 у пациентов с подагрическим артритом продемонстрировал более высокую эффективность первого. Использование Дипроспана позволило снизить дозу НПВП, тем самым уменьшив риск возникновения НПВП-гастропатии [9].
Следовательно, местное применение Дипроспана имеет большие преимущества перед другими ГКС.
Согласно рекомендациям EULAR по диагностике и терапии подагры, внутрисуставные инъекции пролонгированных ГКС считаются наиболее безопасными и эффективными. Дозировка и частота их введения в крупные, средние и мелкие суставы представлены в табл. 2.
Перспективным вариантом для купирования острого приступа подагры является применение средств биологической терапии. Исследования действия анакинры и канакинумаба, рекомбинантных растворимых антагонистов интерлейкина 1 человека, показали, что блокирование интерлейкина 1 может иметь клиническое значение при данной патологии [9, 10]. В частности, при подкожном введении препарата по 300 мг в сутки (инъекции выполнялись трижды) наблюдалось быстрое купирование подагрической атаки, при этом негативных эффектов не зафиксировано. Следовательно, в случае неэффективности традиционных методов (НПВП, колхицина, ГКС) возможно использование биологических препаратов.
Таким образом, раннее распознавание подагрического артрита и правильная медикаментозная тактика помогут сохранить трудоспособность пациентов на долгие годы и улучшить прогноз заболевания.
- КЛЮЧЕВЫЕ СЛОВА: подагра, диагностика, лечение, внутрисуставные инъекции пролонгированных глюкокортикостероидов, Дипроспан
Обезболивающий внутримышечный укол при обострении подагры на пальце ноги
Мы в соцсетях. Применение Кетонала для устранения острого приступа подагры.
re>string(5) «19100» 18 марта 2006
- Шостак Н.А. 1 ,
- Клименко А.А. 1, 2 ,
- Хоменко В.В.
РНИМУ им. Н.И. Пирогова Минздрава России, Москва, Россия. ГБУЗ «ГКБ № 1», Нальчик, Россия
Для цитирования: Шостак Н.А., Клименко А.А., Хоменко В.В. Применение Кетонала для лечения острого приступа подагры. РМЖ. 2006;5:412.
Подагра – это хроническое заболевание, вытекающее из расстройства обмена мочевой кислоты, клинически проявляющееся рецидивирующими артритами, образованием подагрических узлов (тофусов) и поражением внутренних органов [4,5].
Согласно МКБ Х пересмотра рубрика «подагра» (М10) включает: • Идиопатическая подагра (М10.0) • Свинцовая подагра (М10.1) • Лекарственная подагра (М10.2) • Подагра, обусловленная нарушением почечной функции (М10.3) Другие кристаллические артропатии (М11) подразделяются на наследственные, идиопатические и артропатии при других заболеваниях (табл. 1).
Распространенность подагры варьируется в различных регионах и во многом зависит от питания, составляя в среднем 0,1%, соотношение мужчин и женщин (фертильного возраста) – 9:1 [1,3]. Выделяются 4 клинических формы этого заболевания: • острый подагрический артрит, • межприступная подагра, • хронический рецидивирующий артрит, • хроническая тофусная подагра.
Лечение острой подагрической атаки основывается на использовании нестероидных противовоспалительных препаратов (НПВП). Обезболивающая, противовоспалительная активность, связанная с подавлением синтеза ПГ посредством ингибирования циклооксигеназы (ЦОГ) делают абсолютно очевидным назначение НПВП, как препаратов выбора.
Помимо ингибирования ЦОГ, важны и другие механизмы действия НПВП: • подавление функции нейтрофилов и взаимодействия лейкоцитов с эндотелием сосудов; • угнетение активации фактора транскрипции, регулирующего синтез «провоспалительных» веществ ИЛ-1, ИЛ-6, ИЛ-8, ФНО-a. Современным НПВП является кетопрофен (Кетонал), производное пропионовой кислоты. Его противовоспалительное действие выражается не только в ингибировании простагландинов (ПГ) на уровне циклооксигеназы; он также ингибирует липооксигеназу, обладает антибрадикининовой активностью и стабилизирует лизосомальные мембраны.
При внутреннем приеме препарат быстро и полностью абсорбируется из пищеварительного тракта, достигая максимальной концентрации крови через 1-2 часа. Кетонал хорошо проникает в синовиальную жидкость и соединительные ткани. Значительные уровни концентрации достигаются всего через 15 минут после внутримышечного введения 100 мг кетопрофена.
Важным преимуществом препарата является то, что он представлен различными лекарственными формами: капсулами, таблетками форте и ретард, раствором для внутримышечных инъекций, кремом и суппозиториями. Кетонал обладает «сбалансированной» активностью в отношении ингибиции ЦОГ-1 и ЦОГ-2, что позволяет оптимально сочетать высокую эффективность с хорошей преносимостью, сравнимой, по данным ряда авторов, с переносимостью селективных НПВП [2].
Исследователи связывают сильный анальгезирующий эффект Кетонала с его известным воздействием на центральную нервную систему, которое происходит на уровне задних рогов спинного мозга, а также через влияние на таламические центры болевой чувствительности. Это, вероятно, связано с угнетением синтеза простагландинов в центральной нервной системе [2].
Пирогова на кафедре факультетской терапии им. акад. А.И. Нестерова РГМУ проводилось изучение эффективности и безопасности кетопрофена (Кетонал форте, фармацевтическая компания «Лек») 300 мг в сутки у 29 больных (мужчин) с острым приступом подагры (впервые возникшим – 10 и рецидивирующим – 19 человек) в возрасте от 29 до 68 лет.
Длительность заболевания варьировала от 1 месяца до 5 лет. Из обследованных пациентов у 10 был диагностирован острый (впервые проявившийся) подагрический артрит, у 18 – хронический рецидивирующий артрит, у 1 – хроническая тофусная подагра. Острый подагрический артрит проявился как моноартрит у 13 людей, олигоартрит у 11, в то время как 5 имели полиартрит (рис. 1).
Предшествующая терапия НПВП включала диклофенак натрия (7 пациентов), нимесулид [2], ибупрофен [4], пироксикам [6]; 16 человек принимали аллопуринол в дозах от 50 до 200 мг в сутки. Всем исследуемым назначался Кетонал в дозе 100 мг трижды в день на протяжении 7 дней.
Клиническая эффективность и переносимость лечения оценивались до начала лечения, спустя 24 часа и через 7 дней по следующим параметрам: 1. Боль в покое по визуально-аналоговой шкале (ВАШ), в мм. 2. Функциональная недостаточность суставов по ВАШ, в мм.
Эффективность лечения оценивалась как пациентами, так и врачом по следующим критериям: отсутствие результата, удовлетворительный результат, выраженный положительный результат. Критериями исключения выступали непереносимость НПВП и обострение язвенной болезни желудка или двенадцатиперстной кишки, а также наличие ранее зафиксированных желудочно-кишечных кровотечений.
Все больные завершили курс лечения Кетоналом. Динамика клинических показателей у 29 больных с острым приступом подагры представлена в таблице 2, на рисунках 2 и 3. Было установлено, что у всех пациентов до начала лечения отмечался выраженный болевой синдром, который в среднем составил 80,0±2,3 мм по ВАШ, функциональная недостаточность суставов значительной степени (среднее значение по ВАШ 77,2±1,8 мм).
По окончании 7-дневного курса лечения была отмечена значительная положительная динамика оцененных клинических показателей: уровень болевого синдрома снизился на 80,9%, а функциональная недостаточность уменьшилась на 82,3%. Врачебная оценка эффективности терапии показала заметное улучшение состояния здоровья у 26 пациентов (89,7%).
Из 29 пациентов положительный эффект был отмечен у 2 человек (6,9%), тогда как у 1 пациента (3,4%) наблюдалась недостаточная эффективность терапии. В целом, переносимость Кетонала оказалась на удовлетворительном уровне. У всего лишь 4-х пациентов (13,8%) возникли побочные эффекты, проявляющиеся в виде дискомфорта и болей в области живота, а также изжоги, при этом отмена препарата не потребовалась, так как реакции прошли самостоятельно. Таким образом, у врачей теперь есть в арсенале современное и высокоэффективное средство — Кетонал, который в дозировке 300 мг в сутки демонстрирует выраженное противовоспалительное и анальгезирующее действие при остром приступе подагры, а его высокая безопасность позволяет рекомендовать данное средство для лечения острого подагрического артрита.
Литература. 1. Кобалава Ж.Д., Котовская Ю.В., Толкачева В.В., Караулова Ю.Л. Мочевая кислота- маркер и/или новый фактор риска сердечно-сосудистых осложнений. Клиническая фармакология и терапия 2002; 11(3):5-7. 2. Насонов Е.Л., Чичасова Н.В., Шмидт Е.И.
Перспективы использования неселективных нестероидных противовоспалительных средств (на примере кетопрофена) и селективных ингибиторов ЦОГ-2 в медицинской практике. Русский медицинский журнал 2002;10(22):1014-1017. 3. Мухин Н.А. Подагра – это только заболевание суставов? Клиническая фармакология и терапия 1994;1:31-33. 4. Butler R., Morris A., Belch J. и др. Аллопуринол нормализует эндотелиальную дисфункцию у диабетиков 2 типа с легкой гипертензией.
Hypertension 2000; 35:746-751. 5. Johnson R.J., Kivlighn S.D., Kim Y.G. et al.: Reappraisal of the pathogenesis and conseguences of hyperuricemia in hypertension, cardiovascular disease, and renal disease. Am. J. Kidney Dis. 1999:33(2):225-348.
Компрессы
Димексид является наиболее популярным препаратом для приготовления компрессов. Он применяется в качестве вспомогательного средства в лечении подагры, и существует несколько рекомендаций для его правильного использования:
- препарат следует смешать с водой в равных частях;
- в полученной смеси необходимо намочить марлю, прикладывать к пораженному суставу и накрыть пленкой;
- после этого компресс дополнительно обматывается хлопчатобумажной тканью и шерстяным шарфом;
- снимать компресс рекомендуется спустя 30 минут.
Курс лечения может длиться от 10 до 90 дней, и отзывы о его эффективности достаточно положительные. Однако в период острого приступа делать компрессы с Димексидом не рекомендуется.
Народные методы
Приготовить обезболивающие средства можно и дома, используя то, что найдется под рукой. Вот несколько рецептов.
Это вещество широко применяется в кулинарии, но немногие знают о его лечебных свойствах.
Желатин участвует в восстановлении хрящей, делает суставы более эластичными и подвижными.
Препарат также можно использовать для настоев на ночь:
- 1 чайная ложка вещества помещается на марлю, предварительно смоченную в воде.
- Компресс прикладывается к заболевшей области и фиксируется полиэтиленовой пленкой.
Курс лечения составляет одну неделю.
Также желатин используется для изготовления настойки. Необходимо залить немного вещества половиной стакана воды (125 мл). Пусть постоит до тех пор, пока ингредиент не набухнет. После долить еще столько же воды, размешать. Настойку пить примерно месяц перед последним приемом пищи.
Чеснок способен облегчить боли благодаря улучшению кровообращения в пораженном участке и выводу токсинов из организма.
Для приготовления средства нужно взять 400 г чеснока и измельчить с помощью мясорубки. После переложить в глубокую посудину и залить растительным маслом. Хорошенько перемешать и выложить на марлю, чтобы масло стекло. Через 8-10 часов добавить лимонный сок. Принимать лекарство по 1 ч.л. перед каждым приемом пищи, растворяя его в молоке.
Лавровый лист
Чеснок помогает также и в очищении организма от избытка мочевой кислоты. Он используется для приготовления лечебного настоя: 4 г листьев заливаются 300 мл воды, доводятся до кипения и настаиваются в течение 4 часов. После этого настой нужно процедить и пить в течение дня, делая это каждый час.
Приготовление настойки лучше производить в посуде с эмалированным покрытием.
Настойка коровяка на водке
2 ст.л. коровяка скипетровидного соединить с 500 мл водки. Поставить в темное место на 14 дней. После втирать в пораженный участок тела.
Рецепт с дрожжами
Для приготовления компресса 100 г обычного пшена следует измельчить в муку. Смешать с 1 ч. ложкой соли и дрожжей, добавляя воду до получения теста средней консистенции. Затем формируется компресс, который нужно менять каждые два часа. Продолжать процедуру до полного исчезновения боли.
Активированный уголь
Измельчить таблетки так, чтобы получилось 125 г порошка. Смешать его с 1 ст.л. льняных семечек. Залить все это теплой водой так, чтобы получилось кремообразное средство. Наложить на больное место, сверху обернуть фольгой и мягкой тканью. Делать так каждый день на ночь до тех пор, пока боль полностью не уйдет.
Ванны с травами
Теплые ванны, в которые добавляются розмариновое масло и отвар крапивы, оказывают положительное влияние. Масло можно приобрести в аптеках или специализированных магазинах. Для приготовления отвара нужно 8 ст. ложек измельченного растения залить 3 литрами воды, довести до кипения, убрать с плиты и оставить настаиваться. Пораженные участки тела можно погружать в теплую ванну на 15 минут.
Курс лечения включает 20-25 ванн.