Объем простаты в 35 см³ и затемнение размером 25 на 13 мм можно сопоставить, но прямой пропорциональности между ними нет. Чтобы оценить, какое значение может иметь затемнение, нужно учитывать плотность тканей и другие параметры.
Затемнение может указывать на наличие определенных изменений в тканях простаты, таких как воспаление или опухолевые процессы, и требует дальнейшего обследования для точной интерпретации. Важно проконсультироваться с врачом для более детального анализа ситуации.
- Объем простаты составляет 35 см³.
- Размер затемнения – 25 мм на 13 мм.
- Необходимость расчета объема затемнения для диагностики.
- Важность соотношения размеров затемнения и объема простаты.
- Рекомендации по дальнейшим обследованиям и анализам.
Начальное воодушевление, связанное с применением трансректального ультразвукового исследования (ТРУЗИ) простаты для раннего выявления и определения стадии рака, существенно снизилось. В настоящее время ТРУЗИ чаще всего используется для выполнения биопсии простаты и по определённым показаниям, включая оценку мужского бесплодия и диагностику а также дренирование абсцессов предстательной железы [ 1 , 2 ]. Данный метод прекрасно подходит для исследования семенных пузырьков при проблемах с бесплодием, болезненных ощущениях в области промежности и гематоспермии [ 3 ]. Трансабдоминальное УЗИ простаты, проводимое через наполненный мочой мочевой пузырь, имеет ограниченную диагностическую ценность, но может быть использовано для оценки размеров простаты.
Техника визуализации
При трансабдоминальном исследовании простата визуализируется через наполненный жидкостью мочевой пузырь (рис. 15.1). Секторный датчик с частотой 3,5–4,0 МГц располагается в нижней части живота, чуть выше лобкового симфиза, с направлением звукового луча вниз. Простата рассматривается в поперечной и продольной плоскостях. Определяются размеры простаты и могут быть замечены аномалии, такие как кальцификации.
Трансректальный подход позволяет использовать высокочастотные датчики 5–10 МГц, обеспечивающие наиболее детальное УЗИ. Если планируется трансректальная биопсия, пациенту обычно проводят премедикацию антибиотиками. Никакой другой подготовки пациента, такой как клизма, обычно не требуется.
Пациента укладывают на левый бок, сгибая оба колена к груди, а голова располагается на подушке. Пальцевое ректальное исследование производится для оценки размеров простаты и выявления возможных отклонений. Эндоректальный датчик обильно смазан УЗ-гелем и помещён в презерватив, который также дополнительно обработан УЗ-гелем.
Зонд осторожно вводят в прямую кишку, направляя кончик сначала к крестцу, следуя изгибу прямой кишки. Большинство эндоректальных датчиков имеют секторный формат с концевым пламенем. Линейные преобразователи с боковым огнём обеспечивают превосходные изображения, но не могут использоваться для прямой трансректальной биопсии.
Исследуются простата, семенные пузырьки и перипростатические ткани в поперечной и сагиттальной плоскостях. Для выявления сосудистых изменений, связанных с раком простаты и воспалительными процессами, может применяться цветная допплерография [ 4 ]. Обычно изображения рассматриваются в перевёрнутом виде, где преобразователь находится внизу кадра (рис. 15.2). Правая часть тела пациента представлена с левой стороны изображения.
Поскольку объем простаты составляет 35 см³, необходимо рассмотреть размер затемнения 25 на 13 мм в контексте соотношения объемов. Для начала, важно понимать, что размеры затемнения можно использовать для оценки своего объема. В данном случае мы имеем правооугольник с размерами 25 и 13 мм, что позволяет вычислить его площадь. Площадь данного затемнения составит 325 мм².
Для перевода этой площади в объем, необходимо учесть среднюю толщину затемнения. Если предположить, что затемнение имеет определенную глубину, например, 10 мм, то мы можем перемножить площадь на эту толщину. В итоге получим 325 мм² * 10 мм = 3250 мм³, что равняется 3,25 см³. Это позволяет нам осознать, что затемнение занимает относительно небольшую часть общего объема простаты.
Таким образом, затемнение в 3,25 см³ составляет примерно 9,29% от общего объема простаты в 35 см³. Это соотношение может служить важным индикатором для дальнейшей диагностики и мониторинга состояния простаты. Следовательно, важно учитывать эти данные совместно с другими клиническими показателями для более точной оценки состояния пациента.
Рисунок 15.1. Трансабдоминальное УЗИ простаты. Срединная сагиттальная проекция через заполненный мочевой пузырь (b) показывает увеличенную простату (P) у самого основания мочевого пузыря. Отверстие уретры (стрелка) представлено в виде V-образной выемки в предстательной железе.
Рисунок 15.2. Трансректальное УЗИ простаты. A. Поперечное изображение простаты отображается в перевёрнутом виде, при этом интраректальный датчик (Т) находится внизу кадра. Такая ориентация соответствует изображению простаты на КТ или МРТ в положении на спине. Правая сторона пациента (R) находится слева от изображения.
Сканирование средней части простаты демонстрирует, что нормальная периферическая зона (p) чётко ограничена и имеет более высокую эхогенность по сравнению с гипертрофированной внутренней частью железы (I). Хирургическая капсула обозначена стрелками. Стенка прямой кишки (стрелка) видна рядом с датчиком. Курсоры (+) показывают поперечный размер железы. Л, левый бок пациента.
Б. Поперечное изображение, полученное ближе к основанию простаты у другого пациента, показывает четкое отграничение периферической зоны (р) от внутренней железы. Сравните ( A ) и ( B ) и заметите, что периферийная зона тоньше у основания и толще возле вершины. В предстательной железе обоих мужчин наблюдаются изменения внутренних желез при ДГПЖ.
Рисунок 15.3. Анатомия простаты. В изображении представлены анатомические особенности предстательной железы в сагиттальной и поперечной плоскостях. (Адаптировано с разрешения Brant WE, Helms CA. Основы диагностической радиологии. Lippincott-Williams Wilkins, Балтимор, 1999.)
Анатомия
Простата имеет форму округлой перевернутой пирамиды и располагается на мочеполовой диафрагме, сразу за лобковым симфизом ( рис. 15.3 ). Более широкое основание простаты поддерживает основание мочевого пузыря (от основания к основанию). Суженная вершина опирается на мышечную мочеполовую диафрагму.
Семенные пузырьки располагаются в заднем пространстве между мочевым пузырем и простатой. Эти структуры представляют собой извитые трубки, свёрнутые в дольчатый мешок (рис. 15.4). Конечная ампулярная часть семявыносящего протока проходит медиальнее семенного пузырька и соединяется с ним, формируя семявыбрасывающий проток (см. рис.
15.6 ). Семявыделительные протоки проходят от верхнелатерального к нижнемедиальному направлению в верхней половине простаты и впадают в уретру в области верумонтана. Уретра проходит через переднюю часть простаты по дугообразному пути от шейки мочевого пузыря к верхушке простаты. На поперечном сечении уретра имеет подковообразную форму с задним гребнем, образующим verumontanum . В средней части верумонтана находится слепой мешочек диаметром 6 мм — маточка . Маточка – это мюллеров остаток, образующий матку и влагалище у женщин. Простатические протоки впадают на всю длину внутрипростатической уретры. Простата покрыта тонкой, но прочной фиброзной капсулой, окружена жиром и выступающими сплетениями перипростатических вен .
Предстательная железа делится на три анатомические зоны и переднюю нежелезистую область (рис. 15.3). Зоны простаты можно представить как перчатку ловца, держащего мяч для софтбола. «Рукавица» располагается сзади и соответствует периферической зоне (ПЗ). ПЗ у основания простаты тонкая, наподобие пальца перчатки ловца.
ПЗ становится толще к верхушке, напоминая нижнюю часть перчатки. Она охватывает лишь заднелатеральную область прямой кишки и не распространяется вокруг всего объёма железы. ПЗ содержит примерно 70% железистой ткани. Софтбол соответствует «внутренней железе», состоящей из периуретральной переходной зоны (TZ) и центральной зоны пирамидальной формы (CZ).
ТЗ составляет только 5% от общей железистой ткани у молодых мужчин, но является местом доброкачественной гипертрофии предстательной железы (ДГПЖ) и существенно увеличивается у большинства пожилых мужчин. ЦЗ является самой большой у основания простаты и сужается к вершине, составляя 25% вся железистая ткань. При ДГПЖ увеличивающаяся ТЗ сжимает ЦЗ и утончает ПЗ. Передняя поверхность простаты состоит только из фиброзной и мышечной ткани без ацинусов. Это называется передней фибромускулярной стромой и не является очагом заболевания.
Рисунок 15.4. Нормальные семенные пузырьки. Поперечное изображение демонстрирует оба семенных пузырька (ов) нормального типа в форме «галстука-бабочки». Небольшая асимметрия размеров является нормальным вариантом. б, мочевой пузырь.
Рисунок 15.5. Нормальный угол семенного пузырька. Латеральное сагиттальное изображение показывает нормальный, заполненный жиром острый угол ( стрелка ) между гипоэхогенным семенным пузырьком (s) и более эхогенным основанием простаты (P). Мочевой пузырь (б) частично заполнен мочой.
Основная часть рака (70%) наблюдается в ПЗ. Примерно 10% случаев относится к TZ, а 20% — к ЦЗ. Процедура трансуретральной резекции простаты заключается в удалении периуретральной ткани ТЗ выше верумонтана с сохранением полости, непрерывной с просветом мочевого пузыря. Злокачественные образования в ТЗ часто обнаруживаются случайным образом в тканях, взятых во время трансуретральной резекции простаты.
ТРУЗИ позволяет визуализировать семенные пузырьки как овальные гипоэхогенные структуры длиной 3-5 см и диаметром 1-2 см. В аксиальной плоскости пара семенных пузырьков выглядит как «галстук-бабочка» (рис. 15.4). Легкая асимметрия размеров наблюдается довольно часто. Но выраженная асимметрия может свидетельствовать о наличии опухолевого поражения у мужчин с раком предстательной железы.
Острый угол между задними семенными пузырьками и основанием простаты покрыт эхогенным жиром. Утрата этого острого угла предполагает инвазию опухоли в семенные пузырьки ( рис. 15.5 ). Утолщенную ампулярную часть семявыносящего протока часто можно увидеть отдельно от семенных пузырьков ( рис. 15.6 ).
У молодых мужчин ПЗ имеет схожую эхогенность с ТЗ и ЦЗ. С возрастом и в процессе гипертрофии ТЗ внутренняя часть железы увеличивается и становится неоднородной. В результате ПЗ воспринимается как относительно гиперэхогенная и чётко выраженная. Границу между ПЗ и внутренней частью железы называют хирургической капсулой (рис. 15.2). Уретра определяется по средней линии простаты, находя её V-образное отверстие у основания мочевого пузыря (рис. 15.7).
Оценить вес простаты можно с помощью пальцевого ректального исследования. Измерение объема простаты с помощью УЗИ легко соотносится с весом, поскольку 1 см 3 равен 1 грамму. Предстательная железа объем рассчитывается по формуле (длина × ширина × высота × 0,52 = объем). У молодых мужчин нормальная железа составляет 20 г. У пожилых мужчин простата считается увеличенной, если ее вес превышает 40 г.
Рисунок 15.6. Нормальная ампулярная часть семявыносящего протока. На угловом корональном изображении видно левый семенной пузырёк (с) и ампулярную часть семявыносящего протока (г). Соединение семявыносящего протока с семенным пузырьком служит началом семявыбрасывающего протока (д).
Рисунок 15.7. Нормальная простатическая уретра. Сагиттальное срединное изображение простаты с использованием эндоректального линейного датчика показывает простатическую уретру (стрелки) и отверстие уретры (стрелка) у основания мочевого пузыря (b). г, стенка прямой кишки; s, семенной пузырек.
Рак простаты
Рак простаты является наиболее часто встречаемым типом рака среди мужчин. Мужчины в США имеют приблизительно 10% вероятность заболеть этим заболеванием на протяжении жизни и 3% шанс умереть от него. Частота заболевания выше среди афроамериканцев и мужчин с положительным семейным анамнезом. Изначально ТРУЗИ рассматривалось как перспективный метод для скрининга мужчин на предмет рака простаты. Однако установленные показатели чувствительности на уровне 50-70% и специфичности 40-60% делают его недостаточным для полноценного скрининга [ 5 ]. Современные рекомендации Американского онкологического общества по скринингу предписывают ежегодные тесты на простатспецифический антиген (ПСА) и пальцевое ректальное исследование для всех мужчин старше 50 лет, и для мужчин старше 45 лет, если они являются афроамериканцами или имеют семейный анамнез рака простаты [ 6 ]. Биопсия с использованием ТРУЗИ часто рекомендована при уровнях ПСА выше 4 нг/мл и при обнаружении пальпируемых отклонений [ 6 , 7 ].
Нормальный, гиперпластический и неопластический эпителий предстательной железы продуцирует ПСА. Рак повышает уровень ПСА в сыворотке крови в 10 раз выше, чем такой же объем ткани ДГПЖ. ПСА специфичен для органа, но не для заболевания. Помимо рака, уровень ПСА в сыворотке крови повышается при ДГПЖ, простатите, инфаркте предстательной железы, биопсии и хирургическом вмешательстве.
Уровни сывороточного ПСА от 0 до 4 нг/мл считаются нормальными, хотя до 25% мужчин с раком простаты могут иметь ПСА в этом диапазоне [ 6 ]. Значения от 4 до 10 нг/мл рассматриваются как пограничные и связаны с 20% риском возникновения рака. При уровнях, превышающих 10 нг/мл, риск развития рака достигает 67%. Для повышения специфичности ПСА применяются такие методы, как расчёты плотности ПСА и скорости ПСА [ 8 ]. Плотность ПСА определяется как соотношение сывороточного ПСА к объёму простаты, при этом значения выше 0,12 интерпретируются как риск заболевания. Скорость ПСА отражает темпы увеличения уровня ПСА в крови со временем. Показанием к биопсии является рост уровня ПСА на 20% по сравнению с начальным значением в течение года или абсолютное увеличение на 0,75 нг/мл за тот же период.
Биопсия, проводимая под контролем ТРУЗИ, осуществляется с использованием автоматических игл для биопсий 18-го калибра [ 9 ]. Поскольку процедура выполняется трансректально, пациентам назначают антибиотики для профилактики. Все подозрительные образования, выявленные при пальцевом ректальном или ультразвуковом обследовании, подлежат биопсии, также осуществляется отбор 6-10 случайных биопсий из разных участков железы (рис. 15.8). Возможные осложнения после биопсии могут включать гематурию, гематоспермию и инфекции.
Рак предстательной железы распространяется путем прямой инвазии через ее капсулу в перипростатические ткани и семенные пузырьки, лимфатическим путем в регионарные лимфатические узлы и венозным путем в позвоночник. В дальнейшем гематогенное распространение может распространиться на любой орган. Выявления рака простаты включают:
Рисунок 15.8. Биопсия простаты под контролем ТРУЗИ. Сагиттальное изображение левой боковой части простаты показывает иглу (стрелка) в области левого основания во время биопсии простаты по случайному образцу.
- Дискретный узел в ПЗ.
- – Гипоэхогенные узелки (70%) (рис. 15.9) не являются специфичными для рака. Дифференциальный диагноз смотрите в блоке 15.1.
- – Гиперэхогенный/гетерогенный узел (30%).
- – Нередко может наблюдаться гипоэхогенное нечеткое образование (рис. 15.10).
- Рак может иметь изоэхогенные характеристики, что затрудняет его выявление на УЗИ в примерно 25% случаев. Некоторые образования проявляют массовый эффект, изменения контуров, асимметрию размеров или формы железы, а также потерю четкой дифференциации периферической зоны от центральной. Однако большинство изоэхогенных опухолей можно обнаружить только при случайной биопсии, проводимой под контролем УЗИ.
Рисунок 15.9 Гипоэхогенный узел в периферической зоне. На сагиттальном изображении виден плохо выраженный гипоэхогенный узел ( стрелка ) в периферической зоне простаты. Биопсия подтвердила аденокарциному.
Вставка 15.1. Гипоэхогенное образование в области простаты
Наличие ретенционных кист
Доброкачественная гиперплазия, редко в периферической зоне.
Объем предстательной железы в норме
Стандартные размеры предстательной железы следующие:
- Верхненижняя длина — от 2,6 до 4,5 см.
- Ширина в поперечном направлении — от 2,3 до 3,0 см.
- Толщина переднезаднего измерения — от 1,6 до 2,2 см.
Объем здоровой простаты, определяемый по формуле, равен 20–30 см 3 . С годами предстательная железа увеличивается в размерах. Поэтому нормы объема зависят от возраста. Для того чтобы определить нормальный объем по возрасту, умножают 0,13 на количество прожитых лет, и к полученному произведению прибавляют 16,4. У мужчин после 60 лет допустимый объем может превышать 30 см 3 , но незначительно. Если объем простаты:
- 30-40 см3 — незначительное увеличение.
- 40-80 см3 — умеренное увеличение.
- 80-250 см3 — крупная железа.
- 250 см3 и более — гигантская железа.
Даже незначительное увеличение вызывает беспокойство и требует консультации уролога.
Увеличение предстательной железы
Наиболее распространенные причины увеличения предстательной железы:
- Острый простатит, воспаление.
- Злокачественные опухоли, рак.
- Доброкачественная гиперплазия простаты (ДГПЖ) или аденома железы.
Каждое из этих патологических состояний имеет особенности. При остром простатите увеличение объема идет за счет воспалительного отека ткани простаты. При раке рост железы обусловлен бурным делением ненормальных, атипичных, раковых клеток. А при ДГПЖ железа увеличивается из-за недостатка мужского полового гормона тестостерона у зрелых, пожилых мужчин или у стариков. На дефицит тестостерона ткань простаты реагирует ростом, увеличением объема, или гиперплазией.
ДГПЖ является наибольшей причиной увеличения органа. Увеличенная железа начинает сжимать мочеиспускательный канал, что приводит к затруднениям при мочеиспускании. В последующем на фоне гиперплазии может развиваться вторичное воспаление, что вызывает проблемы в интимной сфере.
Уменьшение простаты
Маленький объем простаты у взрослого мужчины не превышает 19–20 см 3 . Уменьшение обусловлено склеротическими процессами, когда нормальная железистая и мышечная ткань в простате замещается соединительной тканью. Причины, чтобы простате уменьшиться в размерах:
- Хронический простатит.
- Эндокринные расстройства.
- Генетические предрасположенности.
- Чрезмерное употребление алкоголя.
- Тяжелые сопутствующие заболевания.
- Аллергические реакции.
Даже при малом размере простаты могут возникать проблемы с мочеиспусканием и эректильной функцией.
Лечение аденомы простаты
При легкой и средней степени ДГПЖ часто применяется консервативное лечение, без оперативного вмешательства. В рамках этого лечения назначают медикаменты, которые действуют специфически на простату. Одним из них является препарат Афалаза. Его активные компоненты:
- Улучшение кровообращения в тканях железы.
- Угнетение гиперпластических процессов.
- Снижение сопутствующего воспаления.
Афалаза выпускается в таблетках для рассасывания. Для того чтобы уменьшить аденому простаты таблетки нужно рассасывать в промежутках между едой. Дозировка и продолжительность приема определяется урологом и зависит от степени увеличения.
Патологии, характеризующиеся увеличением ПЖ
Современная медицина пока не может точно определить причины ненормального увеличения простаты. Исследования установили, что одним из факторов риска является функция яичек — простата не увеличивается у мужчин, у которых яички удалены.
Все другие причины так или иначе связаны с возрастом. Среди них:
- естественное возрастное снижение уровня тестостерона и прирост эстрогена в крови;
- повышение уровня дигидротестостерона — гормона, вырабатываемого простатой. У пожилых мужчин его уровень остается прежним, что приводит к накоплению и увеличению размера железы;
- наследственные предрасположенности — генетическая программа может активизировать рост простаты после 60 лет (это предположение остается гипотезой).
Увеличенная простата в первую очередь негативно сказывается на качестве жизни мужчины. Он испытывает трудности с ночным сном, постоянно ощущает потребность в туалете и не может позволить себе поездки на дальние расстояния и т.д. Аденома и простатит являются наиболее распространенными заболеваниями, связными с разрастанием тканей простаты.
Аденома простаты (доброкачественная гиперплазия)
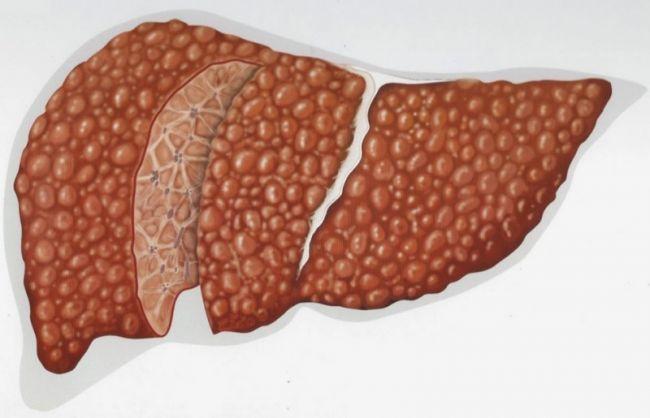
УЗ-диагностика позволяет подробно исследовать структуру простаты. В норме она должна иметь симметричную форму, разделенную продольной бороздой на две части. В каждой из половин должно быть до 25 долей. Большинство урологических заболеваний ведут к потере однородности структуры железы, диффузным изменениям, проявляющимся в виде опухолей, кист и других признаков дисплазии, гиперплазии или атрофии.
По результатам УЗИ врач определяет передне-задний и продольный размеры ПЖ методом сагиттального сканирования, а также поперечный посредством исследования средней части органа. Затем проводятся специальные расчеты, и выносится решение о наличии или отсутствии патологии.
Здоровая предстательная железа имеет четкую структуру, ровные контуры и симметричную форму.
Нормальные размеры предстательной железы на УЗИ у мужчин от 20 до 40 лет:
- Продольный размер — от 24 до 40 мм;
- Поперечный размер — от 27 до 42 мм;
- Переднезадний размер — от 15 до 25 мм.
С возрастом размер органа постепенно увеличивается, что отражает и показатели нормы. Интенсивность этого роста зависит от наследственных факторов, общего состояния здоровья и образа жизни пациента.
Поэтому для постановки диагноза уролог анализирует общую клиническую картину, учитывая как состояние простаты, так и наличие других симптомов: болей, половой слабости, проблем с мочеиспусканием и так далее.
Важность проведения УЗИ
Многие заболевания протекают бессимптомно и обнаруживаются лишь тогда, когда оказать помочь пациенту очень трудно, а порой невозможно. Так, застарелая гиперплазия нередко приводит к острой задержке мочи, при которой выход только один: оперативное вмешательство.
Доброкачественные опухоли предстательной железы в зрелом возрасте могут трансформироваться в злокачественные, а первые выраженные симптомы могут проявиться только после метастазирования.
Посещение кабинета врача всего 1-2 раза в год позволит избежать столь серьезных последствий. Своевременная профилактика урологических заболеваний – гарантия полноценной жизни и здоровья мужчины до самой старости.
Похожие темы научных работ по клинической медицине , автор научной работы — Горбунова Е. Н., Крупин В. Н
Динамика патологических процессов у пациентов с заболеваниями простаты, тактика ведения. Эффективность ретроградной контактной электроимпульсной литотрипсии.
Хроническое воспаление и фиброз как факторы риска простатических интраэпителиальных неоплазий и рака простаты.
Математическое моделирование послеоперационного течения рака простаты. Эластография сдвиговой волны в диагностике заболеваний предстательной железы. Если вы не можете найти нужную информацию, попробуйте сервис подбора литературы. Устали от рекламы? Вы в любое время можете отключить ее.
ULTRASOUND CRITERION OF PERIPHERAL PROSTATE ZONE MEASUREMENT AS PREOPERATIVE PROSTATE CANCER AND PROSTATIC INTRAEPITHELIAL NEOPLASIA PROGNOSTICATION
В данной статье рассматриваются потенциальные возможности измерения размеров периферической зоны простаты и соотношения размеров периферической зоны к объему простаты как дополнительных критериев для диагностики рака простаты и простатической интраэпителиальной неоплазии (ПИН). При соотношении размеров периферической зоны к объему простаты, превышающем 0,16 см/см3, возрастает вероятность выявления рака простаты. Р=0.05.
13. Oremek G.M. Bickeboller, R., Seiffert, U.B., Jonas, D (1995) Aussagekraft des neuenTumormarkers Tumor M2-Pk beiPatientedmitHo-dentumor 12. Symposium fur ExperimentelleUrologie, Berlin, 16. v 18. Marz 1995
14. Oremek G.M. M2 пируваткиназа как опухолевый маркер для рака почек / Oremek G.M. // Anticancer Research. Т. 19. С. 2599-2602
15. Parkin D.M., Bray F., Ferlay J., Pisani P. Глобальная статистика рака, 2002. CA Cancer J Clin 2005;55:74—108
16. Parton M., Gore M., Eisen T. Role of cytokine therapy in 2006 and beyond for metastatic renal cell cancer. J Clin 0ncol2006;24:5584-92
17. Paradis V, Lagha NB, Zeimoura L, Blanchet P, Eschwege P, Ba N, Benoit G, Jardin A, Bedossa P. Экспрессия фактора роста сосудистого эндотелия в карциномах почек. Virchows Arch. 2000 Apr;436(4):351-6.
18. Sato K., Tsuchiya N., Sasaki R et. al. Increased serum levels of vascular endothelial growth factor in patients with renal cell carcinoma.
Jpn J. Cancer Res. 1999; 90 (8): 874 — 879
19. Schneider J., Schulze G. // Anticancer Research. — 2003. — Т. 23. С. 5089-5094
20. Skinner D.G., Colvin R.B., Vermilion CD., et al. Diagnosis and management of renal cell carcinoma.// Cancer.-1971.-v.28.-pp.-1165-77. -32
21. Weyman P.J., McClennan B.L., Stanley R.J. и др. Сравнение КТ и ангиографии при оценке рака почек. // Радиология. — 1980. — Т. 137. С. 417-424.
Е.Н. Горбунова, В.Н. Крупин
УЛЬТРАЗВУКОВОЙ КРИТЕРИЙ ТОЛЩИНЫ ПЕРИФЕРИЧЕСКОЙ ЗОНЫ ПРОСТАТЫ КАК МЕТОД ПРЕДОПЕРАЦИОННОГО ПРОГНОЗИРОВАНИЯ РАКА ПРОСТАТЫ И ПИ.
НЕОПЛАЗИЙ ГОУ ВПО «НижГМА Минсоцразвития РФ», г. Н. Новгород
Статья обсуждает возможность применения измерения толщины периферической зоны простаты и ее соотношения к объему простаты как дополнительных критериев диагностирования ПИН и рака простаты. Если толщина периферической зоны составляет более 0,16 мм/см3, вероятность выявления рака простаты увеличивается, Р=0,05.
Ye.N. Gorbunova, V.N. Krupin ULTRASOUND CRITERION OF PERIPHERAL PROSTATE ZONE MEASUREMENT AS PREOPERATIVE PROSTATE CANCER AND PROSTATIC INTRAEPITHELIAL NEOPLASIA PROGNOSTICATION
Статья рассматривает потенциальные применения измерений размеров периферической зоны простаты и соотношения размеров периферической зоны к объему простаты как дополнительных критериев диагностирования рака простаты и простатической интраэпителиальной неоплазии. При соотношении превышающем 0,16 см/см3 вероятность выявления рака простаты возрастает. Р=0.05.
Ключевые слова: доброкачественная гиперплазия простаты, рак простаты, простатическая интраэпителиальная неоплазия, измерение периферической зоны простаты.
В настоящее время прирост заболеваемости раком простаты (РПЖ) достигает в среднем 3% за год, что позволяет прогнозировать удвоение числа регистрируемых случаев к 2030 г [1]. Непосредственным предраком простаты являются простатические интраэпи-телиальные неоплазии (ПИН), а достоверным методом подтверждения диагноза — биопсия простаты. Качественных дооперационных методов диагностики ПИН не разработано. Так как рак простаты развивается преимущественно в периферической зоне (в 70% случаев [4, 5], мы предприняли попытку установить связь между гистологическим диагнозом и толщиной периферической зоны простаты (ТПЗ), измеряемой при трансректальном ультразвуковом исследовании (ТРУЗИ).
Цель исследования: оценить возможности измерений толщины периферической зоны простаты для диагностики раннего рака простаты и простатической интраэпителиальной неоплазии.
Материал и методы
Толщина периферической зоны определялась на поперечном сечении простаты в области семенного бугорка. Анатомия зон простаты на поперечном сечении представлена на рисунке 1. В области семенного бугорка простата имеет треугольную форму, основание направлено к датчику.
В центре четко видна гипоэхогенная центральная область, над которой просматривается более яркая по эхогенности полоса — передняя фиброзно-мышечная зона. Периферическая часть железы окружает центральную область снизу и с боков и обладает гиперэхогенной структурой по сравнению с центральной зоной. Толщина периферической зоны измерялась латерально от переходных зон до нижнего угла треугольного сечения простаты (линия 8 на рисунке 1). В имеющейся литературе мы не нашли упоминаний о подобной оценке толщины на этом уровне.
Современные представления о развитии ДГПЖ базируются на принципах зональной анатомии и патоморфологии простаты по Мс№а1: доброкачественная гиперплазия развивается из железистой внутренней части железы, т.е. из переходных зон и центральной зоны, а рак исходит главным образом из периферической зоны простаты [4, 6]. Таким образом, при аденоматозном доброкачественном росте мы будем иметь скорее меньшую, сдавленную узлами, периферическую зону, а при злокачественном росте при отсутствии явных узлов мы скорее должны наблюдать большую толщину периферической зоны к объему простаты.
Толщина периферической зоны может варьироваться при равном объеме простаты, и, соответственно, процентное соотношение периферической зоны.
ческой зоны в ткани простаты будет различной. Поэтому по аналогии с ПСА-плотностью рассчитано соотношение «толщина периферической зоны/объем простаты», мм/см3 (ТПЗ/ОП).
Рис. 1. Зональная анатомия предстательной железы по Kaye K.W. (1989) с изменениями. 1 — периферическая зона (75%), 2 — центральная зона (20% железистой ткани), 3 — транзиторные зоны (5%), 4 — периуретральные железы, 5 — передняя фибро-мускулярная строма, 6 — продольные гладкомышечные волокна мочеиспускательного канала, 7 — препростатический сфинктер. S — линия измерения толщины периферической зоны.
Клинические характеристики пациентов
Группа ДГПЖ ПИН1 ПИН2 РПЖ
п 597 47 110 26
Возраст, лет 65,33 68,98 69,52 65,33
Уровень ПСА составил 5,84; 6,51; 6,30; 33,62 нг/мл.
Средний объем простаты равен 69,99±2,19; 70,69±7,8; 67,36±5,04; 48,53±2,45 см³.
Средняя ТПЗ, мм 6,73±0,24 7,13±1,83 7,49±0,6 8,42±1,09
В рамках исследования, проведенного на 780 пациентах с ТРУЗИ, была измерена толщина периферической зоны простаты (ТПЗ). У 597 участников диагноз доброкачественной гиперплазии (ДГПЖ) был подтвержден гистологически, у 47 — ПИН1, у 110 — ПИН2, и у 26 — РПЖ. Все случаи были исключены, если в ткани простаты обнаруживались гипоэхогенные зоны (таблица 1).
Результаты и обсуждение Статистические данные о периферической зоне представлены в табл. 2.
Толщина периферической зоны простаты:
Группа n Средняя толщина, мм Стандартное отклонение Мин. толщина, мм Макс. толщина, мм
ДГПЖ 597 6,73±0,24 2,96 2 20
ПИН1: 47 7,13±1,83 3,03 2 13
ПИН2 110 7,49±0,6 3,16 2 17
РПЖ: 26 8,42±1,09 2,70 2 13
Различия в толщине простаты между упомянутыми группами отсутствуют (р=0,05) (рис. 2).
толщина периферической зоны, мм
Рис. 2. Интервальная оценка средней толщины периферической зоны.
Отношение толщины периферической зоны ________простаты к объему простаты.________________
Группа n Среднее соотношение, мм/см³ Стандартное отклонение Мин. соотношение, мм/см³ Макс. соотношение, мм/см³
ДГПЖ: 597 0,118±0,008 0,07 0,012 0,657
ПИН1 47 0,118±0,038 0,06 0,032 0,283
ПИН2: 110 0,131±0,011 0,07 0,040 0,387
РПЖ 26 0,209±0,049 0,12 0,061 0,633
Чтобы объективно оценить состояние периферической зоны простаты, данные ТРУЗИ были использованы для расчета отношения: толщина периферической зоны к объему простаты (ТПЗ/ОП, мм/см³) (таблица 3).
Средние значения ТПЗ/ОП для ДГПЖ и ПИН1 составляют 0,118 мм/см³, для ПИН2 — 0,131 мм/см³, а для РПЖ — 0,209 мм/см³. Интервалы среднего ТПЗ/ОП представлены на рис. 3. Учитывая доверительные интервалы, разница в среднем отношении ТПЗ/ОП
Выявляемость рака простаты в зависимости от величины ТПЗ/ОП
N 13 (100%) 21 (100%)
ДГПЖ 5 (38,46%) 8 (38,10%)
ПИН2: 6 (46,15%) 8 (38,10%)
0,1 0,15 0,2 0,25 0,3
Отношение ТПЗ/ОП, мм/см3
Рис. 3. Интервальная оценка среднего отношения ТПЗ/ОП.
Выдвинутая гипотеза об относительном росте толщины периферической зоны простаты при ПИН2 и раке простаты апробирована на контрольной группе из 34 пациентов. Средняя ТПЗ составила 9,86+1,31 мм (минимум 2,00 мм, максимум 16,00мм, стандартное отклонение 3,76 мм). Средний объем простаты в этой группе составил 64,31+11,45 см3 (минимум 28,90см3, максимум 175,00см3, стандартное отклонение 32,91 см3).
В группе среднее значение ТПЗ/ОП стало 0,20±0,04 мм/см³ (от 0,01 до 0,40 мм/см³, стандартное отклонение 0,11 мм/см³). Учитывая ранее полученные результаты по увеличению ТПЗ/ОП при раке простаты и ПИН2, контрольная группа из 34 пациентов была разделена на две подгруппы. В первой подгруппе было отмечено ТПЗ/ОП 0,16 мм/см³ (нижняя граница доверительного интервала для среднего отношения ТПЗ/ОП при раке простаты). Данные о распространенности рака простаты в зависимости от величины соотношения ТПЗ/ОП даны в таблице 4 и на рис. 4.
ДГПЖ ПИН1 ПИН2 РПЖ
Рис. 4. Процентное соотношение выявленной патологии в зависимости от ТПЗ/ОП.
В первой подгруппе ДГПЖ была диагностирована у 38,46% пациентов, ПИН1 — у 15,38%, ПИН2 — у 46,15%, а РПЖ не было ни у кого. Во второй подгруппе результаты были схожи: ДГПЖ — 38,10%, ПИН1 — не выявлен, ПИН2 — 38,10%, и РПЖ — у 23,81%. Во всех случаях рака простаты соответствующее соотношение ТПЗ/ОП превышало 0,16 мм/см³. Несмотря на это, стоит отметить, что низкая чувствительность данного маркера может снизить его информативность; вероятно с 95% точностью можно сказать, что при соотношении ТПЗ/ОП >0,16 мм/см³ вероятность обнаружения рака в послеоперационной гистологии повышается на 23,81%.
Таким образом, можно наблюдать, что в ряду ДГПЖ-ПИН1-ПИН2-РПЖ имеется тенденция к росту толщины периферической зоны относительно объема простаты. Как известно, аденоматозная гиперплазия развивается из транзиторной зоны простаты, а рак простаты примерно в 70% случаев развивается из переходной зоны, поэтому имеющаяся тенденция к росту отношения толщины периферической зоны к объему предстательной железы при ПИН1 и ПИН2 подтверждает их предраковую ориентированность. При решении вопроса о целесообразности биопсии простаты с целью гистологической верификации диагноза наряду с прочими факторами (ПРИ, гипоэхогенность по ТРУЗИ, ПСА) возможно оценивать и данный показатель. Показатель ТПЗ/ОП для ДГПЖ и ПИН1 равны, а по интервальным оценкам рост ТПЗ/ОП в ряду ДГПЖ-ПИН2-РПЖ статистически значим при р=0,05, поэтому как пограничную цифру, после которой повышается вероятность обнаружения в гистологическом материале РПЖ, можно предложить величину ТПЗ/ОП> 0,16мм/см3. При прогнозировании, безусловно, должны учитываться уровень ПСА сыворотки крови, ПСА-плотность, возраст, изменения при ТРУЗИ.
Информация об авторах статьи:
i Не удается найти то, что вам нужно? Воспользуйтесь сервисом по подбору литературы.
1. Boyle P., Maisonneuve P., Napalkov P. Incidence of prostate cancer will double by the year 2030: arguments// Europ. J. Urol. — 1996. -Vol. 29 (suppl. 2). — P. 3-9.
2. Kaye K.W. Изменение представлений о сонографической анатомии простаты с доброкачественной гиперплазией. // J. Endourol. 1989. V 3. № 2. С. 103-108.
3. Митьков В.В. Практическое руководство по ультразвуковой диагностике. Oбщая ультразвуковая диагностика. — М.: Издательский дом Видар-М, 2003. — 720с., ил..
4. Пальцев М. А., Аничков Н. М. Патологическая анатомия: Учебник. В 2-х томах. Т.2 Ч. II. – М.: Медицина, 2001. – 680 с.: ил.
5. Переверзев А. С., Коган М. И. Рак простаты: Монография. – Х.: Факт, 2004. – 231 с.
6. Струков А.И., Серов В.В. Патологическая анатомия: Учебник. — 4-е изд., стереотипное. — М.: Медицина, 1995.- 688 с.; ил.
А. В. Гудков, В. С. Бощенко ЭФФЕКТИВНОСТЬ РЕТРОГРАДНОЙ КОНТАКТНОЙ ЭЛЕКТРОИМПУЛЬСНОЙ ЛИТОТРИПСИИ
ГОУ ВПО «СибГМУ Минздравсоцразвития России», г. Томск
Цель исследования заключалась в оценке эффективности ретроградной контактной электроимпульсной литотрипсии (ЭИЛТ) у пациентов с мочекаменной болезнью (МКБ). ЭИЛТ была проведена 436 больным (в возрасте 53±25 лет), среди которых 26 (6%) имели камни почек, 397 (91%) — в мочеточниках и 13 (3%) — в мочевом пузыре, с использованием электроимпульсного литотриптера «Уролит-105М» (Lithotech Medical, Израиль, ООО «МедЛайн», Россия). Выявлено, что ЭИЛТ является эффективным и безопасным методом лечения МКБ, обеспечивая полное разрушение камней в 95% случаев. Применяемые гибкие зонды позволяют разрушать конкременты по всему мочевому тракту — от чашечек почки до мочеиспускательного канала.
A.V. Gudkov, V.S. Bosch’enko
EFFICACY OF RETROGRADE CONTACT ELECTROIMPULSE LITHOTRIPSY
Целью исследования была оценка возможности, эффективности и безопасности ретроградной контактной электроимпульсной литотрипсии (РКЭЛ) у пациентов с уролитиазом. РКЭЛ были выполнены на 436 пациентах (средний возраст 53±25 лет) с использованием нового электроимпульсного литотриптера “Уролит-105M” (Lithotech Medical, Израиль, ООО “MedLine”, Россия); у 26 (6%) пациентов были камни почек, у 397 (91%) — мочеточников и у 13 (3%) — мочевого пузыря. РКЭЛ оказалась эффективным, безопасным и удобным методом лечения уролитиаза, что привело к полному разрушению камней в почках, мочеточниках и мочевом пузыре в 95% случаев. Гибкие электроды РКЭЛ обеспечивают успешное разрушение конкрементов по всему мочевому тракту, начиная от чашечек почек до уретры и удаления образовавшихся фрагментов.
Key words: endoscopic contact electroimpulse lithotripsy, urolithiasis.
Мочекаменная болезнь (МКБ) занимает второе место среди всех урологических заболеваний в России, составляя в среднем 34,2% их общего числа [1, 2]. Часто МКБ приводит к осложнениям, требующим хирургического вмешательства. В последнее время для радикального удаления конкрементов всё чаще используют контактные эндоскопические методики, которые позволяют сократить длительность операции и постоперационного периода, а также снизить риск осложнений по сравнению с дистанционной литотрипсией (ДЛТ) и открытой литотомией [3, 4,
Основной целью данного исследования стала оценка эффективности ретроградной контактной литотрипсии у пациентов с уринационными камнями различных локализаций.
Материал и методы
В исследование вошло 436 пациентов (средний возраст — 53±25 лет, диапазон от 19 до 72 лет) с конкрементами в почках, мочеточниках и мочевом пузыре, которые подписали информированное согласие. По полу пациенты распределились следующим образом:
делились следующим образом: женщин было 201 (46,1%), мужчин — 235 (53,9%). В основном больные были госпитализированы в стационар в экстренном порядке с почечной коликой (401 больных (92%)), либо в плановом порядке (35 больных (8%)).
Все пациенты были разделены на 3 группы в зависимости от местоположения камнеобразований. Первая группа состоит из 26 пациентов (6%) с камнями в почках и Лоханочно-мочеточниковом сегменте (ЛМС), вторая— самая многочисленная группа, 397 пациентов (91%) с камнями мочеточников, третья— 13 пациентов (3%) с камнями мочевого пузыря.
Каждому пациенту проводились: сбор жалоб и анамнеза, физикальное обследование, общий анализ мочи, общий анализ крови, биохимический анализ крови, анализ свертываемости, бактериологический посев мочи, ультразвуковое исследование почек, мочеточников и мочевого пузыря в В-режиме, а также экскреторная урография.
Контактную ЭИЛТ проводили с помощью электроимпульсного литотриптора «Уролит-105М», разработанного и произведенного компаниями Lithotech Medical Ltd.
Нормальный объем простаты, объемы простаты норма
Нормальный объем простаты не должен превышать 26 кубических сантиметров. Однако, этот показатель может варьироваться в зависимости от возраста пациента.
Объем предстательной железы (ПЖ), норма объема предстательной железы очень простая — максимум 26,0 куб см. Размеры и объем предстательной железы меняются с увеличением возраста. Вы можете рассчитать нормальный объем простаты по формуле. И так, формула объем предстательной железы (простаты) в норме в зависимости от возраста мужчины (А. И. Громов):
В данной формуле: А — это объем предстательной железы, Б — возраст пациента (мужчины). Например, у мужчины в 25 лет нормальный объем простаты составляет: 0,13×25 + 16,4 = 19,65 куб. см. У мужчины в 75 лет нормальный объем простаты равен: 0,13×75 + 16,4 = 26,15 куб. см. У мужчины в 55 лет объем предстательной железы в норме равен: 0,13×55 + 16,4 = 23,55 куб. см. У мужчины в 45 лет нормальные объемы простаты составляют: 0,13×45 + 16,4 = 22,25 куб. см.
Если у вас размер простаты превышает 26 см³ и до 50 см³ (например, 27, 28, 29 и так далее до 50 см³) — это весомый повод обратиться к специалисту.
Проблемы с простатой? Обращайтесь в Сарклиник.
Запись на консультацию. Имеются противопоказания. Нужна консультация врача.