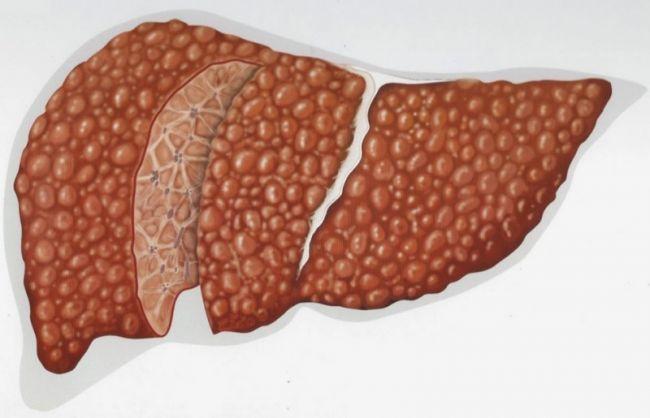
Одной из заболеваний печени, способствующих повышению уровня холестерина у мужчин, является жирная печеночная болезнь (стеатоз). При этом состоянии происходит накопление жира в клетках печени, что нарушает ее функциональные способности, включая метаболизм липидов. В результате уровень плохого холестерина (ЛПНП) может значительно возрасти.
Кроме того, заболевания, такие как цирроз печени, также могут привести к нарушениям обмена веществ, что способствуют повышенному содержанию холестерина в крови. Сатурация печени жировыми клетками уменьшает её способность к детоксикации и усвоению липидов, что ведет к ухудшению общего состояния здоровья и риску сердечно-сосудистых заболеваний.
- Цирроз печени: Хроническое заболевание печени, которое может приводить к нарушению метаболизма липидов.
- Неалкогольная жирная болезнь печени (НАЖБП): Увеличивает уровень холестерина за счет накопления жира в печени.
- Гепатит: Воспаление печени может также влиять на уровень холестерина в крови.
- Роль инсулинорезистентности: Связь между болезнями печени и инсулинорезистентностью, способствующей повышению холестерина.
- Рекомендации по лечению: Включает изменение образа жизни и диету для снижения уровня холестерина.
— Двигаемся дальше. Моей следующей темой станет лекция под названием «Атеросклероз – это болезнь печени?» с вопросительным знаком.
Каковы же причины для подобного утверждения? Печень является основным источником множества липидов, и многие процессы, касающиеся атерогенеза, происходят именно в печени.
Начнем с транспорта экзогенных липидов – триглицеридов и холестерина. Напоминаю, что холестерин представляет собой нерастворимое вещество, которое всасывается в кишечнике и превращается в растворимые формы в составе хиломикронов и свободных жирных кислот. Благодаря действию липопротеид-липазы, хиломикроны трансформируются в редуцированные или эонантные хиломикроны.
Они очень богаты холестерином. Они устремляются в атерому, воспроизводя свой атерогенный эффект.
В то же время существует эндогенный путь метаболизма липидов, который невозможен без нормального функционирования печени. Здесь необходима полноценная активность печеночной липазы. Липопротеиды очень низкой плотности постепенно преобразуются в липопротеиды низкой плотности (ЛНП), теряя свою плотность.
Соответственно, уменьшаются в размерах. Большие липопротеиды очень низкой плотности под воздействием липопротеид-липазы превращаются в мелкие липопротеиды очень низкой плотности. Затем через этап липопротеидов промежуточной плотности они превращаются в ЛНП. Атерогенной фракции служат именно окисленные, мелкие, модифицированные ЛНП, которые стимулируют синтез макрофагов. Инициируется процесс атеросклероза, что и запускает формирование атеросклеротической бляшки.
Давайте немного вспомним основы биохимии. Холестерин – это вещество, жизненно необходимое нам, он играет ключевую роль в синтезе холестероидных гормонов и желчных кислот. Холестерин присутствует в клеточных мембранах всех живых организмов.
Одной из наиболее значительных болезней печени, способствующих повышению уровня холестерина у мужчин, является неалкогольная жировая болезнь печени (НАЖБП). Эта патология характеризуется накоплением жира в клетках печени, что может привести к воспалению и даже фиброзу. При развитии НАЖБП метаболизм липидов нарушается, что, в свою очередь, влияет на уровень холестерина в крови. Это особенно заметно у мужчин, которые часто имеют более высокие риски развития данной болезни из-за особенностей образа жизни и питания.
Кроме того, необходимо отметить, что хронический гепатит, вызванный вирусами, также может повлиять на уровень холестерина. Воспаление печени в результате хронической инфекции становится причиной изменения метаболических процессов, связанных с холестерином. В таких случаях, несмотря на нормальное или низкое потребление жиров с пищей, уровень холестерина может оставаться высоким из-за недостаточной функции печени по его переработке и выведению.
Не менее важным фактором является цирроз печени, который развивается как следствие различных заболеваний печени, включая алкогольную болезнь и гепатиты. При циррозе печень теряет свою способность продуктивно работать, что приводит к как гиперлипидемии, так и к нарушению выведения холестерина. Следовательно, мужчины, страдающие от цирроза, нередко сталкиваются с хронически повышенными уровнями общего холестерина и липопротеинов низкой плотности, что увеличивает риск сердечно-сосудистых заболеваний.
У человека основная часть холестерина (практически 50%) синтезируется именно в печени.
Исходя из этого, для его снижения существует множество оснований, прописанных в рекомендациях как Европейского, так и Российского Общества Кардиологов. Национальное Общество Атеросклероза также активно занимается данной темой и недавно опубликовало обновленные рекомендации за 2011 год.
Синтез холестерина в печени проходит несколько интересных этапов. Здесь ключевую роль играет фермент ГМК КоА редуктаза, который является целью действия статинов. Важно учитывать влияние метаболических процессов и синтеза изопреноидов.
Он приводит к тому, что происходит активация сигнальных молекул, малых молекул, которые опосредуют эффекты. Когда статины действуют на ГНК КоА редуктазу и посредством их влияния на изопреноиды, осуществляются плейотропные действия, которые до сих пор окутывают статины ореолом загадочности.
Что произойдет, если уровень холестерина будет высок? Необязательно, чтобы он поступал извне; его избыток может также образовываться в печени. На вопрос, который сегодня задавался профессору Марееву — что будет, если ежедневно есть много холестерина или скушать его сразу много в течение одного дня, — он ответил, что последствия окажутся одинаковыми. В атерогенезе накопление холестерина не играет значительной роли.
Тем не менее, следование здоровому образу жизни и правильному питанию является важным аспектом в мотивации пациентов.
Если холестерина много, то происходит выраженный синтез (вернее, висцеральный адипоцит – особенная ткань. Она обладает очень высокой чувствительностью к липолитическому действию катехоламина и низкой чувствительностью к антилиполитическому действию инсулина. Это хороший плацдарм для инсулинорезистентности. Если липолиз выражен, то большое количество свободных жирных кислот попадает ни куда-нибудь, а именно в печень через воротную вену.
В организме уже идут определенные процессы. Триглицериды откладываются, синтезируются липопротеиды очень низкой плотности, что приводит к стеатозу органов.
Говоря сегодня об атеросклерозе как о возможной болезни печени, я хочу сказать, что это безобидное заболевание неалкогольная жировая болезнь печени, на мой взгляд, уже на стала только прерогативой лечения гастроэнтерологов. Это прерогатива лечения и терапевтов. У нее есть очень серьезные корреляционные связи с развитием различных сердечно-сосудистых катастроф. Это в большей степени касается стеатогепатита.
Естественное течение неалкогольной жировой болезни печени подразумевает прогрессирование через стадию неалкогольного стеатогепатита и фиброза, о которых мы сегодня много говорили. Мне хочется подробнее обсудить возможные механизмы развития неалкогольного стеатогепатита, перехода к фиброзу, циррозу и гепатоцеллюлярной карциноме (ГЦК). Однако большинство таких пациентов в конечном итоге умирает от инсульта и инфаркта.
Это подтверждается множеством исследований. Сердечно-сосудистые заболевания (ССЗ) являются основной причиной смерти между пациентами с неалкогольной жировой болезнью печени. Это связано с тем, что жир в печени ассоциирован как с традиционными факторами риска развития сердечно-сосудистых заболеваний, так и с суррогатными маркерами:
— изменение толщины комплекса итима-медиа;
— увеличение толщины перикардиального жира;
— увеличение риска по разным шкалам.
В частности, это можно оценить по Флемингенской шкале риска или рисковому индексу Про-Кам.
Неалкогольная жировая болезнь печени, так же как и атеросклероз, представляет собой хронический воспалительный процесс. Учёные проводили сравнительные исследования между пациентами с жировой печенью и без таковой, которые установили, что неалкогольная жировая болезнь печени сопровождается повышенными маркерами воспалительного стресса, такими как С-реактивный белок и фактор фон Виллебранда, что указывает на тромбофилический статус, и эти изменения происходят независимо от возраста, индекса массы тела и артериального давления.
Сейчас рассматривается очень много генов – кандидатов в развитии неалкогольной жировой болезни печени. Много работ посвящено функции микроРНК, которая способствует накоплению липидов и триглицеридов (ТГ) в культуре клеток и подавляет синтез ?-рецепторов.
Полиморфизм гена PNPLA3 подразумевает повышенный риск развития фиброза печени и более неблагоприятный прогресс заболевания. Также наблюдается полиморфизм гена MTP-493 G/T, кодирующий синтез белка адипонутрина.
Белок адипонутрин – ген Patatin-Like Phospholipasa Domain Containing 3находится в длинном плече 22-й хромосомы в положении 13.31. У человека в большей степени распределение таково, что он синтезируется в печени. Его энзиматическая активность проявляется в том, что изменяется активность, во-первых, глицерол фосфата ацилтрансферазы. Во-вторых, ацил глицерол фосфат ацилтрансфераза. Это два фермента, которые необходимы для нормальной работы в основном липопротеидов высокой плотности (ЛВП).
Низкий уровень ЛВП часто коррелирует с высоким содержанием триглицеридов. Адипонутрин косвенно влияет как на синтез триглицеридов в печени, так и на накопление жировой ткани.
В последние годы для изучения вклада полиморфизмов генов собраны достаточно значимые данные. Например, замена изолейцина на метионин в 148-ой позиции активно исследуется в различных популяциях. Данные, представленные на Европейском атеросклеротическом конгрессе в 2011 году, показывают, что частота минорных аллелей адипонутрина наиболее высока у латиноамериканцев и менее распространена среди афроамериканцев.
Эти данные заставляют нас говорить о том, что прогностическое значение или худший прогноз у пациентов с неалкогольной жировой болезнью печени будет наблюдаться у латиноамериканцев. Адипонутрин и его концентрация, синтез увеличиваются в гепатоцитах при ожирении.
Это связано не только с генетическими изменениями, но и с повышением свободных жирных кислот, что способствует накоплению триглицеридов. Увеличение триглицеридов приводит к образованию липопротеидов очень низкой плотности. Исследования показывают, что холестерин может оказывать влияние на активность глюкокиназы, что приводит к её подавлению. Некоторые эффекты статинов, такие как развитие новых случаев диабета, связываются именно с данным механизмом.
Есть определенные параллели в развитии фиброза печени и сердца. Они в рамках сегодняшнего выступления касаются ожирения и метаболического синдрома. Если посмотреть на клинические предикторы развития фиброза и цирроза печени при неалкогольном стеатогепатите, то они очень похожи на некоторые предикторы плохого сердечно-сосудистого риска.
Важными факторами являются Возраст, индекс массы тела, наличие сахарного диабета и артериальной гипертензии (АГ). Провоспалительный статус и повышенные уровни триглицеридов играют роль, равно как и коэффициент де Ритиса, применяемый для оценки статуса пациента в контексте инфаркта миокарда.
Следует отметить, что как в сердце, так и в печени развиваются фиброзные изменения. Механизмы фиброза, которые мы наблюдаем в основном в сердце, представляют собой реактивный фиброз, который может быть периваскулярным или интерстициальным. Периваскулярный фиброз чаще встречается у пациентов с диабетом, а интерстициальный (где накапливаются протеогликаны и элементы клеточного матрикса) характерен для пациентов с артериальной гипертензией.
Эпикардиальный жир имеет массу корреляций. Его толщина коррелирует с массой миокарда и с параметрами, которые характеризуют диастолическую функцию левого желудочка. Очень многие авторы пытаются рассматривать эпикардиальный жир как новый маркер ССЗ, оценивая в миллиметрах толщину этого жира.
Интересные данные можно получить при оценке эпикардиального жира: если его толщина превышает 7 мм, важно также измерить толщину комплекса интима-медиа, и она, скорее всего, окажется выше 0,9. Это указывает на наличие субклинического атеросклероза. Даже течение острого коронарного синдрома (ОКС) зависит от толщины эпикардиального жира.
Таким образом, мы можем с определенной долей допущения сказать, что эпикардиальный жир и жир в печени (что составляет больше 5% при биопсии) может служить определенным связующим звеном оценки возможного риска и фиброза того и другого органа. Измеряется это очень легко. Необходимо вывести парастернальную позицию по длинной оси. В конце систолы провести перпендикуляр к аортальному клапану.
На сечении аортального клапана, красной пунктирной линией выделена толщина эпикардиального жира, измеряемая в миллиметрах.
С другой стороны, выраженное количество эпикардиального жира у пациентов с неалкогольной жировой болезнью печени может рассматриваться как жировой «панцирь» сердца, что приводит к ухудшению релаксации сердца и нарушению диастолической функции.
Он опасен, потому что это та же самая висцеральная жировая ткань, активная. Нет фасции между эпикардиальным жиром и миокардом. Агент ангиотензин-2, свободные жирные кислоты непосредственно попадают в коронарные артерии. Жир сочетается и с эпикардиальным, и с эндокардиальным жиром.
Таким образом, можно утверждать, что жировая печень – это путь к атеросклерозу. Более того, я считаю, что жировая печень и атеросклероз – это две разные болезни, но они развиваются по схожим механизмам, включая инсулинорезистентность и выраженное наличие висцерального жира.
Опосредованные механизмы, которые в итоге приводят к тому, что у такого пациента повышается уровень мелких плотных ЛНП (инвазивные), которые внедряются в субэндотелиальное пространство. Снижение ЛВП.
Теперь, когда мы поняли, что существуют общие механизмы, возникает вопрос: как лечить эти два состояния. Исследование этих механизмов показывает, что препараты, которые доказали свою эффективность в снижении случаев сердечно-сосудистых заболеваний, должны также оказывать влияние и на здоровье печени.
Таким образом, в последнее время активно применяются статины. Вряд ли можно найти другой класс препаратов с таким убедительным воздействием на сердечно-сосудистую смертность и общую смертность. Однако многие врачи настороженно подходят к назначению статинов пациентам с диффузными заболеваниями печени, опасаясь их гепатотоксичности.
В 2010-м году была опубликована работа, которая попыталась раскрыть возможные механизмы влияния статинов при повышении, например, уровня трансаминаз. Оказывается, влияя на ГМГ КоА редуктазу, в то же время статины действуют на посттранскрипционную супрессию матричной РНК селенопротеинов. Действие на активность матричной РНК приводит к тому, что снижается активность очень важного фермента глутатион пероксидазы. Соответственно, снижается концентрация селена.
Это в свою очередь повышает чувствительность печени к любым повреждениям, особенно свободно-радикальным. В таких случаях употребление алкоголя или чрезмерное потребление жирной пищи однозначно увеличивает риск повышения уровня трансаминаз у таких пациентов.
Даже вскрыты молекулярные механизмы влияния статинов при неалкогольной жировой болезни печени. Статины влияют на метаболизм гена, который отвечает за прогрессирование фиброза и репаративные механизмы. Этот ген и его активность участвуют во влиянии на звездчатые клетки. Возможно участие в патогенезе цирроза печени.
Действие статинов на механизмы фиброза не однозначно. Например, в области атеросклеротических бляшек они способствуют усилению фиброза, что делает бляшку более прочной и устойчивой.
Сегодня вопрос о применении статинов у пациентов с заболеваниями печени практически решен после интересного исследования, проведенного Калазани в 2004 году, в котором приняли участие более 4 тысяч человек, распределенных на три группы.
Первой группе он дал статины, у них уровень трансаминазы был выше трех норм (не побоялся дать). Второй группе с нормальным уровнем трансаминаз он тоже дал статины. Третьей группе не дал статины, потому что трансаминазы были повышены. Понаблюдал за пациентами в течение 6-ти месяцев.
Исследования показали, что еще большее повышение уровня трансаминаз наблюдалось в группе, не получавшей статинов. После этого было проведено множество других исследований, подтверждающих, что статины могут улучшать фиброз печени в экспериментальных условиях.
Была тестирована гипотеза определения гепатотоксичности статинов у пациентов с заболеваниями печени. Это было ретроспективное исследование. 320 пациентов с неалкогольной жировой болезнью печени и хроническим (я хочу на это обязательно обратить внимание) гепатитом С. Прием статинов. Огромная доза. Такую дозу мы применяем довольно редко в клинической ситуации – 80 мг в день.
Сравнимая группа пациентов проходила наблюдение в течение 36 недель.
Полученные результаты выглядят следующим образом: уровень аланиновой трансаминазы увеличился на 7,5% у пациентов, проходивших лечение статинами, в то время как среди тех, кто не использовал статины, этот показатель достигал 12,5%. Это свидетельствует о статистически значительной разнице в повышении трансаминаз среди пациентов, не придерживавшихся защиты печени, включая, к примеру, людей с хроническим вирусным гепатитом С.
Потом появилась «первая ласточка» «Dallas Heart Study». 2264 пациента. 140 из них получали статины. Вывод: назначение статинов возможно у пациентов со стеатозом. В этом же исследовании тестировалась и активность адипонутрина.
Также было установлено, что существует связь между уровнем адипонутрина и трансаминаз.
В зависимости от того, находится перед нами гомозиготный или гетерозиготный пациент, уровень АЛТ увеличивается. У гомозиготных пациентов уровень АЛТ был самый высокий.
Мы продолжали исследование и теперь полагаемся только на подобные результаты. Использование статинов у больных с неалкогольной жировой болезнью печени, применяя морфологические методики, является весьма интересным направлением. Мы наблюдали за пациентами в течение длительного времени – целых 16 лет, проводили морфологические исследования.
На морфологическом уровне удалось подтвердить замедление процесса «трансформации» стеатогепатита в фиброз.
Клинические исследования. Небольшое количество пациентов. Здесь тоже есть интересные подводные камни. 45 пациентов с неалкогольной жировой болезнью печени, диабетом. Одной группе дают «Симвастатин» («Simvastatin»), а другой «Симвастатин» с «Эзетимибом» («Ezetinibe»).
«Эзетимиб» – это препарат, блокирующий всасывание холестерина в желудочно-кишечном тракте. В группе пациентов, принимающих только «Симвастатин», наблюдалось более существенное снижение уровня трансаминаз, чем у тех, кто проходил комбинированную терапию.
«Аторвастатин» («Atorvastatin»), конечно, здесь себя зарекомендовал больше всего, поскольку это наиболее применяемый статин. У него есть выраженные плейотропные свойства. Можно увидеть работу, когда по данным морфологического исследования отмечалось уменьшение степени жировой дистрофии гепатоцитов.
Имеется и наш собственный опыт работы с пациентами, у которых выявлен метаболический синдром в сочетании с неалкогольной жировой болезнью печени. У всех таких больных был диагностирован стеатоз, а 42% из них страдали от стеатогепатита.
Встал вопрос о том, как следует лечить пациентов с уровнем трансаминаз, превышающим три нормы. Здесь мы отслеживали клинические показатели, указывающие на риск развития фиброза и цирроза печени и уже обсуждали их. Без назначения статинов таким пациентам, отнесенным к категории очень высокого риска по сердечно-сосудистым заболеваниям, оставаться нельзя.
Есть ли какие-то подходы? Такие подходы есть. Мы применяли различные препараты, которые оказывают аддитивное влияние на уровень холестерина, которые защищают печень. На наш взгляд, довольно перспективно применение в данных ситуациях (конечно, это еще требует изучения) «Адеметионина» («Ademetionine»). Это источник естественных антиоксидантов при неалкогольной жировой болезни печени.
На активность митохондрий влияет множество факторов: это и увеличение оксидативного стресса, и повышение проницаемости мембран, и нейтрализация свободных радикалов, а также антиоксидантные свойства (например, «Адемитионин», «Гептрал» и стабилизация фиброгенеза). Все это обосновывает использование этих препаратов в лечении неалкогольной жировой болезни печени.
В заключение могу сказать, что на сегодняшний день атеросклероз – это не только болезнь сосудов. Сосуд – это то, что поражается в конечной стадии атеросклероза и то, с чем мы начинаем бороться, когда «поздно пить боржоми». Атеросклероз начинается с того, что печень не совсем правильно работает. Этому способствуют очень многие механизмы.
Функции холестерина
Липопротеиды в плазме делятся на два типа:
- Липопротеиды высокой плотности (ЛПВП) – они считаются «хорошим» холестерином.
- Липопротеиды низкой плотности (ЛПНП) – характеризуются низким содержанием белка и высоким содержанием холестерина, и их часто называют «плохим» холестерином.
ЛП низкой плотности опасны для здоровья, так как откладываются на сосудах, образуя атеросклеротические бляшки, что может привести к тяжелым заболеваниям.
Холестерин выполняет несколько важных функций в организме:
- Участвует в синтезе кортикостероидов и половых гормонов стероидного характера.
- Служит основой для образования витамина D и желчных кислот.
- Способствует регулированию проницаемости клеточных мембран и защищает эритроциты от токсинов.
- Придает клеточной мембране жесткость и стабилизирует ее текучесть.
- Оказывает защиту внутренним клеточным структурам от свободных радикалов.
Процессы в печени
Липопротеиды высокой плотности, находясь в кровотоке, поступают в печень. Половина из них используется для синтеза желчных кислот, которые становятся частью желчи и откладываются в желчном пузыре. При приеме пищи желчь попадает в кишечник, помогая в переваривании. Остальные липопротеины участвуют в дальнейших процессах жирового обмена.

Обмен липопротеинов в организме
Процесс синтеза холестерина в печени протекает в зависимости от его уровня в крови: при избытке – он замедляется, при нехватке – наоборот, активируется. Здоровые клетки печени могут поддерживать нормальные уровни холестерина, даже если в рационе много животных жиров или имеются вредные привычки и ожирение.
Однако приходит время, когда печень перестает выполнять эту функцию, и развивается нарушение липидного обмена. Это может быть вызвано несколькими факторами:
- Длительное избыток поступающего с пищей холестерина.
- Выработка холестерина в избыточных количествах.
- Недостаток или отсутствие клеточных рецепторов для захвата холестерина из крови.
- Трудности с выведением холестерина.
Таким образом, нарушения в работе органов и употребление в пищу большого количества продуктов, богатых холестеролом, приводит к нарушению обменных процессов в организме. Изменяются химические и физические свойства желчи, в желчном пузыре начинают формироваться и откладываться камни.
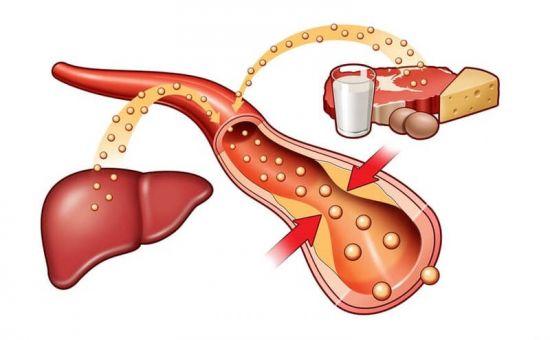
При увеличении уровня «плохого» холестерина в крови начинается его отложение на стенках сосудов, что способствует развитию атеросклероза.
Организм человека – саморегулирующаяся система, и при избытке липопротеидов включаются компенсаторные механизмы. Регулирование выработки холестерина начинается при его определенном уровне в крови.
При наличии различных патологий данные механизмы перестают функционировать, что приводит к накоплению холестерина в организме и создает угрожающие условия для здоровья.
Как снизить уровень холестерина
Корректировка образа жизни может существенно улучшить состояние здоровья, включая снижение уровня холестерина. Это, в свою очередь, позитивно скажется на функции печени, которая, хотя и обладает способностью к самовосстановлению, может сопротивляться этому процессу.
Уменьшите потребление насыщенных жирных кислот Жирные кислоты содержатся в жирном молоке, сыре, мясе, масле. Также они содержится в кокосовом и пальмовом масле.
Откажитесь от трансжиров. Эти вещества содержатся в готовых кондитерских изделиях, маргарине, крекерах, плавленом сыре и сухих супах. Важно внимательно изучать этикетки, поскольку трансжиры могут быть представлены как гидрогенизированные или частично гидрогенизированные.
Откажитесь от продуктов с высокой степенью переработки Эти типы продуктов содержат большое количество консервантов или искусственных красителей — синтетических ингредиентов, которые могут способствовать повреждению печени.
Используйте травы. Некоторые травы помогают снизить уровень холестерина. Исследования подтверждают положительное влияние черного тмина и зеленого чая.
Добавьте в свой рацион артишок обыкновенный. Исследования показывают, что регулярное употребление артишока, в том числе в виде добавок, поддерживает здоровье печени. Мета-анализы показывают, что экстракт артишока способствует снижению общего уровня холестерина, триглицеридов и фракции ЛПНП.
Исключите стимуляторы Если вы хотите поддержать состояние печени, стоит отказаться от стимуляторов — особенно от алкоголя. При употреблении его в чрезмерных количествах этому органу приходится проделывать большую работу по выведению вредных веществ.
Сократите количество принимаемых лекарств. По статистике, люди принимают около 2 миллиардов таблеток ежегодно, что может негативно сказываться на печени. Чтобы улучшить ее состояние, стоит снизить количество принимаемых препаратов до необходимого минимума.
Если вы хотите иметь крепкое здоровье, в первую очередь стоит обратить внимание на свой ежедневный рацион. Исключение продуктов, ухудшающих состояние печени и способствующих повышению холестерина, позволит избежать многих серьезных заболеваний.
Холестерин и неалкогольная жировая болезнь печени
Неалкогольная жировая болезнь печени (НАЖБП) характеризуется накоплением жиров в печени при отсутствии значительного потребления алкоголя. Существует ли связь между холестерином и НАЖБП?

Факторы риска для НАЖБП:
Факторы риска для этого заболевания сходны с факторами сердечно-сосудистых заболеваний и включают:
- ожирение,
- инсулинорезистентность,
- гипертония,
- дислипидемия (повышение уровней жиров в крови),
- высокий уровень холестерина и триглицеридов.
Развитие НАЖБП и его прогрессирование в неалкогольный стеатогепатит (НАСГ) включает множество механизмов, однако молекулярные, генетические и биохимические пути до конца не изучены, несмотря на значительные попытки разобраться в роли метаболизма жирных кислот и триглицеридов.
Роль холестерина и других липидов в развитии НАЖБП

Чтобы лучше понять значение липидов (группы органических веществ, включая жиры и холестерин) в прогрессировании НАЖБП, в исследованиях уделяли особое внимание анализу свободного холестерина в печени. Сравнительный анализ клеток здоровой печени и клеток с НАЖБП выявил повышенную концентрацию свободного холестерина и других липидов в пораженных клетках.
Результаты исследований показывают связь между диетическим холестерином и риском смерти и госпитализации из-за заболеваний печени. Также проводились исследования с использованием мышиных моделей для изучения роли диетического холестерина при НАЖБП.
Исследование метаболизма холестерина при НАЖБП и НАСГ
Также было проведено крупное исследование, в котором анализировались параметры обмена холестерина в НАЖБП и НАСГ. Участниками исследования стали четыре группы пациентов:
- первая группа – худощавые люди (контрольная группа),
- вторая группа – люди с избыточным весом (контрольная группа),
- третья группа – пациенты с НАЖБП,
- четвертая группа – пациенты с НАСГ.
По результатам исследования у пациентов с НАЖБП выявлено увеличении экспрессии фермента, ограничивающего скорость в синтезе холестерина по сравнению с пациентами контрольной группы нормального сложения и контрольной группы с ожирением.
Результаты этих исследований подчеркивают важность регулирования обмена холестерина в печени для развития и прогрессирования НАЖБП и НАСГ и открывают новые направления для дальнейших исследований.
Исследования показали, что пациенты, принимающие статины (препараты для снижения уровня липидов), по-разному реагируют на лечение:
- У больных с НАЖБП, получающих статины, не оказалось увеличения уровня ЛПНП (липопротеины низкой плотности, «плохой» холестерин),
- У пациентов с НАСГ без назначения статинов было отмечено увеличение ЛПНП.
Эти данные повышают вероятность того, что пациенты с НАЖБП по-разному реагируют на терапию статинами по сравнению с контрольными группами, и что нарушение экспрессии ЛПНП может ограничивать гиполипидемический эффект статинов. Эти данные требуют дальнейшего изучения, поскольку люди с НАЖБП страдают повышенным риском сердечно-сосудистых осложнений и пользуются эффективной гиполипидемической терапией.
Почему результаты этих исследований имеют столь важное значение?
В конечном счете, эти и другие исследования могут позволить улучшить терапию неалкогольной жировой болезни печени для снижения уровня заболеваемости у большого числа людей, которым грозит опасность сопутствующих осложнений в ближайшие годы.
Лечение неалкогольной жировой болезни печени
В настоящее время не существует утвержденных терапевтических подходов к лечению неалкогольной жировой болезни печени. Однако терапия всегда включает несколько этапов.
При наличии НАЖБП рекомендуется целенаправленно снижать вес через диету или увеличивая физическую активность.
Медикаментозная терапия должна быть направлена на коррекцию инсулинорезистентности, улучшение функции печени и снижение риска ассоциированных сердечно-сосудистых осложнений . Коррекция липидного профиля у пациентов с НАЖБП является важным звеном терапии, однако, статины в этом случае не являются препаратом первого выбора, даже несмотря на то, что пациенты с НАЖБП имеют высокий риск сердечно-сосудистых заболеваний, так как данная группа препаратов имеет токсическое действие на печень. Поэтому, особый интерес представляет возможность применения препаратов, позволяющих не только скорректировать дислипидемию, но и благотворно повлиять на состояние печени .
В журнале «Медицинский совет» опубликована статья, посвященная программе наблюдений, задача которой заключалась в оценке опыта использования препарата диоскореи (Вазоспонин) для терапии пациентов с неалкогольной жировой болезнью печени (НАЖБП) и дислипидемией.
Согласно данным исследования, включение препарата диоскореи в терапию неалкогольной жировой болезни печени позволяет добиться стойкого снижения атерогенных показателей липидограммы крови, нормализации биохимических маркеров функционального состояния печени, способствует снижению основных симптомов заболевания (слабости, утомляемости, боли, чувства тяжести в области ЖКТ, метеоризма, анорексии, тошноты).
Также было отмечено сокращение жесткости печени, что свидетельствует о регрессии умеренных проявлений фиброза. Это играет важную роль в улучшении прогноза и снижении риска прогрессирования НАЖБП.

Кроме того, предписаны препараты, которые увеличивают чувствительность клеток к инсулину и гепатопротекторы, такие как урсодезоксихолевая кислота или фосфолипиды. Эти средства способны ускорить процесс образования новых гепатоцитов и восстановить поврежденные клетки печени, улучшая их функциональное состояние и восстанавливая клеточные мембраны.
Кому показано определение холестерина в крови?

Определение холестерина в крови показано:
- при наличии сердечно-сосудистых заболеваний, таких как гипертония, ишемическая болезнь сердца, аритмии, а также перенесенные инфаркты или инсульты;
- дополнительно лицам с хроническими заболеваниями почек, диабетом, расстройствами щитовидной железы (гипотиреоз/гиперпаратиреоз) и ожирением;
- если в семье наблюдались случаи инфарктов или инсультов до 60 лет у женщин и 55 лет у мужчин, а также случаи внезапной сердечной смерти (отягощенная наследственность);
- при бесплодии и нарушениях менструального цикла;
- если имеются заболевания печени (для диагностики таких заболеваний);
- всем представителям мужского пола старше 40 лет и женщинам старше 50 лет или при наступлении менопаузы.
Как снизить уровень холестерина?

Коррекция уровня холестерина осуществляется через диетические рекомендации и изменения образа жизни, лечение заболеваний, способствующих росту холестерина, а также медикаментозную терапию для снижения его уровня.
Немаловажным является модификация образа жизни и лечение заболеваний-причин повышения холестерина. Регулярная физическая активность, отказ от курения и алкоголя, снижение избыточной массы тела/ожирения – основные факторы, которые улучшат состояние липидного спектра и печени, снизят риски сердечно-сосудистых осложнений и продлят вашу жизнь.
Вопрос о необходимости лекарственного лечения всегда решается индивидуально врачом на основании оценки сердечно-сосудистого риска. В настоящее время существует несколько групп медикаментов, предназначенных для достижения целевых значений липидограммы: препараты красного дрожжевого риса, статины, ингибиторы всасывания холестерина в кишечнике, фибраты, а также препараты полиненасыщенных жирных кислот. Использование этих препаратов отдельно или их отмена не рекомендуются без консультации врача.