При жировом гепатите печени важно учитывать, что любые лекарства, включая антиоксикапс, следует применять только по рекомендации врача. Антиоксиданты могут помочь в защите клеток печени, однако их применение должно быть обосновано и тщательно контролироваться.
Кроме того, лечение жирового гепатита подразумевает изменения в образе жизни, включая правильное питание и физическую активность. Поэтому перед началом приема антиоксикапс или других добавок необходимо проконсультироваться с медицинским специалистом.
- Жировой гепатит — это заболевание, связанное с накоплением жира в печени.
- Антиоксиданты могут помочь в борьбе с окислительным стрессом, но их использование требует осторожности.
- Применение антиоксидантов при жировом гепатите должно быть согласовано с врачом.
- Некоторые антиоксидантные препараты могут оказать положительное влияние на функцию печени.
- Важно учитывать индивидуальные особенности и сопутствующие заболевания пациента.
Гепатосан® представляет собой лиофилизированные гепатоциты, полученные из свиной печени.
В одной капсуле содержится:
Гепатосан® — 200 мг.
Титана диоксид — 1,333%; красители (желтый хинолиновый — 0,9197%, желтый закатный — 0,0044%), желатин до 100%.
Описание лекарственной формы
Капсулы имеют желтый цвет и выполнены из жесткого желатина номер 0. Порошок внутри капсулы светло-коричневого оттенка с характерным запахом.
Этот препарат способствует повышению детоксикационной и синтетической активности печени, улучшает обменные процессы в клетках печени и помогает в выведении токсинов. Механизм действия препарата охватывает две фазы: первая — кишечная, где происходит детоксикация путем сорбции токсинов, и вторая — метаболическая (гепатопротективная), когда компоненты препарата восстанавливают функциональные возможности печени. В состав препарата входят аминокислоты, микроэлементы, витамины, эссенциальные фосфолипиды, мезенхимальные ферменты, а также цитохромы.
Жировые заболевания печени
Неалкогольная жировая болезнь печени (НАЖБП) имеет множество причин, включая ожирение, употребление алкоголя и диабет. Симптомы, такие как усталость, диспепсия и дискомфорт в области правого подреберья, часто неясны и могут быть незамеченными. Игнорирование жировой болезни печени может привести к серьезным последствиям.
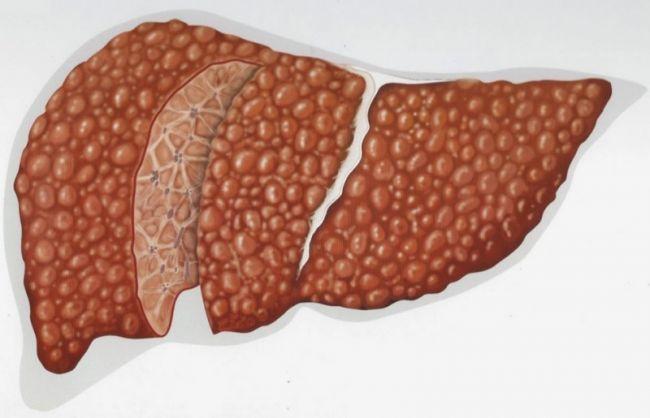
Накопление жира в печени (стеатоз) может вызывать окислительный стресс и хроническое воспаление, что в свою очередь приводит к жировому гепатиту (стеатогепатиту). Если заболевание не будет своевременно диагностировано и лечено, это может вызвать цирроз или, в худшем случае, гепатоцеллюлярную карциному. Поэтому, помимо физической активности, снижения веса и правильного питания, следует обратить внимание на современные медикаментозные методы лечения. В данном обзоре литературы рассматриваются клиническая эффективность и безопасность эссенциальных фосфолипидов при жировых заболеваниях печени.
Эссенциальные фосфолипиды образуют двойной слой клеточных и субклеточных мембран и контролируют их текучесть и биологическую активность (рис. 1). Эффективность ЭФЛ в лечении заболеваний печени была подтверждена способностью некоторых из их молекулярных компонентов интегрироваться в поврежденные части клеточных мембран печени (гепатоциты), тем самым улучшая способность печени к регенерации, а также увеличивая текучесть и функцию плазматических мембран гепатоцитов. ЭФЛ обладают антиоксидантными, антихолестатическими, противовоспалительными, антифибротическими и регенерирующими свойствами.
При жировом гепатите печени вопрос о применении антиоксидантов, в том числе и препарата «Антиоксикапс», требует тщательного рассмотрения. Этот препарат содержит ряд витаминов и активных компонентов, которые могут оказывать положительное влияние на обмен веществ и защитные функции клеток печени. Однако прежде чем принимать его, рекомендую проконсультироваться с врачом, поскольку лишь специалист может оценить индивидуальные характеристики вашего состояния и совместимость с другими методами лечения.
Важно отметить, что хотя антиоксиданты могут помочь в некоторых случаях, их использование не является универсальным решением для всех пациентов с жировым гепатитом. В некоторых клинических случаях избыточное потребление антиоксидантов может даже усугубить ситуацию, особенно если у человека есть сопутствующие заболевания или он принимает другие медикаменты. Поэтому важно положиться на мнение лечащего врача, который сможет дать рекомендации исходя из общего состояния здоровья и специфики заболевания.
В дополнение к приему «Антиоксикапс» следует рассмотреть изменения в образе жизни, включая диету и физическую активность. Эти факторы играют существенно важную роль в терапии жирового гепатита. Медицинский подход к лечению должен быть комплексным, и антиоксиданты могут быть частью этого подхода, но не единственным решением. Не забывайте о необходимости регулярного мониторинга состояния печени и соблюдении рекомендаций вашего врача.
Рис. 1. Эссенциальные фосфолипиды участвуют в формировании клеточных мембран гепатоцитов, что способствует улучшению клеточной активности за счет повышения мембранной текучести, тем самым улучшая обмен веществ и работу рецепторов (по материалам Gundermann et al., 2016).
Препарат рекомендуется для улучшения самочувствия при токсическом или пищевом поражении печени (например, из-за алкоголя, лекарств или несбалансированного питания, ведущего к ожирению и гиперлипидемии), а также при алкогольной или неалкогольной жировой болезни печени (АЖБП, НАЖБП) и гепатите. Тем не менее, применение ЭФЛ не может компенсировать потребление гепатотоксичных веществ, таких как алкоголь, и не заменяет комплексного подхода к изменениям образа жизни, включая уменьшение жировых отложений при избыточной массе тела и ожирении.
Обычная рекомендуемая суточная доза ЭФЛ для детей от 12 лет и старше и для взрослых пациентов составляет 1800 мг: 3 приема по 600 мг. Продолжительность лечения не ограничена по времени. Нормализация показателей ферментов в сыворотке крови у 17 пациентов с жировой дегенерацией печени было показано после 20 дней лечения. По сравнению со значениями до лечения средняя активность сывороточного содержания ГГТ была значительно снижена через 1, 3 и 6 месяцев терапии с помощью ЭФЛ, тогда как в контрольной группе (плацебо) отклонения не были статистически значимыми [2].
Единственное противопоказание к применению ЭФЛ — это гиперчувствительность к основному ингредиенту или каким-либо вспомогательным компонентам (например, соевому маслу). Взаимодействия с другими препаратами встречаются редко, однако не исключены потенциальные взаимодействия ЭФЛ с антикоагулянтами, что может потребовать корректировки дозы последнего.
Редкие побочные реакции могут включать расстройства пищеварения: тошноту или рвоту, диарею, мягкий стул и вздутие живота. К очень редким явлениям относятся аллергические реакции, такие как сыпь и крапивница.
Резюме
Обзор литературы показал, что ЭФЛ оказывают благоприятное воздействие при лечении жировой болезни печени и хорошо переносятся. По мнению авторов, этот вывод подтверждается тем, что все заболевания печени связаны с повреждением клеточных мембран, а ЭФЛ положительно влияют на состав и функцию мембран.
Печень выполняет ключевые метаболические функции и играет важную роль в поддержании врожденного иммунитета и системного гуморального иммунитета. Фосфолипиды способны способствовать поддержанию и восстановлению здоровья печени.
Размер файла: 132KB
При жировом гепатите печени можно принимать антиоксикапс таблеточки можно или нет
1 ГОУ ВПО «Воронежская государственная медицинская академия им. Н.Н. Бурденко Минздравсоцразвития России»
Проведен анализ возможного влияния стеатоза печени на эффективность комплексной противовирусной терапии (КПВТ) хронического вирусного гепатита С (ХВГС). Группа больных ХВГС с гистологически доказанным стеатозом печени (14 человек) сравнивалась с группой больных ХВГС (15 человек) без признаков стеатоза печени.
Пациенты обеих групп получали комбинированную противовирусную терапию (ПЕГ-интерферон+рибавирин) в соответствии с установленными схемами в течение 24 или 48 недель в зависимости от генотипа вируса (3а и 1b). Первоначальная биопсия показала наличие стеатоза печени у 48,3% (14/29) с хроническим вирусным гепатитом С. При генотипе 3а стеатоз печени встречался значительно чаще по сравнению с генотипом 1b (почти в два раза).
В целом (вне зависимости от наличия стеатоза) эффективность комбинированной терапии составила 62,1% среди пациентов с хроническим вирусным гепатитом С. Анализ показал, что стеатоз негативно сказывался на эффективности противовирусного ответа.
УВО чаще отмечался среди пациентов без стеатоза (61,1%) по сравнению с 50,0% при наличии стеатоза, хотя это различие оказалось недостоверным (P>0,05). Вместе с тем наблюдалось также и обратное влияние – КПВТ на стеатоз. Так, в результате эффективной противовирусной терапии стеатоз печени часто регрессировал и даже полностью исчезал. Достоверным снижение частоты стеатоза под влиянием успешной КПВТ было только при 3а генотипе HCV (стеатоз исчезал у половины таких больных). Тем не менее наличие стеатоза печени при ХВГС не является противопоказанием к проведению КПВТ.

110 KB рибавирин, пег-интерферон, противовирусная терапия, стеатоз печени, хронический вирусный гепатит С.
1. Абдурахманов Д.Т. Стеатоз печени при хроническом гепатите С: механизмы развития и роль в прогрессировании заболеваний печени // Клиническая гепатология. — 2005. — № 1. — С. 25-28.
2. Притулина Ю.Г., Целиковский А.В. Жировая дистрофия печени — отличительная черта вирусного гепатита С, вызванного генотипом 3а вируса HCV // Актуальные проблемы инфекционной и неинфекционной патологии : сб. науч. работ, посвящ. 55-летию деятельности Левиной Л.Д. — Ростов н/Д, 2005. — C. 178-179.
3. Alter M.J. Эпидемиология вирусного гепатита и сопутствующей инфекции ВИЧ // J. Hepatol. — 2006. — Vol. 44. — № 1 Suppl. — P. 6-9.
4. Cross T.J.S. Воздействие стеатоза печени на естественное течение хронической инфекции гепатитом C // J. Viral. Hepat. — 2009. — Vol. 16. — № 7. — P. 492-499.
5. Kleiner D.E. Разработка и валидация системы гистологической оценки неалкогольной жировой болезни печени // Hepatology. — 2005. — Vol. 41. — № 6. — P. 1313-1321.
6. Lauer G.M., Walker B.D. Hepatitis C virus infection // N. Engl. J. Med. — 2001. — Vol. 345. — № 1. — P. 41-52.
7. Scheuer P.J. Патология гепатита C // Hepatology. — 1992. — Vol. 15. — № 4. — P. 567-571.
Актуальность проблемы. Хроническим гепатитом C (HCV) страдают примерно 3-5% населения мира, что соответствует минимум 200 миллионам человек [5].
На сегодняшний день «золотым стандартом» лечения хронического вирусного гепатита С (ХВГС) является комбинированная противовирусная терапия (КПВТ) препаратами пегилированного интерферона и рибавирина, которая, однако, оказывается эффективной лишь у 50-80% пациентов [5; 6]. Поэтому вопрос о влиянии различных исходных факторов со стороны вируса или больного на эффективность такой терапии остается крайне актуальным. С другой стороны, высокая стоимость препаратов и большое количество побочных эффектов ограничивают их применение. Прогнозирование эффективности проводимой противовирусной терапии возможно путём оценки динамических (изменяемых в процессе лечения) и генетически детерминированных (независимых) факторов.
Стеатоз печени, который присутствует у пациента, может снижать эффективность противовирусной терапии ХВГС на 30% [1; 6; 7]. Данные исследований показывают, что стеатоз у 30-70% пациентам с ХВГС обнаруживается при биопсии [1; 6].
В общей популяции частота стеатоза не превышает 10% [5; 6], что подразумевает наличие взаимосвязи между ХВГС и стеатозом печени. К тому же, последние исследования подтверждают, что стеатоз печени ускоряет развитие фиброза, и относительно 3а генотипа HCV формируется мнение, что фиброз быстрее прогрессирует по сравнению с 1 генотипом [6]. Стеатоз служит морфологическим индикатором хронической HCV-инфекции, отражая непосредственное цитопатогенное воздействие вируса на гепатоциты и показывая зависимость его активности от вирусного размножения в печени. Ранее мы выявили, что частота и серьезность стеатоза печени интенсивнее при генотипе 3а HCV, чем при 1b [2].
Таким образом, стеатоз печени на фоне ХВГС является актуальной проблемой современной инфектологии в связи с высокой распространенностью, тяжелыми последствиями и негативным влиянием на эффективность противовирусной терапии.
Цель исследования. Задачи исследования сформулированы следующим образом:
1) выяснить частоту и выраженность стеатоза печени у пациентов с хронической HCV-инфекцией для разных генотипов HCV;
2) определить влияние стеатоза печени на эффективность КПВТ как в целом, так и для различных генотипов HCV.
Материалы и методы. Исследование было проведено на базе БУЗ ОКИБ г. Воронежа за период с марта 2005 по февраль 2011 г. До начала КПВТ (пегинтерферон + рибавирин) все 29 пациентов были наивными по КПВТ (ранее никто из них не получал противовирусной терапии по поводу ХВГ). Все пациенты были старше 18 лет. Критериями исключения пациентов были: 1) наличие сопутствующей патологии печени (гепатит В, первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) или любое заболевание печени в стадии декомпенсации; 2) наличие сахарного диабета и/или явных клинико-лабораторных проявлений метаболического синдрома, в т.ч. инсулинорезистентности, определяемой по индексу HOMA; 3) коинфекция ВИЧ; 4) регулярное употребление алкоголя более 50 г/день у мужчин и 25 г/день у женщин в течение последних двух лет перед началом КПВТ; 5) наличие предшествующего противовирусного лечения по поводу ХВГС; 6) длина печеночного биоптата менее 10 мм или наличие в биоптате менее 4 портальных трактов; 7) наличие любого из общепринятых противопоказаний для проведения КПВТ.
Каждому пациенту с ХВГС дважды проводили слепую чрескожную биопсию печени по методике Менгини: первая — в течение 6 месяцев до начала КПВТ, вторую — после завершения терапии. Парафиновые образцы печени оценивались в сертифицированной лаборатории ЮВЖД одним и тем же гистологом, который не имел информации о пациенте, кроме факта наличия у него хронической HCV-инфекции. Образцы окрашивались гематоксилин-эозином, а для оценки фиброза использовалась окраска на ретикулин.
Гистологическая активность гепатита и степень (стадия) фиброза оценивались по шкале Knodell и Metavir. Степень (выраженность) стеатоза (S) определялась по классификации Kleiner [5] в зависимости от процента гепатоцитов с жировыми вакуолями: S0 — менее 5%, S1 — 5-33%, S2 — 33-66% и S3 — более 66%. Классификацию долькового воспаления по Kleiner и соавт. (2005) не применяли в данной работе, так как она уже учитывается в индексе гистологической активности (ИГА) по Knodell. Поскольку число пациентов в группах S1, S2 и S3 было незначительным, эти группы были объединены, и для анализа влияния стеатоза на эффективность противовирусной терапии ХВГС сравнивали только две группы: без стеатоза (S0) и с его наличием (S1+S2+S3).
Длительность КПВТ пегилированным (ПЭГ) интерфероном и рибавирином составляла в зависимости от генотипа HCV 24 недели (3 генотип HCV) или 48 недель (1 генотип). Использовались либо пегилированный интерферон альфа-2а (Пегасис) 180 мкг п/к 1 раз в неделю, либо пегилированный интерферон альфа-2b (ПегИнтрон) 100-150 мкг п/к 1 раз в неделю в зависимости от массы тела (предварительный анализ не выявил статистических различий между этими двумя препаратами в нашем исследовании). Рибавирин назначался в зависимости от массы тела в суточной дозе 1000-1200 мг per os, разделенной на 2 приема в день.
Эффективность КПВТ определялась процентом пациентов с ХВГС, достигших устойчивого вирусологического ответа. Устойчивый вирусологический ответ (УВО) означал отсутствие РНК HCV в крови через 24 недели после завершения терапии.
Все пациенты прошли полное клиническое обследование, включая серологию на маркеры вирусных гепатитов В, С, D с помощью методов ИФА и молекулярной диагностики (ПЦР), а также определение уровня α-фетопротеина, содержания железа и меди в сыворотке крови. Перед началом КПВТ серологически исключалось наличие аутоиммунного гепатита и других связанных состояний.
Всем больным выполнялись ФГС и УЗИ органов брюшной полости утром натощак после минимум 10-часового голодания.
Каждому пациенту была выполнена двукратная пункционная биопсия печени, а также проведена фиброэластометрия с использованием фиброскана (Fibroscan FS-502, Echosens, Франция). Однако для оценки степени (выраженности) фиброза печени основное внимание было уделено результатам пункционной биопсии.
Для диагностики инсулинорезистентности (ИР) применялся HOMA-индекс, который рассчитывался по формуле: HOMAИР = инсулин натощак (мЕ/л) × глюкоза натощак (мМоль/л) / 22,5 (норма для взрослых — значение выше 2,5 указывает на инсулинорезистентность). В данное исследование не включались пациенты с установленной ИР.
Результаты показали, что, как и в большинстве глобальных исследований [1-3], среди наших пациентов преобладал генотип HCV 1b. Частота его встречаемости составила 58,6% (17 из 29), тогда как генотип 3a был выявлен у 41,4% (12 из 29). В данном исследовании не было зарегистрировано другие генотипы.
По данным первой биопсии (таблица 1), стеатоз печени был отмечен у 48,3% (14/29) больных ХВГС. У 51,7% (15/29) стеатоза не было — S0, у 27,6% (8/29) отмечался легкий стеатоз — S1, у 24,1% (4/29) — стеатоз был умеренным — S2, и у 6,9% (2/29) он был выраженным — S3.
Таблица 1 — Характеристика пациентов в зависимости от наличия и степени стеатоза печени перед началом КПВТ
С наличием стеатоза (S1+S2+S3),
Без стеатоза (S0), N=15
НАЖБП и стеатогепатит – одни из самых распространенных болезней печени
Суть этих двух заболеваний заключается в накоплении жира внутри печени. Жировая болезнь чаще развивается у людей с ожирением, особенно с явным накоплением жира в области живота. У таких пациентов часто наблюдаются и другие негативные последствия, связанные с ожирением:
- Диабет второго типа — в 75% случаев.
- Повышенный уровень холестерина — в 92% случаев.
Практически у всех больных возникает гипертония, обусловленная скоплением холестерина в сосудах и сопутствующими заболеваниями почек.
Отложение жира часто сопровождается воспалительным процессом в печени – стеатогепатитом. НАЖБП и стеатогепатит постепенно переходят в печёночный фиброз – состояние, при котором печеночные клетки заменяются соединительной тканью. В результате орган не может выполнять свои функции, и у заболевшего возникает печёночная недостаточность.

Особенно часто такая ситуация развивается, если пациент не изменяет свой образ жизни — не снижает вес и продолжает употреблять пищу, богатую холестеринами.
Аспирин останавливает симптомы
Регулярное употребление аспирина способствует снижению проявлений заболевания и уменьшает риск развития фиброза. Это было отражено в исследовании, опубликованном в журнале «Clinical Gastroenterology and Hepatology».

Ученые изучали взрослых с указанными болезнями с 2006 года. Всем участникам проводили биохимические анализы крови и УЗИ печени для оценки состояния органа. Также была выполнена биопсия для гистологического анализа образцов тканей.
Пациенты принимали аспирин и регулярно обследовались на фиброз. Прием лекарства осуществлялся в течение 9 лет. Оказалось. что оно тормозит фиброз и позволяет сохранить функцию печени:
- Из 361 пациента, 151 человек (41,8%), принимающих аспирин ежедневно, заболевали фиброзом на 34% реже, и результаты их печеночных проб оставались стабильными или улучшались. Таким образом, можно утверждать, что заболевание в этой группе «замерло».
- У 17 пациентов, у которых на старте исследования уже были признаки фиброза, заболевание прогрессировало у 86. Среди них количество больных, принимавших ежедневно аспирин, было ниже на 63%.
Авторы сделали вывод, что полученные данные позволяют считать аспирин гепатопротектором — средством, которое защищает печень. Исследования, направленные на изучение механизмов воздействия аспирина на функции печени, могут способствовать разработке новых препаратов для лечения заболеваний этого органа.
Напитки и рецепты для восстановления и очищения печени
В этом разделе будут рассмотрены различные напитки и рецепты, которые могут поддержать восстановление и очищение печени. Используйте данные рекомендации для улучшения состояния этого важного органа.
- Зеленый чай: Один из наиболее популярных и полезных для печени напитков. Благодаря антиоксидантным свойствам, он способствует выведению токсинов, улучшению пищеварения и снижению уровня жира в печени.
- Цитрусовые: Лимоны, апельсины и грейпфруты богаты витамином C, который необходим для выработки печени ферментов для удаления токсинов. Регулярное потребление цитрусовых или свежевыжатых соков может значительно улучшить состояние печени.
- Имбирный чай: Имбирь обладает противовоспалительными свойствами и помогает улучшить пищеварение и общее состояние печени. Чай можно приготовить, нарезав свежий имбирь и залив его горячей водой. Для улучшения вкуса добавьте лимон и мед.
- Зеленый сок: Шпинат, петрушка, базилик и руккола содержат много антиоксидантов и фитонутриентов, способствующих очищению печени. Сделайте зеленый сок, смешав эти ингредиенты с водой в блендере или соковыжималке, и добавив немного лимона для свежести.
- Чистая вода: Не забывайте пить достаточное количество воды в течение дня, это важно для нормальной работы печени. Вода помогает вымывать токсины и поддерживает водный баланс клеток печени.
Включение этих напитков в ваш рацион может помочь восстановить и очистить печень, повышая ее функциональность и улучшая общее состояние здоровья. Однако перед внесением изменений в свой рацион всегда рекомендуется проконсультироваться с врачом или диетологом.
Видео по теме:
Какие напитки рекомендуются при жировом гепатозе печени?
При жировом гепатозе печени рекомендуется потреблять больше воды, натуральные соки без сахара, зеленый чай и травяные отвары.
Можно ли пить алкогольные напитки при жировом гепатозе печени?
Употребление алкоголя при жировом гепатозе строго не рекомендуется. Алкоголь может усугубить уже существующие повреждения печени и усиливать симптомы заболевания.
Какие типы напитков следует избегать при жировом гепатозе печени?
При жировом гепатозе печени следует избегать напитков, которые содержат большое количество сахара и кофеина, газированных и энергетических напитков, а также сладких алкогольных коктейлей.
Можно ли пить газированные напитки при жировом гепатозе печени?
Газированные напитки не советуются при жировом гепатозе печени, так как они могут вызвать вздутие живота и усугубить симптомы заболевания.
Какой вред могут нанести сладкие прохладительные напитки при жировом гепатозе печени?
Сладкие безалкогольные напитки, содержащие повышенное количество сахара, увеличивают нагрузку на печень и способствуют прогрессированию жирового гепатоза. Кроме того, они могут привести к накоплению лишнего веса, что также негативно сказывается на здоровье печени.