Даклавизар и совальди, применяемые для лечения гепатита C, могут вызывать побочные эффекты, однако в большинстве случаев они являются легкими и проходят после завершения курса лечения. У пожилых пациентов возможны более серьезные реакции, поэтому важно внимательно следить за состоянием здоровья и консультироваться с врачом.
Хотя побочные эффекты при использовании этих препаратов, как правило, не угрожают жизни, у пожилых людей может быть повышенный риск развития осложнений. Поэтому перед началом терапии нужно тщательно оценить общее состояние здоровья пациента и рассмотреть все возможные риски.
- Даклавизар и софосбувир используются для лечения гепатита С.
- Основные побочные эффекты включают усталость, головную боль и тошноту.
- У пожилых пациентов побочные эффекты могут проявляться сильнее из-за сопутствующих заболеваний.
- Важно наблюдать за состоянием больных после окончания лечения для предотвращения осложнений.
- В большинстве случаев лечение безопасно при соблюдении рекомендаций врача.
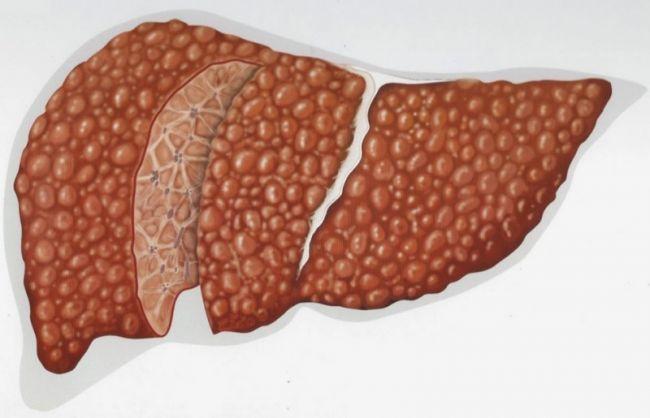
Гепатит С представляет собой угрожающее инфекционное заболевание, которое сопровождается серьезным воспалением и повреждением печени. Инфекция может произойти через контакт с кровью инфицированного, в ходе медицинских и косметических процедур, а также при сексуальных контактах. Процесс лечения этой болезни длителен и требует назначения специальных противовирусных препаратов. Эти медикаменты могут быть высокими по цене, и эффективность лечения во многом зависит от регулярности приема и соблюдения других указаний. Одна из популярных схем терапии гепатита С включает в себя прием Софосбувира и Даклатасвира, которая дает положительные результаты при различных генотипах вируса.
Оригинальные препараты, используемые для лечения гепатита С (Sovaldi и Daklinza), изготавливаются в Соединенных Штатах. Хотя они обладают высокой эффективностью, их главной проблемой является стоимость, что делает невозможным для многих пациентов пройти полный курс лечения и избавиться от гепатита.
Аналоги этих запатентованных американских препаратов – Софосбувир и Даклатасвир, производятся в Индии и содержат те же активные вещества. Такие препараты называются дженериками – это альтернативы оригинальным средствам. Они прошли все необходимые тестирования и имеют соответствующую документацию, подтверждающую их качество. Благодаря появлению этих дженериков на рынке, многие пациенты получили возможность пройти качественное лечение с минимальными побочными эффектами, что помогло им избавиться от гепатита С.
Ранее лечение гепатита С осуществлялось при помощи интерферонов – препаратов, которые активируют иммунную защиту организма в борьбе с вирусной инфекцией. Они не отличались особой эффективностью, имели ряд противопоказаний и вызывали серьезные эффекты. Единственное, что стимулировало пациентов отказываться от более качественных лекарств и останавливать выбор на интерферонах – это их низкая стоимость. Препараты Софосбувир, Даклатасвир и другие дженерики доказали свою эффективность против вирусного гепатита и имеют несколько преимуществ:
При назначении препарата Даклавизар совальди, который используется для лечения хронического гепатита C, важно учитывать возраст и общее состояние здоровья пациента. У пожилых людей организм зачастую менее устойчив к лекарственным препаратам, и побочные эффекты могут проявляться более ярко. Исследования показывают, что у старшей категории пациентов побочные эффекты могут продолжаться дольше и проявляться в более тяжелой форме, что требует внимательного мониторинга.
В процессе терапии далеко не всегда удается предсказать, когда конкретные побочные эффекты у пациента прекратятся. Некоторые из них могут быть временными, но в отдельных случаях — хроническими. Совета по обязательному контролю за состоянием здоровья пациентов, особенно пожилых, стоит придерживаться особенно тщательно. Подход к лечению таких пациентов должен быть индивидуальным, с акцентом на регулярные медицинские осмотры и оценку побочных эффектов.
Что касается опасности побочных эффектов для жизни пожилых людей, то при наличии сопутствующих заболеваний и ослабленного иммунитета риск может увеличиваться. Поэтому крайне важно, чтобы лечение проводилось под наблюдением опытных специалистов. Они могут в любой момент вмешаться в терапевтический процесс, чтобы минимизировать риски и адаптировать лечение для достижения наилучших результатов с учетом состояния здоровья пациента.
- вызывают незначительные побочные реакции;
- легко переносятся пациентами, включая пожилых;
- обладают высокой эффективностью, что сокращает продолжительность противовирусной терапии в 2–3 раза;
- могут применяться даже при наличии ослабленного иммунитета и осложнений, таких как цирроз печени и ВИЧ.
Препарат Софосбувир создан специально для борьбы с гепатитом С. Его действие основывается на нарушении репликации вируса, воздействуя на процессы его РНК. Кроме того, данный препарат способствует укреплению иммунных сил организма и может быстро снижать вирусную нагрузку.
При его применении курс терапии продолжается не более 24 месяцев и заканчивается выздоровлением. При осложненных формах и в сочетании с другими патологиями (циррозом, ВИЧ) лечение более длительное, осуществляется комбинацией нескольких специфических средств. Одно из них – это таблетки Даклатасвир. Появление этого препарата и определение эффективности комбинации двух медикаментов позволяет полностью отказаться от приема более токсичных интерферонов.

Даклатасвир применяется в качестве дополнения к Софосбувиру, а не в качестве самостоятельного средства.
Схема применения дженериков для разных генотипах гепатита С
Протокол лечения гепатита С с использованием Софосбувира и Даклатасвира может варьироваться в зависимости от генотипа вируса и наличия сопутствующих заболеваний. В случаях без осложнений для лечения достаточно принимать Софосбувир по предписанию. Длительность курса составляет 8 недель, по истечении которых контрольный анализ покажет значительное уменьшение концентрации вируса. У некоторых пациентов возможно полное выздоровление за этот период, а в других случаях стойкий результат может проявиться уже через месяц.
Перед началом терапии необходимо выявить генотип вируса гепатита С. Этот вирус имеет различные варианты, которые отличаются по своим свойствам и влиянию на печень. Всего выделяют 6 генотипов, при этом самым опасным считается генотип 1, так как он наиболее сложно поддается лечению. Наиболее распространены генотипы 2 и 3.
Лечение вирусного гепатита С 1 генотипа
Для пациентов с 1 генотипом применяется лечение с помощью Софосбувира и Ледипасвира или Даклатасвира, а также их комбинаций. В отсутствие ВИЧ курс лечения длится 12 недель, после чего проводится контрольный анализ. Если присутствует ВИЧ, терапия может имей продолжительность до 24 недель.
Для терапии хронического гепатита С 1 генотипа рекомендован Софосбувир в следующих комбинациях:
- в комбинации с Ледипасвиром или с Ледипасвиром и Рибавирином;
- с Даклатасвиром или с комбинацией Даклатасвира и Рибавирина;
- с Симепревиром;
- непосредственно с Рибавирином или с Рибавирином и Пегинтерфероном.
Воспаление печени различной природы несет риски для человека. При отсутствии соответствующего лечения оно может привести к циррозу, при котором нормальная ткань заменяется соединительной. Это состояние представляет серьезную опасность для жизни и затрудняет терапию вирусного гепатита. При наличии цирроза и воспаления печени могут применяться следующие схемы лечения с использованием Софосбувира:
- с Ледипасвиром или с Ледипасвиром и Рибавирином;
- с Симепревиром или с Симепревиром и Рибавирином;
- с Рибавирином или с Рибавирином и Пегинтерфероном.
Многие пациенты возвращаются к лечению повторно за несколько лет. Подбор подходящего протокола может быть затруднен, особенно до появления дженериков. Комбинации Софосбувира рекомендуется назначать в случаях отсутствия положительного ответа на прежние методы терапии. Курс длится 12 недель, и препарат можно комбинировать следующим образом:
- с Ледипасвиром или с Ледипасвиром и Рибавирином;
- с Симепревиром;
- с Рибавирином или с Рибавирином и Пегинтерфероном.
Самое опасное осложнение инфекционного воспаления печени – это ВИЧ. Эти два заболевания часто проявляются совместно, и курс терапии будет длительным. Лечение специфическими препаратами может продолжаться до 24 недель, и его эффективность может отличаться. Софосбувир в такой ситуации можно сочетать следующим образом:
- в комбинации с Ледипасвиром на протяжении 12 недель – эффективность 97 %;
- с Даклатасвиром в течение 12 недель – эффективность 97 %;
- с Рибавирином на протяжении 24 недель – эффективность до 82 %.

Прежде чем начать лечение, важно провести анализ для определения генотипа вируса.
Генотип 1 считается наиболее опасным, поскольку многим пациентам не удается избавиться от вируса даже после длительного лечения. Возбудитель персистирует в печеночной ткани и периодически провоцирует обострение болезни. Однако лекарственные средства нового поколения оказались более эффективными, и шанс на выздоровления при многих комбинациях достигает до 100%.
Схема терапии при 2 генотипе вируса
Генотип 2 вируса встречается повсеместно и встречается у большинства пациентов с данным диагнозом. Для его терапии Софосбувир оказывается эффективным в комбинации с:
- с Даклатасвиром – при курсе лечения 24 недели его эффективность достигает 100 %;
- с Рибавирином – при терапии продолжительностью 12 недель эффективность составляет 94 %;
- с Даклатасвиром и Рибавирином – при курсе 24 недели эффективность тоже достигает 100 %.
В случаях сочетания данного генотипа с ВИЧ для терапии используется стандартная комбинаторика Софосбувира и Даклатасвира. При терапии в течение 12 недель эффективность составляет до 88%, а при 24-недельном лечении – до 100 %.
Второй генотип сравнительно легко поддается лечению. Схемы терапии простые и не требуют применения интерферонов. При наличии осложнений курс придется продлить в 2 раза, но по его окончании можно полностью избавиться от возбудителя гепатита.
Применение медикаментов для пациентов с 3 генотипом
Гепатит С 3 генотипа является одним из наиболее распространенных. Для его лечения предпочитают использовать менее токсичные препараты, однако если они не дают результата, может потребоваться назначение интерферонов. Стандартные схемы лечения с использованием Софосбувира следующие:
- с Даклатасвиром (12 недель, 94 %);
- с Рибавирином (24 недели, 100 %);
- с Рибавирином и Пегинтерфероном (24 недели, 100 %).
Существует и способ лечения гепатита С 3 генотипа, если ранее назначенный пациенту курс терапии оказался малоэффективным. Он будет включать Софосбувир и другие препараты:
- с Рибавирином (24 недели, 85 %);
- с Рибавирином и Пегинтерфероном (12 недель).
3 генотип гепатита С в сочетании с циррозом печени или ВИЧ помогает излечить с помощью схемы, состоящей из Софосбувира и Рибавирина. Курс терапии в обоих случаях продолжается 24 недели, но его эффективность отличается. При циррозе печени эффективность достигает 86 %, а в случае с ВИЧ – до 91 %.
Терапия 4 генотипа вируса гепатита С
4 генотип встречается сравнительно редко. Вирус плохо поддается терапии, а схемы лечения схожи с подходами, применяемыми для 1 типа вируса. Эффективность различных схем может варьироваться от 89 до 100 %, что является хорошим результатом.

Дженерики – это аналоги оригинальных лекарственных препаратов, которые показывают не меньшую эффективность
При неосложненном гепатите С применяются такие комбинации Софосбувира:
- с Ледипасвиром на протяжении 12 недель;
- с Рибавирином и Пегинтерфероном на протяжении 12 недель;
- с Рибавирином – курс длится 24 недели.
При сочетании вирусного гепатита 4 генотипа с циррозом печени можно выбрать одну из следующих комбинаций Софосбувира;
- с Ледипасвиром – 12 недель;
- с Рибавирином – 24 недели.
При диагностике данного вида вирусного гепатита в сочетании с ВИЧ назначается Софосбувир совместно с другими препаратами:
- с Даклатасвиром на протяжении 12 недель;
- с Рибавирином и Пегинтерфероном также на протяжении 12 недель.
Если пациенты с гепатитом С не показывают положительного результата на все способы лечения, допускается использование Софосбувира в сочетании с другими препаратами:
- с Ледипасвиром – 12 недель;
- с Рибавирином – 24 недели.
Перед началом лечения у пациента определяют концентрацию вируса в крови. Повторные анализы необходимо сдавать в течение приема медикаментов, чтоб определить эффективность лечения. Если лекарства не подходят больному, лечение можно будет пройти затем заново с использованием более сильных препаратов.
Фармакологическое действие
Фармакологические характеристики Совальди зависят от активного ингредиента – Софосбувира (Sofosbuvir). Этот компонент является нуклеотидным аналогом, предназначенным для комбинированного лечения гепатита.
Препарат используется для терапии гепатита C. Молекулярная формула состоит из двадцати двух молекул углерода, двадцати девяти молекул водорода, одной молекулы фтора, трех молекул азота, девяти молекул кислорода и одной молекулы фосфора. Лекарственное средство Всемирной Организации Здравоохранения включено в список жизненно важных препаратов.
Активное вещество ингибирует рибонуклеиновую кислоту полимеразы, которая необходима вирусу для воспроизведения своей РНК. Это ингредиент продемонстрировал высокую эффективность и минимальные побочные эффекты. В сравнении с другими медикаментами, его усвояемость в организме значительно выше.
После перорального применения средство всасывается в желудочно-кишечном тракте, обладая хорошей биологической доступностью, достигающей 92 %. Активный компонент связывается с белками на уровне до 62 %. Основные метаболические процессы проходят в печени, а период выведения составляет около 27 часов.
Выводится из организма через пищеварительную систему до восьмидесяти процентов в виде неактивных метаболитов. Четырнадцать процентов выводятся через мочевую систему. Фармакологические исследования у детей до восемнадцати лет не проводились. У пациентов пенсионного возраста до семидесяти пяти лет не оказал терапевтического влияние на организм.
Несмотря на то, что у молодых пациентов иммунный ответ оказался сопоставимым, не выявлено значительных различий между пациентами различных полов и рас. Для больных с заболеваниями почек требуется постоянный мониторинг анализов, так как фармакологические свойства препарата Совальди несколько отличаются от таковых у здоровых людей.
Совальди показан для лечения гепатита С. Лекарства назначаются для терапии у взрослых пациентов в качестве комбинированного лечения с другими лекарствами. Совальди назначается для лечения острого и хронического течения.
Противопоказания
Применение Совальди противопоказано для лиц, у которых имеется повышенная чувствительность к активному веществу, для женщин в период беременности и лактации, а также для детей до восемнадцати лет. Пациентам с нарушениями функции почек не следует назначать это лекарство. Совальди показан для пациентов с первого, четвертого, пятого и шестого генотипами вируса, а также тем, кто применяет иные препараты для лечения вирусной инфекции.
Совальди предназначен для перорального применения. Рекомендуется принимать одну таблетку по четыреста миллиграммов единовременно во время еды, запивая необходимым количеством воды. Таблетку нельзя разламывать, нужно глотать целиком, поскольку она воздействует на организм постепенно.
Длительность терапии Совальди устанавливает лечащий врач, он производит контроль состояние пациента на протяжении курса терапии. Если пациент пропустил прием таблетки, то ему необходимо принять как только вспомнил о пропуске. Принимается одна доза, двойную дозу принимать нельзя. Пропуск должен составлять не больше восемнадцати часов.
Если прошло более восемнадцати часов с момента пропуска дозы, дальнейший прием нужно возобновить согласно назначенной схеме. Если рвота произошла в течение двух часов после приема, следует принять еще одну таблетку. Если же рвота произошла позже двух часов, дополнительный прием не требуется.
Всасывание и распределение действующего компонента Совальди происходит в течении двух часов. Препарат используется в комбинированном лечении, поэтому интервал между приемами разных лекарств составляет шестьдесят минут.
Daclavizar as an Integral Component of Pangenotypic Regimens for the Treatment of Chronic Viral Hepatitis C Using Drugs with Direct Antiviral Action
Данный обзор посвящен вопросам лечения хронического вирусного гепатита С. Применение препарата с прямым противовирусным действием — ингибитора NS5A РНК-зависимой РНК-полимеразы Даклавизара в сочетании с софосбувиром у пациентов с хроническим вирусным гепатитом С имеет высокий уровень эффективности, безопасности и переносимости.
Даклавизар является значимой частью пангенотипных схем терапии хронического вирусного гепатита С с использованием препаратов с направленным противовирусным действием.
1 Кафедра госпитальной терапии № 2 Лечебного факультета ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» МЗ РФ, Москва 2 ФГАУ «НМИЦ «Лечебно-реабилитационный центр» МЗ РФ, Москва
Обзор рассматривает насущную проблему — лечение хронического вирусного гепатита С. Комбинированная терапия с применением препарата Даклавизара, ингибитора NS5A-комплекса РНК-зависимой РНК-полимеразы, в сочетании с софосбувиром, гарантирует высокую эффективность, безопасность и хорошую переносимость у больных хроническим гепатитом С.
Хронический вирусный гепатит С (ВГС) — одна из самых распространенных хронических инфекций в мире, которая связана с тяжелыми медико-социальными последствиями в виде формирования цирроза и рака печени, что определяет большую нагрузку на общественные системы здравоохранения во всем мире. По данным Всемирной организации здравоохранения, на сегодняшний день насчитывается более 280 млн. человек, инфицированных вирусом гепатита С и имеющих признаки хронической инфекции [1, 2]. В этой связи в последнее время во всем мире отмечается значительное возрастание необходимости в трансплантации печени у пациентов, страдающих ВГС [3]. Также существенно повышаются финансовые и организационные затраты общественных систем здравоохранения, связанные с раком печени, что обусловлено необходимостью дорого-
Лечебное дело 4.2020-
имеет дело с проблемами химиотерапевтического лечения, которое часто оказывается с малой эффективностью и требует трансплантации печени [4].
Кроме того, коинфекция ВГС, например, у пациентов с ВИЧ-инфекцией, а также с другими хроническими инфекциями, вызванными вирусами гепатита В и D, существенно ускоряет темпы прогрессирова-ния фиброза печени со значительно более быстрым формированием цирроза печени и гепатоцеллюлярной карциномы [4, 5]. У пациентов с онкологическими заболеваниями наличие хронического ВГС может негативно влиять на проводимое химиоте-рапевтическое лечение, значительно повышая шансы развития гепатотоксичности. Статистические данные по распространенности хронического ВГС свидетельствуют о том, что суммарные антитела к вирусу методом иммуноферментного анализа выявляются в среднем у 2,5—3,4% населения Российской Федерации, из них у 80% име-
Этап 2 ИФН + рибавирин
Этап 3 ПЕГ-ИФН + + рибавирин
ПЕГ-ИФН + рибавирин + ингибиторы протеаз
Пангенотипные препараты с прямым противовирусным действием
Продолжительность терапии, нед
До 72 24-48 12-48 12-24 8-12-24
Рис. 1. Эволюция лечения хронического ВГС. ИФН — интерферон, ПЕГ-ИФН — пегилирован-ный интерферон, УВО — устойчивый вирусологический ответ.
Наличие активного процесса обуславливает положительные результаты по РНК вируса в сыворотке. Таким образом, простые вычисления показывают, что общее количество пациентов с хроническим ВГС составляет приблизительно 5 миллионов [6, 7].
Понимание серьезности бремени ВГС для системы общественного здравоохранения обоснованно требовало разработки высокоэффективных анти-вирусных схем, над созданием которых работа ведется чуть более 20 лет (рис. 1).
Начальные подходы к лечению хронического ВГС включали в себя использование коротких интерферонов (ИФН) (преимущественно ИФН-а), затем их комбинации с гуаназиновым нуклеотидным аналогом -рибавирином, затем — комбинации пеги-лированных ИФН-а всё с тем же рибавири-ном, что и было на протяжении нескольких лет неким «золотым стандартом» лечения данного заболевания. Целью такого лечения было достижение устойчивого вирусологического ответа (УВО), что означало стойкое отсутствие РНК вируса гепатита С в биологических средах организма как минимум на 6-м месяце после завершения терапии. Дальнейшее наблюдение за пациентами и детальное изучение тонкой биологии вируса позволили констатировать, что между дефинициями «УВО» и «излечение» можно по-
Установить равенство между возможностью полного выздоровления от хронической инфекции.
Согласитесь, что в нынешней практике врача подобных случаев крайне мало, если не сказать прямо — нет вообще. Достигался данный результат весьма трудно, что было связано как с особенностями пациента (избыточная масса тела, перегрузка железом, наличие сопутствующих неалкогольной жировой болезни печени, сахарного диабета, различные варианты полиморфизма гена ^В28), так и с особенностями вируса и его кинетики в организме пациента (генотип вируса, уровень виремии на старте лечения, показатель виремии на 4-й и 12-й неделях терапии). Особенно сложно приходилось и врачу, и пациенту, когда развивались хорошо известные побочные эффекты, связанные с использованием ИФН (депрессия, алопеция, нейтропения, дисфункция щитовидной железы) и рибавири-на (кожный зуд, непродуктивный упорный кашель, гемолитическая анемия).
Несмотря на колоссальные усилия со стороны врачей и пациентов, результаты такого лечени мог ли бы быть разочаровывающими. Частота достижения устойчивого вирусологического ответа (УВО) у больных с хроническим гепатитом С не превышала 50%, у остальных выявлялись случаи отсутствия реакции на лечение, так называемый «прорыв» в процессе терапии или рецидив инфекции в краткосрочные сроки после завершения довольно сложного и частично малорезультативного курса лечения. Длительность такой наименее успешной терапии колебалась от 24 недель до 72 недель, что объясняло необходимость внедрения новых, более эффективных и безопасных подходов к лечению ВГС [1, 2, 8].
Детальное изучение тонкой биологии вируса позволило выявить ряд ключевых ферментов репликации, которые стали мишенями при разработке эффективных лекарственных препаратов. Это К83/КБ4 — сериновый протеазный комплекс и К85Л/КБ5В — комплекс РНК-зависимой РНК-полимеразы (рис. 2). Данные ферменты были воссозданы в формате 3D-модели, где были четко идентифицированы их активные центры, что в дальнейшем позволило создать весьма эффективные лекарственные препараты, блокирующие эти центры по типу «ключ—замочная скважина» [8].
Клиническая практика инфекционистов и гастроэнтерологов пополнилась новыми классами препаратов, название которых дает четкое понимание их механизма действия:
— «. превир» — ингибитор протеазы комплекса К83/КБ4 (паритапревир, гразопревир и т.д.);
Би Лечебное дело 4.2020-
— «.свир» — ингибитор КБ5Л-комплекса РНК-зависимой РНК-полимеразы (даклатаcвир, велпатасвир и т.д.);
— «. бувир» — ингибитор КБ5В-комп-лекса РНК-зависимой РНК-полимеразы (софосбувир, дасабувир и т.д.).
Эти классы препаратов быстро и эффективно блокируют репликацию вируса гепатита С, а возможность их перорального комбинирования обеспечивала достижение УВО без необходимости применения ИФН и рибавирина у большинства пациентов [8, 9]. Следует отметить хорошую переносимость этих схем, а также короткий курс лечения, что способствует успешной интеграции этих методов в программу государственной гарантии бесплатного медицинского обслуживания граждан Российской Федерации за счет средств обязательного медицинского страхования [10]. Более того, дальнейшие исследования разнообразных комбинаций пероральных противовирусных препаратов с различными механизмами действия сформировали универсальные или пангенотипные схемы, позволяющие достигать высоких результатов УВО (более 90—95%) при лечении разных генотипов вируса гепатита C. Такие схемы терапии больше не требуют на начальном этапе определения генотипа вируса или уровня виремии, полиморфизмов гена ^В28 и т.д. [8, 9].
DCV + SOF ± RBV LED/SOF ± RBV VEL/SOF
(п = 602) (п = 182) (п = 53)
Рис. 3. Сопоставимая эффективность комбинации даклатасвир + софосбувир и других панге-нотипных пероральных схем лечения ВГС у пациентов (n = 837), получивших хотя бы одну дозу препарата и прошедших оценку по итогам 12 нед терапии (УВО определялся для популяции пациентов mlTT). DCV — даклатасвир, LED — ледипасвир, RBV — рибавирин, SOF — софосбувир, VEL — велпатасвир.
Особое внимание следует уделить оценке результативности противовирусного лечения ВГС именно схемам даклатасвир + софосбувир благодаря их доступности, пангенотипности и отличной переносимости, а Высокой вероятности достижения УВО у данной категории пациентов. Стоит отметить, что в Российской Федерации в 2020 году был зарегистрирован собственный препарат даклатасвир под торговым названием Даклавизар (владелец регистрационного удостоверения АО «Фармстандарт»). Эффективность этой комбинации в рамках пангенотипного лечения хронического ВГС была подтверждена результатами крупных многоцентровых клинических исследований и, что особенно важно, данными практической работы.
Так, в одном из исследований оценивалась эффективность использования комбинации даклатасвир + софосбувир у 1021 пациента (у 506 человек имел место генотип 1 вируса, у 16 — генотип 2, у 314 — генотип 3, у 13 — генотип 4, у 166 — генотип 6). В 12 клинических центрах Таиланда 767 пациентов
В группу комбинированной терапии даклатасвир + софосбувир вошли 197 пациентов, получавших ледипасвир/софосбувир, и 57 — велпатасвир/софосбувир с рибавирином или без него. Частота достижения УВО на 12-й неделе для пациентов независимо от генотипа вируса (популяция mITT) сложилась следующим образом: у группы даклатасвир + софосбувир (n = 602) — 98,0%, у ледипасвир/софосбувир (n = 182) — 97,9%, у велпатасвир/софосбувир (n = 53) — 96,5%. Таким образом, комбинация даклатасвир + софосбувир демонстрирует сравнимые результаты с другими пероральными противовирусными схемами лечения ВГС, с практически одинаковым профилем безопасности (рис. 3) [11].
Большой интерес представляет обзор литературы, включивший в себя публикации из баз данных MEDLINE, Embase, CENTRAL и иные релевантные публикации рандомизированных и нерандомизированных клинических исследований, а также обсервационных исследований, в которых оценивались эффективность и безопасность различных пероральных противовирусных схем лечения ВГС на основе софосбувира. В общей сложности
Лечебное дело Ш0 6
было проанализировано 238 публикаций, которые включают 142 исследования. Комбинация даклатасвир + софосбувир продемонстрировала сопоставимую эффективность и безопасность с другими пероральными схемами для лечения хронического ВГС, средняя эффективность этой комбинации в общей популяции составила 94%, наивысший уровень УВО отмечен у пациентов с генотипом 1 вируса без признаков цирроза (95,6%) и у инфицированных генотипом 2 вируса (100,0%) [12].
Еще в одном исследовании также оценивалась эффективность различных пер-оральных схем противовирусной терапии ВГС, в том числе с использованием комбинации даклатасвир + софосбувир. В исследование было включено в общей сложности 328 пациентов из США, Великобритании, Франции, Германии, Испании и Италии. Были продемонстрированы высокие эффективность и безопасность комбинации даклатасвир + софосбувир, сопоставимые с таковыми других пероральных комбинаций (софосбувир/ледипасвир, софосбу-вир/велпатасвир). Частота УВО в общей группе пациентов составила более 94% с хорошей переносимост ью лечения на всем его протяжении [13].
Что говорят представленные данные? Даклатасвир (Даклавизар) является безусловно важным компонентом пангенотипных схем для перорального лечения хронического ВГС препаратами с прямым противовирусным механизмом. Данный препарат характеризуется высокой безопасностью и хорошей переносимостью, что позволяет использовать его в разных категориях пациентов как без назначения рибавирина, так и в сочетании с ним.
четании с последним. Назначение комбинации Даклавизара с софосбувиром должно осуществляться в строгом соответствии с инструкцией к препарату. При этом следует подчеркнуть, что при назначении подобной комбинации лекарственных препаратов на этапе лечения уже не требуется проведение оценки динамики виремии в реперных точках, как это было ранее при использовании, например, препаратов ИФН.
Эффективность комбинированного использования Даклавизара с софосбувиром в контексте системы общественного здравоохранения, а также отсутствие влияния на результаты лечения таких факторов, как ожирение, полиморфизм гена ЛБ28, избыток железа и инсулинорезистентность, делает данное лекарственное сочетание крайне удобным. Каждый случай лечения имеет свой уникальный путь, что вписывается в общепринятые стандарты организации медицинской помощи и модели финансирования в базовой программе обязательного медицинского страхования. На текущий момент, в рамках этой структуры оказания медицинских услуг гражданам Российской Федерации, были разработаны клинико-статистические группы для лечения пациентов с хроническим ВГС, что значительно увеличивает доступность и качество такой терапии в рамках государственной программы гарантии бесплатной медицинской помощи гражданам Российской Федерации [10, 14].
Вы можете ознакомиться со списком литературы на нашем сайте www.atmosphere-ph.ru
Daclavizar as an Integral Component of Pangenotypic Regimens for the Treatment of Chronic Viral Hepatitis C Using Drugs with Direct Antiviral Action I.G. Nikitin
Данный обзор посвящен вопросу лечения хронического вирусного гепатита С. Применение препарата с прямым вирусоактивным механизмом действия — ингибитора NS5A и РНК-зависимой РНК-полимеразы Даклацивира в сочетании с софосбувиром у пациентов с хроническим гепатитом С демонстрирует высокую эффективность, безопасность и хорошую переносимость.
Key words: hepatitis C, liver cirrhosis, daclatasvir, antiviral treatment.
Совальди
Таблетки капсульной формы, покрытые желтой пленочной оболочкой, имеют гравировку “GSI” с одной стороны и «7977» с другой.
Фармакодинамика
Механизм действия
Софосбувир является гепатитным ингибитором РНК-зависимой РНК-полимеразы NS5B, которая необходима для вирусной репликации. Он представляет собой нуклеотидное пролекарство, которое после внутреклеточного метаболизма превращается в активный аналог уридинтрифосфата (GS-461203). Используя полимеразу NS5B, GS-461203 может интегрироваться в синтезируемую цепь РНК вируса гепатита С, выступая как цепеобрывающий агент. Этот активный метаболит софосбувира (GS-461203) подавляет активность полимераз генотипов 1b, 2a, 3a и 4a в концентрациях, которые приводят к 50 % ингибированию (IC50) в диапазоне от 0,7 до 2,6 мкмоль. GS-461203 не влияет на полимеразы ДНК и РНК человека, а также на полимеразу митохондриальной РНК.
Противовирусная активность
В исследованиях с использованием репликонов ВГС значения эффективной концентрации (EC50) софосбувира против полноразмерных репликонов генотипов 1а, 1b, 2а, 3а и 4а составили 0,04, 0,11, 0,05, 0,05 и 0,04 мкмоль, соответственно, а значения EC50 софосбувира против химерных репликонов генотипа 1b, несущих последовательности NS5B из генотипов 2b, 5а или 6а, составили 0,014–0,015 мкмоль. Среднее значение ЕС50± SD софосбувира в отношении химерных репликонов, несущих последовательности NS5B из клинических изолятов, составило 0,068 ± 0,024 мкмоль для генотипа 1а; 0,11 ± 0,029 мкмоль для генотипа 1b; 0,035 ± 0,018 мкмоль для генотипа 2 и 0,085 ± 0,034 мкмоль для генотипа 3а. Противовирусная активность софосбувира in vitro в отношении менее часто встречаемых генотипов 4, 5 и 6 была аналогичной активности в отношении генотипов 1, 2 и 3.
Не обнаружено значимого изменения активности софосбувира при наличии 40 % человеческой сыворотки.
Резистентность
В клеточных культурах
Пониженная чувствительность к софосбувиру ассоциировалась с первичной мутацией S282Т в NS5B всех исследованных генотипов репликонов ВГС (1b, 2а, 2b, 3а, 4а, 5а и 6а). Сайт-направленный мутагенез подтвердил, что мутация S282Т в репликонах 8 генотипов ответственна за снижение в 2–18 раз чувствительности к софосбувиру и уменьшение способности вируса к репликации на 89–99 % по сравнению с соответствующим вирусом дикого типа. Рекомбинантная NS5B полимераза из генотипов 1b, 2а, 3а и 4а, экспрессирующая замену S282Т, продемонстрировала пониженную чувствительность к активному метаболиту софосбувира (GS-461203) по сравнению с аналогичными полимеразами дикого типа.
В клинических испытаниях
Из 991 пациента, принимавшего софосбувир в рамках клинических испытаний, 226 были отобраны для анализа на наличие резистентности из-за вирусологической неэффективности или отказа от препарата при уровнях РНК вируса гепатита С >1 000 МЕ/мл. Изменение последовательностей в NS5B по сравнению с исходными данными исследовали у 225 пациентов, при этом глубокое секвенирование (с порогом 1 %) было проведено у 221 из них. Мутация S282T, связанная с устойчивостью к софосбувиру, не была найдена ни у одного из этих пациентов, что подтверждено как глубоким, так и популяционным секвенированием. У единственного участника, получавшего монотерапию Совальди, была обнаружена мутация S282T. Эта мутация вернулась к исходному аллелю в течение следующих 8 недель и не была найдена через 12 недель после прекращения терапии с использованием глубокого секвенирования.
Также были выявлены две мутации NS5B, L159F и V321A, в образцах нескольких пациентов с генотипом 3 в стадии рецидива после завершения лечения в рамках клинических испытаний. Эти мутации не влияли на фенотипическую чувствительность к софосбувиру или рибавирину у изолятов с мутациями. Кроме того, в ходе терапии у пациента с частичным ответом были зафиксированы мутации S282R и L320F методом глубокого секвенирования. Значимость этих находок в клинической практике пока не установлена.
Влияние исходных полиморфизмов ВГС на эффективность лечения
При анализе влияния исходных полиморфизмов на исход терапии не наблюдалось статистически значимой связи между наличием любого исходного варианта NS5B ВГС (мутация S282Т) и эффективностью лечения.
Перекрёстная резистентность
Репликоны вируса гепатита С, экспрессирующие мутацию S282T, были полностью чувствительны к другим классам противовирусных препаратов для лечения гепатита C. Софосбувир сохранял активность в отношении вирусов с мутациями L159F и L320F, связанными с устойчивостью к другим нуклеозидным ингибиторам. Препарат также полностью сохраняет активность в отношении мутаций, которые приводят к резистентности к другим противовирусным средствам с другими механизмами действия, включая ненуклеозидные ингибиторы полимеразы NS5B, ингибиторы NS3 протеазы и ингибиторы NS5A.
Эффективность софосбувира оценивалась в пяти исследованиях с участием 1568 пациентов в возрасте от 19 до 77 лет с хроническим гепатитом С (ХГС), вызванным вирусами генотипов от 1 до 6.
Дети
Эффективность и безопасность препарата Совальди для детей и подростков младше 18 лет не была установлена. Данные об этом отсутствуют.
Фармакокинетика
Софосбувир — это нуклеотидное пролекарство, которое активно метаболизируется. Формирующийся в гепатоцитах активный метаболит не выявляется в крови. Большая часть (>90 %) метаболита, GS-331007, не имеет активности и образуется через последовательные и параллельные пути метаболизма активного компонента.
Всасывание
После приёма внутрь софосбувир быстро всасывался, а его максимальная концентрация (Сmax ) в плазме крови достигалась через 0,5–2 ч вне зависимости от величины принятой дозы. Сmax неактивного метаболита (GS-331007) в плазме крови достигалась через 2–4 ч после приёма препарата. По результатам популяционного анализа фармакокинетических данных у пациентов с генотипами 1–6 ВГС, значения площади под кривой «концентрация-время» (АUС0–24) софосбувира и неактивного метаболита (GS-331007) в равновесном состоянии была равна 1010 нг × час/мл и 7200 нг × час/мл, соответственно. По сравнению со здоровыми добровольцами, АUС0–24 софосбувира и неактивного метаболита (GS-331007) у пациентов с ХГС была на 57 % выше и на 39 % ниже, соответственно.
Распределение
Софосбувир не является субстратом для печеночных транспортных белков, таких как переносчик органических анионов 1B1 или 1B3. Неактивный метаболит (GS-331007) не является ни субстратом, ни ингибитором органов почечных канальцев, включая переносчики органических анионов 1 или 3, переносчики органических катионов 2, белки многофункциональной лекарственной резистентности (MRP2), гликопротеин Р, белок резистентности рака молочной железы (BCRP) или переносчики MATE1.
Софосбувир примерно на 85 % связывается с белками плазмы крови человека (данные ex vivo), и связывание не зависит от концентрации препарата в диапазоне 1–20 мкг/мл. Неактивный метаболит (GS-331007) в минимальной степени связывается с белками плазмы крови человека. После однократного приёма 400 мг [ 14 С]-софосбувира здоровыми добровольцами, соотношение радиоактивности 14 С в крови/плазме составляет приблизительно 0,7.
Метаболизм
Софосбувир претерпевает интенсивный метаболизм в печени, образуя активный нуклеозидный (уридиновый) аналог трифосфата (GS-461203). Процесс активации включает гидролиз карбоксилэстеразами 1 и A, и расщепление фосфорамидата нуклеотид-связывающим белком 1 с гистидиновыми триадами (HINT1), за которым следует фосфорилирование через биосинтез пиримидинового нуклеотида. Дефосфорилирование приводит к образованию неактивного нуклеозида (>90 %), который не может быть полностью рефосфорилирован и не оказывает действия против HCV in vitro. Софосбувир и неактивный метаболит (GS-331007) не подлежат метаболизму с участием UGT1A1 или изоферментов CYP3A4, CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6.
После однократного перорального приема 400 мг [14 С]-софосбувира, системная экспозиция софосбувира составила около 4 %, а неактивного метаболита (GS-331007) — более 90 % от общей системной экспозиции препарата (сумма AUC софосбувира и его метаболитов с учетом молекулярной массы).
Выведение
После однократного перорального приёма 400 мг [ 14 С]-софосбувира среднее общее выведение радиоактивной дозы составило более 92 %, при этом приблизительно 80 %, 14 % и 2,5 % выводилось почками, кишечником и лёгкими, соответственно. Большая часть дозы софосбувира, выводимая почками, представляла неактивный метаболит (GS-331007) (78 %), тогда как 3,5 % выводилось в виде софосбувира. Эти данные показывают, что почечный клиренс является основным путём выведения неактивного метаболита (GS-331007) с преимущественной активной секрецией. Средний период полувыведения софосбувира и неактивного метаболита (GS-331007) составляет 0,4 часа и 27 часов, соответственно.
Установлено, что при натощак приеме софосбувира в дозах от 200 мг до 400 мг AUC софосбувира и неактивного метаболита (GS-331007) практически пропорциональна дозе.
Фармакокинетика у особых групп пациентов
Дети
Параметры фармакокинетики софосбувира и неактивного метаболита (GS-331007) у детей не установлены.
Пожилые пациенты
В рамках исследований с пациентами, страдающими хроническим гепатитом С, в возрасте от 19 до 75 лет не было отмечено клинически значительного влияния возраста на уровень экспозиции софосбувира и неактивного метаболита (GS-331007). Частота ответа среди пациентов старше 65 лет была сопоставима с таковой у молодых участников.
Пол и раса
Отсутствуют клинически значимые различия в фармакокинетике софосбувира и его неактивного метаболита в зависимости от пола и расы.
Почечная недостаточность
По сравнению с пациентами с нормальной функцией почек (клиренс креатинина, КК, >80 мл/мин), не инфицированными ВГС, при почечной недостаточности лёгкой, средней и тяжёлой степени тяжести, AUC0–inf софосбувира была выше, соответственно, на 61 %, 107 % и 171 %, a AUC0–inf неактивного метаболита (GS-331007) была выше на 55 %, 88 % и
У пациентов с хронической почечной недостаточностью (ХПН) AUC0–inf софосбувира была на 28 % выше, если софосбувир принимали за 1 час до гемодиализа, и на 60 % выше, если препарат принимали через 1 час после гемодиализа по сравнению с пациентами с нормальной функцией почек. Точные показатели AUC0-inf неактивного метаболита (GS-331007) у пациентов с ХПН установить не удалось, однако есть данные о десятикратном и двадцатикратном увеличении его экспозиции у таких пациентов.
Основной неактивный метаболит (GS-331007) может быть эффективно удалён с помощью гемодиализа (клиренс составляет около 53 %). После 4-часового сеанса гемодиализа выводится примерно 18 % от принятой дозы препарата. У пациентов с почечной недостаточностью лёгкой или средней степенью тяжести не требуется изменения дозы препарата. Безопасность применения софосбувира не оценивали у пациентов с почечной недостаточностью тяжёлой степени тяжести и пациентов с терминальной стадией почечной недостаточности (см. разделы «Способ применения и дозы» и «Противопоказания»).
Печёночная недостаточность
Пациенты с печеночной недостаточностью средней и тяжелой степени показали на 126 % и 143 % выше AUC0–inf софосбувира соответственно по сравнению с лицами с нормальной функцией печени. AUC0–inf неактивного метаболита (GS-331007) также была выше — на 18 % и 9 %. Исследования показывают, что цирроз не оказывал статистически значимого влияния на экспозицию софосбувира и его метаболита. Рекомендуется не изменять дозировку софосбувира у пациентов с легкой, умеренной и тяжелой печеночной недостаточностью.
Взаимосвязь фармакокинетики/ фармакодинамики
Доказано, что эффективность лечения, в частности, быстрый вирусологический ответ, коррелирует с уровнем экспозиции софосбувира и его неактивного метаболита (GS-331007). Тем не менее, ни один из этих показателей не является основным суррогатным маркером для оценки эффективности (СВO12) при использовании терапевтической дозы в 400 мг.
Sovaldi: история самого продаваемого препарата за всю историю фармотрасли

Вирус гепатита С, носителем которого являются 130-150 млн человек, приводит к трансплантации печени или смерти больного. В 2013 году на рынок вышел первый препарат, излечивающий эту смертельную инфекцию, но по-прежнему остается много открытых вопросов.
Певица Натали Коул, дочь Нэта Кинга Коула, ушла из жизни в возрасте 65 лет, страдая от сердечной недостаточности. Долгие годы она боролась с вирусом гепатита С, который, как считают врачи, стал причиной ее смерти. Болея бессимптомно на протяжении более 25 лет, Натали узнала о своем диагнозе только после 60 лет и открыто заявила о своих проблемах со здоровьем в 2008 году.
Стандартом лечения в это время была комбинация интерферона с рибавирином — противовирусных препаратов, неспецифичных к вирусу гепатита С. Натали признавалась, что лечение хуже самой болезни. «Вирус гепатита С повлиял на мою работу и на мою жизнь. После начала лечения я плохо себя чувствовала, все время уставала, и меня постоянно тошнило. Я за короткое время потеряла более 10 кг», — делилась она. Действительно, побочных эффектов такой терапии не сосчитать, включая постоянные усталость и слабость, гриппоподобные симптомы, проблемы с пищеварением и со сном. Могут появиться сильная аллергическая реакция и аутоиммунные заболевания, серьезные нарушения работы сердечно-сосудистой (включая инсульт) и пищеварительной систем, щитовидной железы, легких и печени вплоть до печеночной недостаточности и смерти пациента.
Лечение не оказало ожидаемого эффекта: менее половины пациентов достигают полного выздоровления, в том числе и Натали. Она перенесла трансплантацию почки, вызванную воздействием препаратов, которая в конечном итоге продлила ее жизнь всего на несколько лет — певица скончалась 31 декабря 2015 года.
По данным статистики, гепатит С является ведущей причиной заболеваний печени. По оценкам, в мире хронической формой этого вируса заражены от 130 до 150 миллионов людей. Каждый год приблизительно 700 тысяч пациентов умирают от заболеваний, связанных с вирусом. При этом только каждый четвертый инфицированный осведомлен о своей болезни.
Вирус распространяется через кровь: при переливании, через общий шприц, во время нанесения татуировки, при половом акте, контакте с кровью носителя. Заразиться можно даже при посещении стоматолога, салонов маникюра и парикмахерских, поскольку инструменты могут быть недобросовестно стерилизованы. У большинства пациентов с хронической формой заболевания развивается цирроз или рак печени. Эти осложнения влекут за собой в лучшем случае трансплантацию печени, в худшем — летальный исход.
Революция в лечении гепатита С произошла в конце 2013 года, когда на рынке появились новые противовирусные препараты прямого действия, эффективность которых может достигать 100%. Эти лекарственные средства гораздо лучше переносятся пациентами, а курс лечения занимает всего 8–12 недель.
Первым препаратом этой группы стал препарат Sovaldi (софосбувир) от Gilead, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в декабре 2013 года. Gilead приобрела в 2011 году небольшую компанию Pharmasset Inc. — разработчика Sovaldi — за $11,2 млрд. Pharmasset была приобретена с премией к рынку в 89%, при этом за четыре года до сделки она с трудом разместилась на бирже по оценке менее $200 млн. Рынок встретил такое приобретение Gilead неоднозначно: риски были крайне высоки, перспективы рынка — неочевидны, а уплаченная сумма — огромна.
На рискованный шаг решилась и одна из крупнейших фармацевтических компаний — Bristol-Myers Squibb. В 2012 году она приобрела компанию Inhibitex за $2,5 миллиарда, предложив премию в 163% к рыночной стоимости. Inhibitex работала над созданием лекарства, аналогичного Sovaldi. Однако в том же году Bristol-Myers Squibb была вынуждена списать практически всю сумму покупки, так как клинические испытания были остановлены из-за проблем с безопасностью: у одного из участников исследования возникли серьезные побочные эффекты, и он, к сожалению, скончался от осложнений лечения.
В отличие от старой неспецифической терапии, прямодействующие противовирусные препараты блокируют работу вирусных белков и размножение вируса в организме. Sovaldi стал первым препаратом, который полностью ингибирует работу ключевого вирусного белка (NS5B), необходимого для репликации вируса.
Данный белок отсутствует в организме человека, поэтому считается, что лечение с помощью Sovaldi редко вызывает побочные эффекты. Однако вопросы по безопасности препаратов прямого действия и, в частности, Sovaldi, неожиданно стали появляться спустя три года после одобрения терапии. Несколько крупных организаций, в том числе FDA и Институт безопасных методов лечения (Institute for Safe Medication Practices), предупреждают о том, что эта группа лекарств может вызывать печеночную недостаточность из-за обострения гепатита В и даже смерть пациента. Компания Gilead пока что отрицает наличие причинно-следственной связи между приемом софосбувира и вышеназванными побочными эффектами.
Невзирая на высокую цену, с препаратом Sovaldi связано множество примеров успешного лечения. Американская актриса и фотомодель Памела Андерсон в 2002 году объявила о своей болезни — гепатите С. Она заявила, что вирус попал в ее организм во время татуажа с использованием нестерильной иглы. В ноябре 2015 года стало известно, что после 16 лет мучительного лечения, Памела смогла полностью излечиться от гепатита С благодаря Sovaldi.
На запуске Sovaldi стал самым успешным препаратом по объему продаж за всю историю фармотрасли. Продажи Gilead препаратов Sovaldi, Harvoni и Epclusa (последние два препарата — комбинации с Sovaldi) составили в дебютном полном 2014 году более $10 млрд, а в 2015 году — более $19 млрд. В 2015 году доля Gilead на рынке гепатита С составила более 90%. Sovaldi одобрен в 65 странах мира, им воспользовались уже более 1 млн пациентов. В дальнейшем по мере излечения пациентов, усиления конкуренции и снижении цен прогнозируется сокращение продаж.
Sovaldi устраивает практически всех пациентов, кроме одного значительного фактора — цены. Одна таблетка (400 мг) стоит в США $1,000. Таким образом, полный 12-недельный курс лечения обойдется в $84 тысячи, что делает его недоступным для большинства больных. Между тем, себестоимость производства активной фармацевтической субстанции на весь курс составляет лишь около $100.
Такая высокая цена привела к беспрецедентным мерам. Национальная служба здравоохранения Великобритании задержала включение Sovaldi в список лицензированных лекарств, оплачиваемых государством, из-за его высокой стоимости, несмотря на признание высокой экономической эффективности софосбувира Национальным институтом здравоохранения и качества медицинской помощи. Генеральный прокурор штата Массачусетс пригрозила компании Gilead судебными исками из-за завышенной цены жизненно важного препарата, которая значительно нагружает государственные финансовые программы. По всему миру продолжаются судебные разбирательства, направленные на оспаривание патентов Gilead и развитие дженерикового производства.
Несмотря на это, Джон Мартин (John C. Martin), бывший председатель правления компании Gilead, стал миллиардером, среди прочего, благодаря Sovaldi. По оценке Forbes, его текущее состояние превышает $1 млрд. Основной доход Джону принесли опционы за счет роста стоимости компании — за 20 лет его руководства (он присоединился к компании в 1990 году в качестве главы НИОКР) цена акции Gilead выросла в 100 раз. Однако в марте прошлого года 64-летнему Джону Мартину пришлось покинуть свой пост, в том числе в связи с волной возмущения общественности в отношении цены Sovaldi.
Следует ли оправдывать цену Sovaldi? С точки зрения государственного управления, стоимость новой терапии объясняется не только ее клинической эффективностью и преимуществами по сравнению с существующими методами лечения, но и снижением общих расходов системы здравоохранения. До появления Sovaldi препараты, стоимостью $50 тысяч, могли предоставить лечение лишь одному из трех носителей вируса, что означало стоимость излечения около $150 тысяч. Sovaldi же, при цене в $84 тысячи, обеспечивает излечение практически 100% пациентов, и, следовательно, стоимость лечения оказывается значительно ниже.
Кроме того, лечение последствий гепатита С обходится дороже, чем лечение самого заболевания. Так, например, в США только на операцию по пересадке печени тратится около $200 тыс. К этому нужно добавить непрямые расходы — средства, которые человек не смог заработать из-за госпитализации, потери работы вследствие острой или хронической инфекции и преждевременной смерти. Такие косвенные финансовые потери даже выше, чем прямые. Не стоит также забывать о том, что носители вируса способствуют появлению новых случаев заражения и распространению заболевания.
Успех Sovaldi кардинально изменил расстановку сил на рынке лечения гепатита С. Компания Merck, которая на протяжении многих лет была одним из лидеров, в одночасье потеряла свои позиции с выходом Sovaldi на рынок. Компания принялась искать возможности приобретения высокотехнологичного препарата с аналогичным механизмом действия. В 2014 году Merck приобрела компанию Idenix за $3,8 миллиарда, предложив практически беспрецедентную премию к рыночной стоимости — около 250% для активов с капитализацией более $1 миллиарда.
Idenix была основана со-основателем Pharmasset (разработчика Sovaldi) — предприимчивым Жаном-Пьером Соммадосси. Механизм действия препарата Idenix аналогичен тому, что у Sovaldi. Жан-Пьер также является членом консультативного совета инвестиционного фонда ATEM Capital (основанного Антоном Гопкой — Forbes) и сейчас возглавляет свою третью компанию, которая разрабатывает препарат нового поколения против гепатита С. Интересно, что среди крупных акционеров Idenix была и другая фармацевтическая компания Novartis с долей в 22%, которая впоследствии получила от Merck компенсацию в размере более $800 миллионов за сделку.
Пока препарат Idenix находится в разработке, Merck продолжает активно конкурировать с Gilead. В декабре прошлого года Merck смогла оспорить часть патентной защиты Sovaldi, и суд обязал Gilead выплатить более $2,5 млрд в качестве компенсации с прежних продаж Sovaldi — это крупнейший объем выплат в патентном споре за всю историю. Кроме того, Merck стала агрессивно снижать цены на свои препараты против гепатита С: так, ее препарат, одобренный в начале 2016 года, стоит номинально до 40% дешевле, чем Sovaldi. Таким образом, ожидается, что эффективная конкуренция на рынке постепенно обеспечит снижение цены препаратов прямого действия.
По различным оценкам, в России от 3,6 до 6 миллионов людей являются носителями вируса гепатита С, в основном это лица в возрасте 30-40 лет. В 2015 году только около 15 тысяч из них получили какое-либо лечение. Доступ к новым эффективным препаратам имеют менее 1% выявленных зараженных. Стоимость курса лечения специализированными препаратами превышает 800 тысяч рублей, и большинство пациентов вынуждены оплачивать его самостоятельно.
Как считают эксперты, в ближайшее время ожидается волна пациентов с циррозом и раком печени. С сопутствующей эпидемией ВИЧ ситуация выглядит критичной (см. также статью «Связанные одной лентой» на «Биомолекуле»). Однако федеральной программы по борьбе с гепатитом в РФ нет.
Гепатит С имеет все шансы стать первой вирусной инфекцией, которую можно будет искоренить без вакцины. Цена успеха Sovaldi заключается в десятилетиях исследований вирусной биологии, проведенных тысячами ученых, десятках неудавшихся клинических программ, миллиардах долларов, которые были потрачены, и миллионах спасенных жизней по всему миру.
Данный текст опубликован в рамках специального проекта Forbes и научно-популярного портала «Биомолекула», посвященного достижениям молекулярной биологии и их внедрению в биотехнологии и медицину. Расширенная версия статьи доступна на сайте «Биомолекулы».