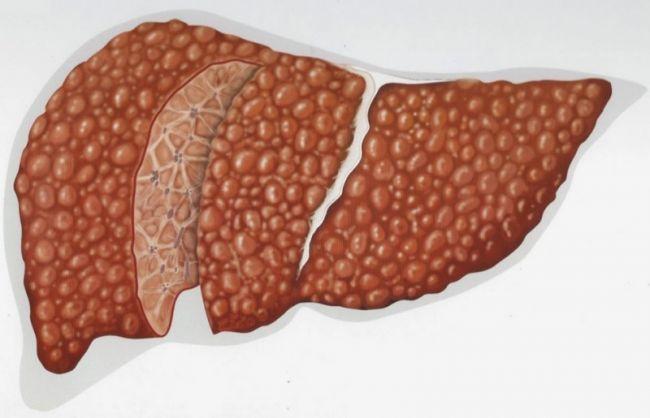
После удаления желчного пузыря в области прокола может возникнуть образование кругов, что часто связано с отечностью и реакцией организма на хирургическое вмешательство. Это нормальное явление, которое обычно проходит самостоятельно в течение нескольких дней.
Тем не менее, если круги сопровождаются сильной болью, покраснением или выделениями, важно обратиться к врачу для исключения возможных осложнений, таких как инфекция или гематома. В большинстве случаев забота о себе и наблюдение за местом прокола помогут избежать проблем.
- После удаления желчного пузыря могут возникать круги вокруг прокола.
- Круги могут быть связаны с воспалением, отеком или заживлением ткани.
- Образование кругов не всегда является признаком осложнения, но требует наблюдения.
- Важно следить за состоянием прокола и сообщать врачу о любых необычных симптомах.
- Рекомендации по уходу за швами могут помочь предотвратить осложнения.
Желчнокаменная болезнь (ЖКБ) на сегодняшний день является одним из наиболее часто встречающихся заболеваний. Она занимает третье место среди заболеваний, уступая только сердечно-сосудистым патологиям и диабету. В развитых странах от ЖКБ страдает от 10 до 15% взрослого населения. В России каждый год к врачам по поводу данного заболевания обращаются около 1 миллиона человек.
В стране количество операций холецистэктомии каждый год занимает второе место, уступая только аппендэктомиям. В крупных городах, таких как Москва, на 100 000 жителей проводится примерно 7000 подобных операций в год.
С каждым годом все большее количество этих операций выполняется с применением малоинвазивных методик, таких как хирургия с малой травматичностью или эндовидеохирургия. Из-за растущего числа операций на ЖКБ увеличивается и количество пациентов, страдающих от различных послеоперационных осложнений. По различным данным, от 1 до 2 из 10 пациентов, перенесших холецистэктомию, продолжают ощущать дискомфорт в области кишечника, боль и нарушения пищеварения, а также повторные болевые эпизоды. Медики используют термин «постхолецистэктомический синдром» (ПХЭС) для обозначения таких симптомов. Возвращение боли наблюдается в половине случаев в течение первого года после операции, но может появляться и позже.
Терминология и классификация
Термин ПХЭС был введен в 30-е годы ХХ века американскими хирургами и используется до настоящего времени. Он объединяет большую группу патологических состояний в гепатопанкреатодуоденальной зоне, которые существовали до холецистэктомии, сопутствовали холециститу, осложнили его или возникли после операции. Во многом это объединение связано с тем, что при повторном обращении больного с жалобами после перенесенной холецистэктомии редко удается правильно поставить диагноз без многокомпонентного, комплексного обследования. При этом обобщающий термин ПХЭС используется в качестве временного диагноза в процессе обследования больного в соответствии с дифференциально-диагностическим алгоритмом. В дальнейшем, в большинстве случаев, удается выяснить причину жалоб больного и более общий термин уступает место конкретному диагнозу.
После удаления желчного пузыря, пациенты могут заметить образование кругов или отеков вокруг места прокола. Как эксперт в области медицины, я могу утверждать, что это явление обычно связано с индивидуальной реакцией организма на операцию. Операция, как и любая хирургическая манипуляция, вызывает стресс для тканей и может приводить к различным изменениями в области вмешательства.
Круги или отеки часто возникают из-за накопления жидкости в области прокола. Это может быть следствием воспалительного процесса или нормальным этапом заживления. Важно понимать, что организм реагирует на вмешательство, и в большинстве случаев такие симптомы являются временными и проходят со временем. Однако, если отеки нарастают или возникают дополнительные симптомы, важно своевременно обратиться к врачу для оценки состояния.
Кроме того, образование кругов может быть связано с неправильным уходом за раной или инфекцией. Пациентам рекомендовано следовать указаниям врача по уходу за послеоперационной областью, чтобы минимизировать риск осложнений. Как правило, при соблюдении всех рекомендаций заживление проходит без каких-либо проблем, и все изменения в области прокола нормализуются в течение нескольких недель.
- функциональные нарушения,
- органические патологии.
В свою очередь, к органическим относят:
- поражения желчных путей;
- патологии пищеварительной системы, включая заболевания печени, поджелудочной железы и двенадцатиперстной кишки;
- болезни и состояния, не связанные с гастроинтестинальными расстройствами.
Однако сам постхолецистэктомический синдром встречается довольно редко и является следствием адаптационных изменений в системе желчеотведения, которые происходят после удаления желчного пузыря — органа, служащего резервуаром для хранения и сгущения желчи. В большинстве случаев проблема заключается в других заболеваниях, которые проявляют симптомы, схожие с ПХЭС.
По результатам современных гастроэнтерологических исследований, у половины пациентов основная причина жалоб кроется в функциональных расстройствах пищеварительного процесса. Органические нарушения обнаруживаются у одной трети обращающихся, но лишь в 1,5% случаев эти проблемы действительно являются результатом операции, и всего 0,5% пациентов с диагнозом ПХЭС нуждаются в повторной операции. Возникновение ПХЭС тоже поднимает вопросы юридической и страховой ответственности, что усложняет ситуацию. В связи с этим, среди разнообразных диагнозов, связанных с ПХЭС, выделяют две основные группы, в зависимости от взаимосвязи с предыдущей операцией:
- заболевания, не связанные с перенесенной процедурой, зачастую являющиеся следствием диагностических ошибок;
- патологии, непосредственно вызванные хирургическим вмешательством — операционные ошибки.
К диагностическим ошибкам относят:
- Необнаруженные до операции сопутствующие заболевания или болезни, симптоматика которых схожа с желчнокаменной болезнью. Это случаи, когда диагностика была ошибочной, и хотя желчный пузырь, заполненный камнями, был удален, истинный источник боли остался невыявленным.
- Патологии других органов, находящихся в аналогичной области, не имеющие отношения к операции, но по проявлениям напоминающие рецидив желчнокаменной болезни и усиливающиеся после вмешательства.
К операционным ошибкам относят
- Остаточный холедохолитиаз (камни, оставшиеся в желчных протоках).
- Папиллостеноз (сужение мест впадения желчных протоков в кишечник).
- Опухоли желчных протоков и головки поджелудочной железы.
- Повреждения желчных протоков, возникшие во время операции.
Большинство подобных ошибок связано с недостаточным дооперационным обследованием и несоответствием объема хирургического вмешательства реальному состоянию основного заболевания. Явно это проявляется при лечении сложных форм желчнокаменной болезни, когда производится лишь стандартная холецистэктомия, а не более комплексные варианты операции. Здесь можно говорить о ошибке, связанной с «неполным диагнозом — недостаточным объемом операции».
Наиболее опасной группой являются прямые ятрогенные хирургические осложнения. Симптомы ПХЭС у пациентов с различными расстройствами живота могут проявляться в разное время после холецистэктомии и иногда могут быть продолжением тех же нарушений, что имели место до операции и не исчезли после нее. Разнообразие симптоматики и различное время её проявления зависят от конкретных причин, вызывающих эти расстройства.
Похожие темы научных работ по клинической медицине , автор научной работы — Горский В. А., Фаллер А. П., Ованесян Э. Р., Агапов М. А
Профилактика формирования грыж после лапароскопической холецистэктомииПричины формирования грыж после лапароскопической холецистэктомииГрыжи пупочного порта: превентивная герниопластикаПрименение синтетических материалов в профилактике и лечении послеоперационных грыж малых доступовЛапароскопическая холецистэктомия из двух доступов — опыт отечественных авторовi Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
i Устали от рекламы? Вы можете отключить баннеры.
Causes of the formation of hernias after laparoscopic cholecystectomy
Исследователи провели анализ случаев послеоперационных грыж у 32 пациентов. Рассмотрены общие и локальные причины. Предложенные технические подходы, использованные для устранения локальных причин, позволили снизить частоту послеоперационных грыж с 1,9% до 0,5%.
ОШИБКИ И ОПАСНОСТИ В ХИРУРГИИ
В.А. Горский, А.П. Фаллер, Э.Р. Ованесян, М.А. Агапов
ПРИЧИНЫ ФОРМИРОВАНИЯ ГРЫЖ
ПОСЛЕ ЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТЭКТОМИИ
Кафедра хирургии (зав. — проф. Б.К. Шуркалин) медико-биологического факультета Российского государственного медицинского университета, 55-я Городская клиническая больница (главврач — проф. О.Н. Румянцев), Москва
Введение. Вопрос о приоритете лапароскопической холецистэктомии (ЛХЭ) в хирургическом лечении желчнокаменной болезни сегодня уже не вызывает сомнений.
Широкое внедрение ЛХЭ вначале вызвало огромный интерес хирургов, обусловленный положительными первоначальными результатами вмешательства, особенно уменьшением травмы брюшной стенки и ускоренной реабилитацией пациентов. Тем не менее, первоначальный оптимизм был омрачен такими негативными «сопутствующими» проблемами, как увеличение числа крупных и мелких интраоперационных повреждений внепеченочных желчных протоков [5-8]. Кроме традиционной «ахиллесовой пяты» ЛХЭ — травмы общего желчного протока, вскоре появилась еще одна послеоперационная проблема, возможно и менее опасная для жизни, но тем не менее, серьезно снижающая качество жизни — образование послеоперационных грыж.
Как в отечественной, так и зарубежной литературе этот вопрос освещен недостаточно. Существуют лишь единичные публикации, в которых указывается на развитие вентральных грыж после лапароскопических вмешательств [1, 3, 10]. Поэтому считаем необходимым обратить внимание на причины возникновения данного осложнения.
Материал и методы. Проведенные клинические исследования основываться на опыте хирургического лечения 32 пациентов с послеоперационными вентральными грыжами, возникшими после ЛХЭ в период с 2002 по 2006 годы. У 17 пациентов ЛХЭ производилась в нашей клинике, у 15 — в других учреждениях Москвы. За указанный период в нашей клинике было проведено 1506 ЛХЭ, что дало 1,1% случаев формирования грыж после операции.
Возраст пациентов с послеоперационными грыжами варьировался от 25 до 79 лет, среди них только один мужчина (3,1%) и 31 женщина (96,8%).
Ретроспективный анализ историй болезни пациентов, перенесших ЛХЭ, позволил определить временной фактор образования послеоперационных вентральных грыж. У 23 (67,6%) больных грыжи сформировались в первые 6 мес после операции, у 10 (29,4%) пациентов — в течение первого года, у 1 (2,9%) больного — в течение 4 лет. Грыжи локализовались в проекции послеоперационного рубца и околопупочной области справа.
Перед операцией пациенты с вентральными грыжами проходили обследование для выявления сопутствующих заболеваний (ЭКГ-мониторинг, исследование функций внешнего дыхания и прочее), а также их коррекцию.
Все операции проводились планово. Два пациента попали с ущемленными грыжами, однако в процессе транспортировки они самостоятельно вправились.
Методом выбора анестезии был эндотрахеальный наркоз. Разрез производили в проекции грыжевого образования, с обязательным иссечением пупочного кольца. Из многочисленных способов устранения послеоперационных вентральных грыж отдавали предпочтение аллопластике с применением полипропиленовых сетчатых имплантатов «Prolene mesh» фирмы «Ethicon» (Великобритания) — 23 (71,9%) больных.
Операции выполнялись с использованием подшивания имплантата нитью «Prolen» 2/0 в варианте надапоневротического расположения. У 9 (28,1%) пациентов была выполнена мышечно-апоневротическая аутопластика с образованием дупликатуры по Сапежко, что применялось при наличии дефектов апоневроза размером до 3 см и качественной ткани в области грыжевых ворот, что позволяло избежать натяжения тканей и нарушений их питания.
Послеоперационный период протекал без осложнений, повторных случаев грыж и летальных исходов не было зарегистрировано.
Результаты и обсуждение. Мы полагаем, что условия возникновения грыж после ЛХЭ зависят от двух групп факторов — общих и местных.
Общие причины: 1) генетическая детерминированная слабость соединительной ткани; 2) избыточная масса тела; 3) пожилой и старческий возраст пациентов ввиду наличия у них дряблости тканей и снижения интенсивности процессов регенерации; 4) сопутствующая соматическая
Общая патология (сахарный диабет, сердечно-сосудистые и легочные заболевания, кахексия, авитаминоз и т.д.); 5) повышение внутрибрюшного давления как в раннем послеоперационном периоде (парез кишечника, кашель, рвота, задержка мочеиспускания, психоз любого происхождения), так и в позднем послеоперационном периоде (несоблюдение режима физических нагрузок, беременность).
Локальные причины: 1) использование трансректального доступа для вставки первого троакара; 2) увеличение разреза при удалении желчного пузыря; 3) неадекватное зашивание дефекта передней брюшной стенки; 4) осложнения операционной раны — серома, гематома, нагноение, эвентрация.
По нашему глубокому убеждению, основной этиологической причиной появления любой грыжи (а не только послеоперационной) следует считать заложенную генетически детерминированную слабость соединительной ткани, которая является предрасполагающим фактором ее возникновения. А все остальные причины возникновения грыж следует относить к факторам производящим или провоцирующим. Хотя понятно, что в этиологии появления послеоперационных грыж значительно больше местных производящих факторов, чем при обычных приобретенных грыжах.
При ретроспективном анализе историй болезни выяснилось, что у 20 (62,5%) пациентов наблюдалась предрасположенность к грыжеобразованию из-за функциональной недостаточности соединительной ткани. Об этом можно было судить по наличию у больных: варикозной болезни — 12 случаев, геморроя — 4, дивертикулеза толстой кишки — 1. Трое из пациентов ранее перенесли операции по поводу грыж других локализаций.
Кроме того, стоит иметь в виду и другие общие факторы, осложняющие не только заживление раны, но в некоторой степени затрудняющие выполнение оперативного вмешательства, такие как избыточный вес пациента.
Ожирение считается одним из наиболее значимых контролируемых факторов образования послеоперационных грыж — 23 (71,8%) пациента имели ожирение Ш-1У степени и выраженную подкожную жировую клетчатку передней брюшной стенки толщиной более 4-5 см. У данной группы больных, безусловно, следует стремиться к предоперационному снижению массы тела. Однако это было невозможно по объективной причине — все они были оперированы по экстренным или срочным показаниям по поводу деструктивного холецистита.
Пожилой возраст пациентов представляет собой еще один рискованный аспект, так как с возрастом наблюдается потеря упругости тканей, ослабление их механических характеристик и замедление процессов восстановления. Более половины пациентов с вентральными грыжами (56,2%) оказались старше 60 лет. У 26 (81,2%) из них были диагностированы одно или несколько сопутствующих заболеваний, например, сахарный диабет (у 4 больных), а также болезни сердечно-сосудистой (у 17) и дыхательной систем.
Следовательно, указанные выше факторы, способствующие образованию грыж, особенно у пациентов с острым холециститом, практически невозможно изменить. Проблематично предотвратить их возникновение, но важно учитывать их при выборе подхода к хирургическому вмешательству [2].
Местные факторы формирования грыж в большей степени контролируемы. Для введения 1-го троакара и удаления желчного пузыря при ЛХЭ мы используем два типа разреза — справа от пупка и выше пупка. Белая линия живота на уровне и выше пупка представляет собой мем-бранозную часть передней брюшной стенки, ее самое тонкое и потенциально слабое место [9].
Также существуют данные в научной литературе, указывающие на риск образования послеоперационных вентральных грыж, когда доступ осуществляется выше уровня пупка [3, 10]. Такой подход считается целесообразным для пациентов с долихоморфной конституцией, и точка оптимального вставления эндоскопа определяется вычитанием длины желчного пузыря, установленной при предоперационном ультразвуковом исследовании, из рабочей длины лапароскопа. Результирующую величину располагают на белой линии живота пациента от проекции шейки пузыря на переднюю брюшную стенку. В этом случае оптика будет находиться на максимальном расстоянии от зоны операции, что позволит надежно контролировать все этапы вмешательства [4]. На данный момент отдаленные итоги применения этой методики не были проанализированы.
Для большинства пациентов мы осуществляем введение первого троакара и удаления желчного пузыря через разрез, расположенный справа от пупка, который фактически является трансректальным. В ситуациях, когда пузырь удаляется через 20-миллиметровый троакар и при отсутствии послеоперационного нагноения, мы не наблюдали случаев формирования грыж. Однако расширение доступа при извлечении увеличенного желчного пузыря, особенно при остром холецистите, или пузыря с крупными камнями, либо переполненного множеством мелких конкрементов, осложняет местное восстановление.
Грыжи после лапароскопической холецистэктомии
Крупные камни желчного пузыря, по нашему мнению, создают дополнительные трудности для хирурга. Это может привести к необходимости увеличивать размер разреза для извлечения желчного пузыря, что в свою очередь может повредить ткани и привести к образованию грыж. В нашем исследовании конкременты диаметром более 3 см были зафиксированы у 9 пациентов, от 2 до 3 см — у 8, от 1 до 2 см — у 7, а от 0,5 до 1 см — у 5. У 3 больных были обнаружены множественные мелкие камни.
Методика ушивания ран при лапароскопической холецистэктомии также имеет критическое значение в контексте предотвращения формирования послеоперационных грыж. При закрытии мест введения 5- и 10-миллиметровых троакаров мы сшиваем лишь кожу. Ни в одном случае при этом не было зафиксировано гранулем. Как при использовании 20-миллиметрового троакара, так и при расширении раны, околопупочная область сшивается в два слоя: брюшина и апоневроз вместе, и кожа отдельно. В настоящее время мы применяем более эффективный способ ушивания ран в этой зоне.
По нашему мнению, основным недостатком трансректального доступа являются трудности, испытываемые хирургом при ушивании влагалища прямой мышцы живота. Благоприятные условия для возникновения грыжи создаются, когда ушивается только передний листок влагалища прямой мышцы живота и не захватывается задний.
Это особенно актуально для пациентов с избыточным весом, когда хирург не может точно контролировать глубину введения иглы с небольшим размером разреза. Поэтому для уверенного закрытия раневого дефекта прямой мышцы живота мы стали использовать иглы «Endo Close». На финальной стадии операции перед даже легким упаковкой раны троакар задерживается.
Это необходимо для поддержания герметичности в брюшной полости и упрощения выполнения интраабдоминального этапа ушивания. На расстоянии 1 см от края разреза апоневроза иглу с прикрепленной лигатурой проводим через все слои брюшной стенки. Затем с помощью манипулятора мы высвобождаем нить и оставляем в брюшной полости, после чего извлекаем иглу.
Далее мы прошиваем «холостой» иглой с противоположной стороны. Нить захватывается манипулятором и вместе с иглой вытягивается наружу. После наложения швов все тампоны удаляются, и швы постепенно затягиваются. В завершение ушиваем кожу отдельно.
В качестве шовного материала для закрытия троакарной раны нами используется викрил № 4. Число накладываемых швов индивидуально и зависит от длины рассеченного апоневроза. В среднем для герметичного ушивания необходимо 3-4 шва. Данная методика проста в выполнении, обеспечивает надежное ушивание всех слоев раны и дает возможность визуального контроля за объемом захватываемых в шов тканей. Методика применяется нами в течение последнего года. За
В данный момент случаи образования грыж у пациентов, перенесших лапароскопическую холецистэктомию, не наблюдаются.
Инфекция раны в большинстве случаев вызывается интраоперационным контаминацией брюшной стенки. Частота подобных осложнений после лапароскопической холецистэктомии, согласно литературным данным, составляет 0,44-0,47% [11, 12]. реальное количество нагноений ран может быть значительно выше, так как они могут проявляться после выписки граждан из стационара. В исследуемом материале нагноение послеоперационных ран стало причиной возникновения грыж у 7 пациентов, а серомы — у 6. Основной причиной осложнений, по нашему мнению, является инфицирование раны во время извлечения разрушенного желчного пузыря из брюшной полости без контейнера.
К сожалению, приходится признать, что даже при самом строгом соблюдении асептики и техники операции не удается полностью избежать возникновения раневой инфекции. Действенным способом сокращения числа раневых инфекционных осложнений является превентивная антибактериальная терапия во время операции, использование контейнеров для извлечения желчного пузыря, а Введение в раневые каналы раствора диоксидина. Строгое соблюдение указанных мер позволило нам существенно сократить число нагноений операционных ран на протяжении последних 3 лет, снизив частоту этого осложнения с 1,9 до 0,5%.
Таким образом, можно подвести итог. 1. Формирование грыж представляет собой значительную проблему в процессе послеоперационного восстановления у пациентов, перенесших лапароскопическую холецистэктомию.
2. Данное осложнение снижает восприятие ценности лапароскопического доступа в глазах пациентов. Поэтому важно обратить внимание на контролируемые факторы, способствующие образованию послеоперационных грыж с целью их предотвращения.
1. Абдуллаев Э.Г., Феденко В.В., Бабышин В.В. и др. Послеоперационные вентральные грыжи после лапароскопических вмешательств // Вестн. эндоскопии.—2001.—№ 4.—С. 2225.
2. Антропова Н.В., Шулутко А.М. Тактика лечения хронических послеоперационных грыж с учетом индекса рисков // Хирургия.—1996.—№ 6.—С. 45-48.
3. Баулина Е.А., Николашин В.А., Баулин А.А. Влияние места извлечения желчного пузыря на риск возникновения грыж после эндохирургии // Эндоскоп. хир.—2007.—№ 1.—С. 12-13.
4. Бондарев А.А., Мясников А.Д. Методологические принципы оценки и выбора оптимального доступа в эндохирургии // Там же.—С. 16.
5. Галлингер Ю.И. Интраоперационные осложнения при лапароскопической холецистэктомии, их предупреждение и лече-
ния // Рос. журн. гастроэнтерол. гепатол.—1994.—№ 4.— С. 77-81.
6. Гальперин Э.И. Повреждения желчных протоков вследствие холецистэктомии // Хирургия.—1998.—№ 1.—С. 5-7.
7. Емельянов С.И. Эндоскопическая хирургия осложненных форм желчнокаменной болезни // Материалы IV конференции хирургов-гепатологов России и стран СНГ «Современные проблемы хирургической гепатологии».—Тула, 1996.—С. 4344.
8. Карпенкова В.И. Лапароскопическая холецистэктомия — осложнения и их предотвращение // Анн. Науч. центра хирур-гии.—1997.—№ 6.—С. 14-18.
9. Кошев В.И., Петров Е.С., Иванова В.Д. Функциональная защита белой линии живота и возникновение грыж // Материалы конференции «Актуальные вопросы герниологии».—М., 2002.—С. 72-73.
10. Оскретов В.И., Литвинова О.М., Скрипицина О.В. Основные причины возникновения троакарных грыж после видеолапароскопической холецистэктомии // Эндоскоп. хир.—2007.— № 1.—С. 65-66.
11. Сажин В.П., Климов Д.Е., Сажин А.В., Наумов И.А. Особенности лечения пациентов с крупными послеоперационными и рецидивирующими вентральными грыжами // Герниология.—2004.— № 1.—С. 11-15.
12. Gislason H., Gronbech J.E., Soreide O. Взрыв живота и послеоперационные грыжи после крупных операций на органах пищеварительной системы — сравнение методик закрытия // Eur. J. Surg.—1995.—Vol. 5.— P. 349-354.
Материал поступил в редакцию 10.10.2007 г.
V.A.Gorsky, A.P.Faller, E.R.Ovanesyan, M.A.Agapov
ПРИЧИНЫ ФОРМИРОВАНИЯ ГРЫЖ ПОСЛЕ ЛАПАРОСКОПИЧЕСКОЙ ХОЛЕЦИСТЭКТОМИИ
Авторы провели анализ случаев возникновения послеоперационных грыж у 32 пациентов. Рассмотрены как общие, так и локальные причины. Предложенные технические решения, направленные на устранение локальных причин, смогли снизить частоту послеоперационных грыж с 1,9% до 0,5%.
Классификация
Наиболее обоснованной признана классификация Chevrel J.P., Rath А.М., представленная в 1999 году. Согласно этой классификации, послеоперационные грыжи разделяют по нескольким параметрам:
- Локализация: срединная, боковая, комбинированная. Выпячивания после холецистэктомии обычно имеют комбинированное или срединное расположение.
- Частота рецидивов: фиксируется один и более случаев. Рецидивы регистраются через обозначение «R» в медицинской документации, и, в зависимости от частоты рецидива, рядом с латинской буквой указывается определенное число. Например, если грыжа возникла в том же месте в второй раз, это фиксируется как R2.
- Ширина грыжевых ворот: менее 4 см (W1), 4-10 см (W2), 10-15 см (W3), более 15 см (W4).
Также обсуждаются вопросы возможности вправления выпячиваний и количество камер (однокамерные и многокамерные).
Фото
Далее будет представлено, как выглядит послеоперационная грыжа после холецистэктомии.

Вентральная грыжа после срединной лапаротомии


Лечение постхолицистэктомического синдрома
Поскольку ПХЭС не является самостоятельной болезнью, методы лечения синдрома всегда определяются его причинами. Неправильный подход к лечению постхолицистэктомического синдрома может не только усугубить проблемы, но и увеличить выраженность неприятных симптомов.
Основные принципы лечения ПХЭС включают два ключевых аспекта:
- сбор анамнестических данных — врач осторожно изучает предыдущие медицинские документы, уделяя особое внимание предоперационной диагностике и исследованию проведенной операции;
- устранение причин синдрома;
- профилактику и лечение возможных осложнений.
Лечение основывается, в основном, на:
- диетической терапии;
- медикаментозной терапии;
- хирургическом вмешательстве (при необходимости) 7 .
Вместе с комплексным лечением эти меры могут уменьшить выраженность симптомов ПХЭС 8 .
Применение ферментных препаратов при постхолицистэктомическом синдроме
В некоторых случаях ПХЭС может сопровождаться проблемами в работе пищеварительной системы. Это связано с тем, что сигнал для выработки желчи и ферментов поджелудочной железы возникает в момент приема пищи. Если сигнал отсутствует или нарушен, это влияет на все последующие процессы. В итоге пища не обрабатывается должным образом, и организм недополучает необходимые вещества. Это может негативно сказываться на общем состоянии человека и проявляться в виде тяжести после еды, дискомфорта, вздутия или диареи.
Для нормализации процессов пищеварения созданы ферментные препараты, которые обеспечивают поступление ферментов в организм извне, тем самым компенсируя их недостаток. Одним из наиболее известных средств в этой категории является Креон ®.
Препарат выпускается в форме капсул, содержащих сотни мельчайших частиц под названием Креон минимикросферы ®12 . Они не превышают по размеру признанной границы в 2-х мм 9,10,12 . Маленький размер частиц позволяет препарату Креон ® воссоздавать процесс пищеварения, каким он был задуман в организме, и тем самым справляться с неприятными симптомами. Минимальной стартовой дозировкой считается 25 000 единиц 10 .

Ключевым аспектом терапии при ПХЭС является назначение ферментотерапии. Часто это обусловлено нарушением работы поджелудочной железы, что ведет к недостаточной выработке ферментов. В результате могут возникнуть проблемы с пищеварением, проявляющиеся в виде дискомфорта, болей в области живота, ощущения тяжести, газообразования и диареи. Нехватка ферментов негативно сказывается на усвоении необходимых питательных веществ, что приводит к дефициту витаминов и минералов.
Креон ® представляет собой современный ферментный препарат, способный восполнять нехватку собственных ферментов, что улучшает усвоение пищи и способствует нормализации пищеварительных процессов. Дополнительную информацию о препарате можно найти здесь.
Источники
Надо ли принимать лекарства и соблюдать диету после удаления желчного пузыря?

Учитывая, что состав желчи может быть «литогенным», то есть предрасположенным к образованию камней, профилактическое лечение препаратами желчных кислот по рекомендации врача является важной мерой для предотвращения камнеобразования в желчевыводящих путях.
Стоит отметить, что традиционные диеты, такие как стол номер 5, в настоящее время утратили свою актуальность. Важно акцентировать внимание на качестве питания. Все ограничения в рационе следует обсуждать с вашим лечащим врачом, так как они часто имеют индивидуальный характер.
Современные рекомендации не содержат убедительных статистических данных о полезности соблюдения низкожировой диеты. Основной акцент стоит делать на снижении потребления добавленного сахара, а также заменить белый хлеб на цельнозерновой. В целом, рекомендуется следовать принципам «здоровой тарелки».
Правило «здоровой тарелки»
Около половины каждого приема пищи должно составлять ассортимент овощей и фруктов. Овощи стоит употреблять в вареном, тушеном или свежем виде, в то время как картофель рекомендуется ограничить из-за его способности повышать уровень сахара в крови. Фрукты можно есть как свежими, так и приготовленными.
В рацион следует включать цельнозерновые продукты — это занимает около ¼ тарелки. В качестве таковых выступают цельная пшеница, ячмень, пшено, киноа, овсянка, гречка, неочищенный рис и изделия из них, включая макароны из цельной пшеницы.
Белку отводится ¼ тарелки. Нежирная говядина, индейка, курица, рыба, фасоль, орехи – здоровые и разнообразные источники белка. Их можно добавить в салат, и они хорошо сочетаются с овощами.
Полезные растительные масла, такие как оливковое, кукурузное, подсолнечное и арахисовое, рекомендуется употреблять в умеренных количествах.
В качестве напитков лучше выбирать воду, кофе или чай без сахара или с минимальным его содержанием.
Подобнее о том, как жить без желчного пузыря, и как меняется работа желчевыделительной системы после холецистэктомии, мы рассказали в видео:
Надо ли «чистить» желчные протоки при отсутствии желчного?
Не существует необходимости в какой-либо «чистке» желчных протоков; достаточно профилактического приема препаратов желчных кислот по назначению лечащего врача.

Прежде всего, рекомендуется обратиться к врачу для осмотра у специалиста, а также сдать анализы крови на клинические и биохимические параметры.
Для получения инструментальных данных потребуется пройти УЗИ органов брюшной полости, рентгенологическом исследовании пищевода, желудка и двенадцатиперстной кишки, провести видеогастродуоденоскопии и МР-холангиографию.
Если Вас беспокоят боли в животе, расстройство стула или другие неприятные симптомы, появившиеся с течением времени после удаления желчного пузыря, вы можете получить консультацию в специализированном «Гастроэнтерологическом центре Эксперт». Также у нас разработана комплексная программа «Реабилитация после удаления желчного пузыря», в которую включены необходимые для контроля ЖКТ после удаления желчного пузыря обследования и прием гастроэнтеролога.

Автор статьи: гастроэнтеролог Ибрагимова Зейнаб Магомедовна.
Для получения информации о времени работы специалиста вы можете обратиться на страницу врача.