Аллопуринол следует принимать строго по назначению врача, обычно один раз в день, после еды, запивая достаточным количеством воды. Это помогает обеспечить лучший эффект и минимизировать возможные побочные реакции со стороны желудочно-кишечного тракта.
Для достижения нормализации уровня мочевой кислоты необходимо регулярно контролировать её содержание в крови и при необходимости корректировать дозировку препарата. Важно также поддерживать адекватный уровень гидратации и придерживаться диеты с низким содержанием пуринов.
- Аллопуринол принимается по назначению врача для контроля уровня мочевой кислоты.
- Важно начинать с низкой дозы и постепенно увеличивать её для предотвращения обострений.
- Принимать препарат следует ежедневно, желательно в одно и то же время.
- Обильное питье (не менее 2 литров в день) помогает предотвратить образование камней в почках.
- Регулярно контролируйте уровень мочевой кислоты с помощью анализов.
- Обсуждайте все побочные эффекты или изменения состояния со своим врачом.
Составляющие компоненты: микрокристаллическая целлюлоза (МКЦ-101 Премиум) – 54,0 мг; кукурузный крахмал – 25,0 мг; натриевая соль карбоксиметилкрахмала – 10,0 мг; повидон-К25 – 8,0 мг; коллоидный диоксид кремния – 1,0 мг; стеарат магния – 2,0 мг.
Содержимое в одной таблетке 300 мг:
Основной компонент: аллопуринол – 300,0 мг.
Вспомогательные вещества: целлюлоза микрокристаллическая (МКЦ-101 Премиум) — 162,0 мг, крахмал кукурузный — 75,0 мг, карбоксиметилкрахмал натрия — 30,0 мг, повидон-К25 — 24,0 мг, кремния диоксид коллоидный — 3,0 мг, магния стеарат — 6,0 мг.
Описание
Таблетки круглой формы, плоскоцилиндрические, имеют белый или слегка желтоватый оттенок, оснащены риской и фаской.
Фармакодинамика
Аллопуринол является структурным аналогом гипоксантина. Аллопуринол, а также его основной активный метаболит — оксипуринол, подавляют ксантиноксидазу — фермент, обеспечивающий преобразование гипоксантина в ксантин, и ксантина в мочевую кислоту. Аллопуринол уменьшает концентрацию мочевой кислоты в сыворотке крови и моче, таким образом он предотвращает отложение кристаллов мочевой кислоты в тканях и/или способствует их растворению. Помимо подавления катаболизма пуринов у некоторых (но не у всех) пациентов с гиперурикемией, большое количество ксантина и гипоксантина становится доступно для повторного образования пуриновых оснований, что приводит к угнетению биосинтеза пуринов de novo по механизму обратной связи, что опосредовано угнетением фермента гипоксантин-гуанин фосфорибозил-трансферазы. Другие метаболиты аллопуринола — аллопуринол-рибозид и оксипуринол-7 рибозид.
Фармакокинетика
Всасывание
Аллопуринол проявляет активность при пероральном приеме. Препарат быстро абсорбируется из верхних отделов gastrointestinal tract. По данным фармакокинетических исследований, его уровень в крови обнаруживается уже через 30–60 минут после приема.
Биодоступность аллопуринола находится в диапазоне от 67 % до 90 %. Обычно максимальная концентрация в плазме крови достигается примерно через 1,5 часа после перорального приема. Далее уровень препарата быстро уменьшается. Через 6 часов после приема в плазме остаются лишь минимальные следы. Максимальная концентрация активного метаболита — оксипуринола, как правило, фиксируется через 3–5 часов после приема аллопуринола. Концентрация оксипуринола в крови уменьшается гораздо медленнее.
Аллопуринол – это препарат, который я рекомендую принимать строго по указанию врача. Обычно его назначают для снижения уровня мочевой кислоты в организме, особенно при подагре. Важно следовать назначенной дозировке, чтобы избежать неприятных побочных эффектов и достичь оптимальных результатов в контроле уровня мочевой кислоты.
Я всегда обращаю внимание на то, что аллопуринол следует принимать регулярно, не пропуская дозы. Наиболее распространённый режим – это принимать его один раз в день, желательно в одно и то же время, это помогает поддерживать стабильный уровень препарата в крови. Бывает, что в начале лечения уровня мочевой кислоты может временно повышаться. Это нормально, и поэтому важно продолжать принимать лекарство и следить за его уровнем под контролем врача.
Кроме того, я советую не забывать о сопутствующих мерах. Важно следить за диетой и избегать продуктов, богатых пуринами, таких как красное мясо, Alcohol и некоторые виды рыбы. Употребление достаточного количества воды также критично, так как это помогает выводить мочевую кислоту из организма. В комбинации с аллопуринолом такие изменения в образе жизни способствуют более эффективному контролю уровня мочевой кислоты и общему улучшению состояния здоровья.
Распределение
Аллопуринол практически не связывается с плазменными белками, поэтому изменения в уровне связывания с белками не должны существенно влиять на выведение препарата. Объем распределения аллопуринола составляет около 1,6 л/кг, что свидетельствует о его хорошем поглощении тканями. Хотя содержание аллопуринола в различных органах человека не изучалось, можно предположить, что он и его метаболит оксипуринол накапливаются в печени и стенке кишечника, где активность ксантиноксидазы наиболее высокая.
Биотрансформация
Аллопуринол метаболизируется под воздействием ксантиноксидазы и альдегидоксидазы с образованием оксипуринола. Оксипуринол также угнетает активность ксантиноксидазы, однако его ингибирующее действие не столь значительно, как у аллопуринола, зато он обладает намного большей продолжительностью полувыведения. Таким образом, после приема суточной дозы аллопуринола происходит стойкое угнетение действия ксантиноксидазы в течение суток.
Выведение
Приблизительно 20 % принятого per os аллопуринола выводится через кишечник в неизменённом виде. Около 10 % суточной дозы экскретируются клубочковым аппаратом почки в виде неизменённого аллопуринола. Ещё 70 % суточной дозы аллопуринола выводится с мочой в форме оксипуринола.
Оксипуринол выводится через почки в неизмененном виде, но из-за повторной абсорбции в канальцах его полувыведение достаточно продолжительно. Полувыведение аллопуринола составляет 1–2 часа, в то время как для оксипуринола этот период колеблется от 13 до 30 часов. Такие заметные различия, вероятно, обусловлены вариациями в исследовательских методах и/или клиренсе креатинина у респондентов.
Пациенты с нарушением функции почек
У больных с нарушениями почечной функции выведение аллопуринола и оксипуринола может значительно замедляться, что приводит к повышению их концентрации в крови при длительной терапии. У пациентов с недостаточностью функции почек и клиренсом креатинина 10–20 мл/мин, после продолжительного применения аллопуринола в дозе 300 мг в сутки, уровень оксипуринола в плазме мог достигать около 30 мг/л. Такая концентрация может наблюдаться у людей с нормальной функцией почек при терапии оксипуринолом в дозе 600 мг в сутки. Соответственно, пациентам с нарушениями почек следует снижать дозу аллопуринола.
Пожилые пациенты
У пожилых пациентов значительные изменения фармакокинетических свойств аллопуринола маловероятны. Исключение составляют пациенты с сопутствующей патологией почек (см. раздел «Пациенты с нарушенной функцией почек»).
АЛЛОПУРИНОЛ АВЕКСИМА
вспомогательные компоненты: микрокристаллическая целлюлоза 101; кукурузный крахмал; натриевая соль карбоксиметилкрахмала; повидон К-25; стеарат магния; коллоидный диоксид кремния.
Аллопуринол является структурным аналогом гипоксантина. Аллопуринол, а также его основной активный метаболит — оксипуринол, ингибируют ксантиноксидазу — фермент, обеспечивающий преобразование гипоксантина в ксантин, и ксантина в мочевую кислоту. Аллопуринол уменьшает концентрацию мочевой кислоты как в сыворотке крови, так и в моче. Тем самым он предотвращает отложение кристаллов мочевой кислоты в тканях и/или способствует их растворению. Помимо подавления катаболизма пуринов у некоторых (но не у всех) пациентов с гиперурикемией, большое количество ксантина и гипоксантина становится доступно для повторного образования пуриновых оснований, что приводит к угнетению биосинтеза пуринов de novo по механизму обратной связи, что опосредовано угнетением фермента гипоксантин-гуанин фосфорибозил-трансферазы.
Показания к применению
Снижение образования мочевой кислоты и ее солей при наличии подтвержденного накопления этих соединений (например, подагрический артрит, кожные тофусы, нефролитиаз) или при предполагаемом клиническом риске их накопления (например, в лечении злокачественных новообразований с угрозой развития острой нефропатии на фоне мочевой кислоты).
К основным клиническим состояниям, которые могут сопровождаться накоплением мочевой кислоты и ее солей, относятся:
— мочекаменная болезнь (образование камней из мочевой кислоты);
— острая мочекислая нефропатия;
— злокачественные опухоли и миелопролиферативный синдром, который характеризуется высокой скоростью обновления клеточной массы, когда развивается гиперурикемия после осуществления цитотоксической терапии;
— определенные нарушения ферментов, сопровождающиеся избыточным образованием солей мочевой кислоты, например, пониженная активность гипоксантин-гуанин-фосфорибозилтрансферазы (включая синдром Леша-Найхана), заниженная активность глюкозо-6-фосфатазы (включая гликогенозы), повышенная активность фосфорибозилпирофосфат-синтетазы, повышенная активность фосфорибозилпирофосфат-амидо-трансферазы, пониженная активность аденин-фосфорибозилтрансферазы.
Лечение мочекаменной болезни, сопровождающейся образованием 2,8-дигидроксиадениновых (2,8-ДГА) конкрементов в связи с пониженной активностью аденин-фосфорибозилтрансферазы.
Профилактика и лечение мочекаменной болезни с образованием смешанных кальциево-оксалатных камней на фоне гиперурикозурии, когда диетотерапия и увеличение потребления жидкости оказываются недостаточными.
Способ применения и дозы
Прием внутрь. Препарат необходимо использовать один раз в день после еды, запивая обильным количеством воды. При превышении суточной дозы 300 мг или наличии побочных эффектов со стороны ЖКТ, дозу следует разделить на несколько приемов. Таблетки аллопуринола 300 мг можно разделить по риске на две равные части.
Для взрослых
Для того, чтобы уменьшить риск развития НР рекомендуется применять аллопуринол в начальной дозе 100 мг один раз в день. Если этой дозы недостаточно для того, чтобы должным образом снизить концентрацию мочевой кислоты в сыворотке крови, то суточную дозу препарата можно постепенно увеличивать по 100 мг каждые 1-3 недели до достижения желаемого эффекта. При повышении дозы аллопуринола каждые 1-3 недели необходимо определять концентрацию мочевой кислоты в сыворотке крови до достижения ее целевого значения. Следует проявлять особую осторожность при нарушении функции почек.
При подборе дозировок препарата рекомендуется основывать выбор на следующих схемах дозирования (в зависимости от выбранного режима рекомендуется использовать таблетки по 100 мг или 300 мг):
Рекомендованная доза препарата составляет: 100-200 мг в сутки при легком течении заболевания; 300-600 мг в сутки при среднетяжелом течении; 700-900 мг в сутки при тяжелом течении. Максимальная суточная доза – 900 мг. Если при расчете дозы исходить из массы тела пациента, то доза аллопуринола должна составлять от 2 до 10 мг/кг/сутки.
Дети и подростки от 3 до 15 лет
Рекомендуемая доза: для детей 3–10 лет — 5–10 мг/кг/сутки; от 10 до 15 лет — 10–20 мг/кг/сутки. Если расчетная доза составляет менее 100 мг, следует выбирать таблетки по 100 мг. Суточная дозировка не должна превышать 400 мг.
Аллопуринол редко применяется в педиатрической практике. Исключение составляют злокачественные онкологические заболевания (особенно лейкозы) и некоторые ферментативные нарушения (например, синдром Леша-Найхана).
Пожилые пациенты
Поскольку специальные данные по применению аллопуринола в популяции людей пожилого возраста отсутствуют, для лечения таких пациентов следует применять препарат в минимальной дозе, обеспечивающей достаточное снижение концентрации мочевой кислоты в сыворотке крови. Особое внимание необходимо уделить рекомендациям по подбору дозы препарата для пациентов с нарушением функции почек (см. раздел Особые указания).
Проблемы с функцией почек
Поскольку аллопуринол и его метаболиты выводятся через почки, нарушения их функции могут привести к накоплению препарата и замедлению его выведения из организма, что увеличивает период полувыведения этих компонентов из плазмы. При тяжелой почечной недостаточности рекомендуется использовать аллопуринол в дозе ниже 100 мг в сутки или вводить разовые дозы по 100 мг с interval больше одного дня.
Если условия позволяют контролировать концентрацию оксипуринола в плазме крови, то дозу аллопуринола следует подобрать таким образом, чтобы концентрация оксипуринола в плазме крови был ниже 100 мкмоль/л (15,2 мг/л).
Выведение аллопуринола и его производных может быть достигнуто при помощи гемодиализа. В случае, если процедуры диализа проводятся 2-3 раза в неделю, нужно рассмотреть вопрос о переходе на альтернативный режим – применение 300-400 мг аллопуринола сразу после завершения диализа (в промежутках между сеансами препарат не принимается).
У пациентов с нарушением функции почек комбинирование аллопуринола с тиазидными диуретиками следует проводить с исключительной осторожностью. Аллопуринол следует назначать в самых низких эффективных дозах при тщательном мониторировании функции почек (см. раздел «Взаимодействие с другими лекарственными средствами»).
Проблемы с функцией печени
При нарушениях работы печени необходимо снизить дозировку препарата. В начале терапии рекомендуется контролировать лабораторные показатели функции печени.
Состояния, сопровождающиеся усилением обмена солей мочевой кислоты (например, злокачественные новообразования, синдром Леша-Найхана)
Перед началом применения цитотоксических средств требуется коррекция уже существующей гиперурикемии и/или гиперурикозурии с помощью аллопуринола. Многие важны аспекты включают адекватную гидратацию для поддержания оптимального диуреза и ощелачивание мочи, что способствует повышению растворимости мочевой кислоты и ее солей. Дозировка аллопуринола должна находиться на уровне нижнего предела рекомендованного диапазона.
Если нарушение функции почек обусловлено развитием острой мочекислой нефропатии или другой почечной патологии, то лечение следует продолжать в соответствии с рекомендациями, представленными в подразделе «Нарушение функции почек».
Принятые меры могут помочь снизить риск накопления ксантина и мочевой кислоты, что может усложнить течение заболевания.
Рекомендации по мониторингу
Для коррекции дозы препарата необходимо с оптимальными интервалами оценивать концентрацию солей мочевой кислоты в сыворотке крови, а также уровень мочевой кислоты и уратов в моче.
Срок годности
Не применять по истечении срока годности.
Условия отпуска
Отпускается по рецепту.
Наименование держателя (владельца) регистрационного удостоверения/ Организация, принимающая претензии потребителей
125284, Россия, г. Москва, Ленинградский проспект, д. 31А, стр. 1.
Тел.: +7 (495) 258-45-28.
Производитель **
ООО «Авексима Сибирь».
652473, Россия, Кемеровская обл. – Кузбасс, г. Анжеро-Судженск, ул. Герцена, д. 7.
Кемеровская область – Кузбасс, г. Анжеро-Судженск, ул. Герцена, д. 7.
Фармакокинетика
Аллопуринол эффективен при пероральном приеме. Он быстро усваивается из верхних отделов желудочно-кишечного тракта (ЖКТ). Согласно фармакокинетическим исследованиям, аллопуринол обнаруживается в крови уже через 30-60 минут после приема. Его биодоступность варьируется от 67% до 90%.
Максимальный уровень аллопуринола в плазме крови (ТСmах) обычно фиксируется примерно через 1,5 часа после перорального приема. С этого момента его концентрация в плазме постепенно уменьшается. Через 6 часов после приема остаются лишь минимальные следы аллопуринола. Наибольшая концентрация (Сmах) активного метаболита — оксипуринола, возникает через 3-5 часов после перорального потребления аллопуринола, при этом уровень оксипуринола в плазме снижается значительно медленнее.
Распределение
Аллопуринол обладает низкой способностью связываться с белками в плазме, что означает, что его клиренс не будет значительно изменяться в результате вариаций уровня связывания с белками. Объем распределения (Vd) аллопуринола составляет приблизительно 1,6 литра на килограмм, указывая на его значительное накопление в тканях организма. Хотя исследование концентрации аллопуринола в различных тканях человека еще не проводилось, предполагается, что аллопуринол и его метаболит оксипуринол накапливаются в печени и слизистой кишечника, где активность ксантиноксидазы высока.
Биотрансформация
Аллопуринол метаболизируется ксантиноксидазой и альдегидоксидазой, в результате чего образуется оксипуринол, который также подавляет активность ксантиноксидазы. Тем не менее, оксипуринол действует менее активно по сравнению с аллопуринолом, но его период полувыведения (Т1/2) значительно продолжительнее.
Благодаря этому после единовременного приема аллопуринола в суточной дозе его ингибирующее действие на ксантиноксидазу сохраняется на протяжении 24 часов. У пациентов с нормальной функцией почек уровень оксипуринола в крови медленно растет до достижения стабильной концентрации. При использовании аллопуринола в дозе 300 мг в день его концентрация в плазме обычно составляет от 5 до 10 мг/л. Кроме того, к метаболитам аллопуринола относятся аллопуринол-рибозид и оксипуринол-7-рибозид.
Приблизительно 20% принятого перорально аллопуринола выводится через кишечник в неизмененном виде. Около 10% суточной дозы экскретируются клубочковым аппаратом почки в виде неизмененного аллопуринола. Еще 70% суточной дозы аллопуринола выводится почками в форме оксипуринола.
Оксипуринол выводится через почки в неизмененном состоянии, однако из-за канальцевой реабсорбции его период полувыведения длится дольше. Т1/2 аллопуринола составляет 1-2 часа, в то время как Т1/2 оксипуринола варьирует от 13 до 30 часов. Эти различия могут быть связаны с особенностями исследований и/или клиренсом креатинина (КК) у пациентов.
Пациенты с нарушением функции почек
У людей с нарушениями функции почек вывод аллопуринола и оксипуринола может существенно замедляться, что при длительном применении приводит к повышению их концентрации в плазме. У пациентов с нарушенной функцией почек и значением КК в диапазоне 10-20 мл/мин, после длительного приема аллопуринола в дозе 300 мг в сутки, уровень оксипуринола в плазме доходил до примерно 30 мг/л. Аналогичная концентрация может наблюдаться у пациентов с нормальными почками при назначении аллопуринола в дозе 600 мг в сутки. Таким образом, при лечении пациентов с проблемами в работе почек необходимо уменьшать дозу аллопуринола.
Пациенты пожилого возраста
У пациентов пожилого возраста значительные изменения фармакокинетических свойств аллопуринола маловероятны. Исключение составляют пациенты с сопутствующей патологией почек (см. раздел «Пациенты с нарушением функции почек»).
Противопоказания
Гиперчувствительность к аллопуринолу или любому из вспомогательных веществ, входящих в состав препарата.
Аллопуринол противопоказан при печеночной недостаточности, хронической почечной недостаточности (на стадии азотемии), при остром приступе подагры и для детей младше трех лет (в виде кислых лекарств).
Также его применение не рекомендуется во время беременности и лактации (см. раздел «Применение в период беременности и грудного вскармливания»).
С осторожностью
Показания к противопоказанию включают нарушения функций печени, гипотиреоз, диабет, гипертонию, первичный гемохроматоз, совместный прием с ингибиторами АПФ или диуретиками. У детей до 15 лет аллопуринол назначается только во время цитостатической терапии при раковых заболеваниях и ферментных нарушениях. Пожилые пациенты также должны принимать его с осторожностью, как и лица с нарушениями функций почек, что может вызвать задержку препарата и его метаболитов в организме, увеличивая период полувыведения этих веществ.
Применение во время беременности и в период грудного вскармливания
Беременность
Доказательства безопасности использования аллопуринола во время беременности ограничены, хотя этот препарат применялся в течение многих лет без заметных побочных эффектов. Во избежание риска для матери и плода, беременным не стоит принимать аллопуринол, если нет менее опасных аналогов лечения, и заболевание не угрожает жизни беременности.
Период грудного вскармливания
Данные исследования показывают, что аллопуринол и оксипуринол могут проникать в грудное молоко. У женщин, принимающих аллопуринол в дозе 300 мг в сутки, концентрация аллопуринола достигала 1,4 мг/л, а оксипуринола – 53,7 мг/л. Однако информации о влиянии таких веществ на находящихся на грудном вскармливании младенцев не представлено. Таким образом, применение аллопуринола в период лактации противопоказано.
Отсутствуют современные клинические данные для определения частоты развития НР. Их частота может варьировать в зависимости от дозы и от того, назначался ли препарат как монотерапия или в комбинации с другими препаратами.
Частота появления нежелательных реакций (НР) классифицируется на основе приблизительных данных, и для большинства НР отсутствует информация о частоте появления.
Классификация НР по частоте проявления следующая:
очень частые (≥1/10),
частые (от ≥1/100 до
- Вакансии
- Сообщить о нежелательной реакции
Побочные эффекты
Не допускается применение препарата при повреждении функционала почечной и печеночной систем, высоком уровне сенситивности к действующему ингредиенту.

Применение при беременности
Аллопуринол противопоказан во время беременности, а также при кормлении новорожденного грудным молоком. Вместе с тем, схема лечения и индивидуальные дозировки должны определяться только врачом. Также необходим регулярный контроль уровня уратов и концентрации мочевой кислоты в организме. Взрослый пациент может принимать от 100 до 900 мг аллопуринола от 2 до 4 раз в день.
Пациентам в детском возрасте до 15 лет обычная суточная доза колеблется в пределах 10-20 мг на единицу веса, что в общем составляет 100 – 400 мг. Прием осуществляется после принятия пищи. Повышение дозировки разрешается проводить под контролем врача при условии, что концентрация камней и мочевой кислоты в крови и урине не снижается.
При наличии нарушений в работе почек и печени необходимо быть осторожным с использованием данного препарата, возможно, потребуется снижение дозы. Это также касается случаев с пониженной активностью щитовидной железы. На начальных этапах терапии рекомендуется проводить анализы для оценки состояния печени.
Введение таблеток должно сопровождаться увеличением суточного объема употребляемой жидкости до 2-х литров. Вначале терапии подагрического синдрома, который непосредственно связан с обменными процессами в организме, происходит обострение патологии. Для его предупреждения разрешается применение нестероидных противовоспалительных средств или колхицина.
Медицинские специалисты предупреждают, что даже при правильной схемы лечения может происходить распад крупных фракций уратов в почечных лоханках. У детей назначение данного препарата возможно только при диагностировании опухолей для подавления раковых клеток, к примеру, при лейкозе, или при нарушениях, связанных с ферментативными процессами.
Для нормализации уровня мочевой кислоты у онкологических пациентов аллопуринол назначается перед началом цитостатической терапии. При лечении с применением химиотерапевтических препаратов отмечается значительное снижение психомоторной активности. Поэтому лицам, работающим с транспортными средствами или механизмами, требующими быстрой реакции, рекомендуется использовать этот препарат только в условиях стационара. Вопрос о назначении препарата пожилым пациентам должен решаться лечащим врачом.
Аллопуринол не улучшает сердечно-сосудистые исходы при ишемической болезни сердца
В 12 выпуске Европейского кардиологического журнала от 12 марта 2023 года опубликованы результаты исследования о влиянии аллопуринола на сердечно-сосудистые исходы при ишемической болезни сердца.

В ходе метаболизма пуринов, который превращается в мочевую кислоту, активированная ксантиноксидаза (КСO) генерирует активные формы кислорода (АФК) и способствует воспалению сосудов, увеличивая риск сердечно-сосудистых заболеваний. Уровень КСO заметно повышен в атеросклеротических бляшках у пациентов с проявлениями атеросклероза.
Повышенная экспрессия КСO может быть результатом колебательного напряжения сдвига. Повышенные концентрации мочевой кислоты в сыворотке и подагра также были признаны независимыми факторами риска сердечно-сосудистых заболеваний.
Несмотря на антиоксидантные свойства мочевой кислоты, которая может нейтрализовать пероксинитриты, ее уровень может способствовать атеросклерозу, увеличивая митохондриальную дисфункцию, выработку АФК и воспалительные процессы. Высокие уровни мочевой кислоты в сыворотке ассоциированы как с морфологическими изменениями в атеросклеротических бляшках, так и с повышенной смертностью от ИБС. Связь между повышенным уровнем мочевой кислоты в сыворотке и риском сердечно-сосудистых заболеваний сохраняется даже после учета основных факторов риска, включая функции почек. На основе этих данных европейские рекомендации по лечению артериальной гипертензии стали включать уровень мочевой кислоты в рутинные обследования для оценки риска сердечно-сосудистых заболеваний у гипертоников. Эти наблюдения стали основой гипотезы о том, что ингибирование КСO может предотвратить развитие сердечно-сосудистых заболеваний.
В рамках многоцентрового, проспективного, рандомизированного исследования в Великобритании (ALL-HEART) проводилось сравнение стандартной терапии и лечения аллопуринолом пациентов старше 60 лет с ишемической болезнью сердца (ИБС) без подагры в анамнезе. Участники были рандомизированы (1:1) для получения перорального аллопуринола с возможным увеличением дозировки до 600 мг в день (300 мг в день для пациентов с легкой почечной недостаточностью) или продолжения традиционного лечения.
Первичным исходом была комбинация не фатального инфаркта миокарда (ИМ), инсульта или смерти от сердечно-сосудистых заболеваний. Анализировались все пациенты из группы с обычным лечением и те, кто принял по крайней мере одну дозу рандомизированного препарата в группе аллопуринола. После рандомизации и исключения 216 пациентов, остался 5721 участник (средний возраст 72 ± 7 лет, 76% мужчины, 99% белые) были включены в модифицированную популяцию с намерением лечиться, из них 2853 — в группу аллопуринола и 2868 — в группу обычного лечения. Наиболее часто принимаемая доза аллопуринола составляла 600 мг в сутки. Средний период наблюдения составил 4,8 года.
Не было обнаружено различий между группами лечения по критериям (включая нефатальный инфаркт миокарда, нефатальный инсульт, смерть от сердечно-сосудистых заболеваний, смерть от всех причин, госпитализации в связи с острым коронарным синдромом, коронарной реваскуляризацией и госпитализацией по поводу сердечной недостаточности) независимо от исходной концентрации мочевой кислоты в сыворотке.
У 2447 участников группы аллопуринола, у которых уровень мочевой кислоты в сыворотке измерялся исходно и через 6 недель после рандомизации, уровень снизился со среднего значения 0,34 ± 0,1 ммоль/л до 0,18 ± 0,1 ммоль/л.
Из общего числа 1637 (57%) участников в группе с аллопуринолом отказались от рандомизированного лечения, в основном из-за нежелательных реакций или изменений в предпочтениях. Частота серьезных нежелательных реакций, возникновения раковых заболеваний или общего уровня смертности не отличалась между группами и не было зафиксировано серьезных побочных эффектов, которые могли бы привести к летальному исходу.
Исследование ALL-HEART стало первым значимым проспективным рандомизированным экспериментом, изучающим эффект аллопуринола у пациентов с ишемической болезнью сердца (ИБС). Среди более 5000 участников с ИБС, но без наличия подагры, не удалось выявить каких-либо преимуществ применения аллопуринола в контексте основных сердечно-сосудистых результатов. Хотя у пациентов, получавших аллопуринол, была отмечена более низкая заболеваемость подагрой после второго года исследования, это может быть связано с некоторыми систематическими ошибками в самоотчетах и ожиданиями, связанными с длительной терапией, снижающей уровень уратов среди людей с повышенным риском подагры. В этом исследовании также не зафиксированы клинические улучшения от применения аллопуринола или повышения качества жизни. Таким образом, аллопуринол вновь пополнил перечень противовоспалительных средств, показавших свою неэффективность в случае сердечно-сосудистых заболеваний, оставляя открытым вопрос, какие пациенты могут извлечь выгоду от противовоспалительной терапии.
Предыдущие небольшие интервенционные и обсервационные исследования, изучающие влияние уратснижающей терапии на сердечно-сосудистые исходы у пациентов с подагрой, дали противоречивые результаты. В двух относительно крупных исследованиях, CARES и FAST, пациентов с подагрой и установленным сердечно-сосудистым заболеванием были рандомизированы для лечения аллопуринолом или более новым ингибитором КСО, фебуксостатом. В исследовании CARES показатели смертности от всех причин и смерти от сердечно-сосудистых заболеваний были значительно выше при применении фебуксостата, чем при применении аллопуринола, что привело к предостережениям регулирующих органов против использования фебуксостата у пациентов с ранее существовавшими сердечно-сосудистыми заболеваниями. Отсутствие контрольной группы с плацебо или обычным лечением в этих исследованиях исключает однозначную интерпретацию их результатов.
Одним из ограничений исследования ALL-HEART является способ получения информации о соблюдении рандомизированной терапии: данные сообщались самими пациентами во время шестинедельных визитов и ежегодных контрольных осмотрах. Тем не менее, контрольные проверки назначения параллельно подтверждали отчеты участников. Значительное снижение уровня мочевой кислоты в сыворотке крови через шесть недель демонстрирует хорошую приверженность пациентов лечению аллопуринолом.
Известно, что препарат вызывает кожную сыпь, особенно вскоре после начала терапии. Чтобы избежать редкого, но потенциально серьезного осложнения тяжелой сыпи, аллопуринол немедленно прекращали, если участники сообщали о какой-либо сыпи. Это могло привести к большему отказу от терапии. Однако аналогичные показатели отмены наблюдались в исследовании CARES. Дозы аллопуринола, использованные в исследовании ALL-HEART (600 мг в день для большинства участников), были выше, чем дозы, обычно используемые при лечении подагры, но все еще в пределах разрешенного диапазона доз для этого показания (100–900 мг в день в Великобритании).
К участникам исследования не допускались пациенты с наличием подагры в анамнезе, что могло привести к тому, что средний уровень мочевой кислоты в крови в группе аллопуринола оказался относительно низким. Это, вероятно, ослабило потенциальные преимущества аллопуринола в качестве антиоксиданта, хотя в предварительно подготовленном анализе подгрупп данный эффект оставался нейтральным. В одном недавнем крупном обсервационном исследовании было установлено, что оптимальные уровни мочевой кислоты в сыворотке, связанные со смертностью от всех причин и сердечно-сосудистыми заболеваниями, ниже, чем пороги, обычно ассоциирующиеся с повышенным риском подагры.
Большинство участников ALL-HEART страдали от длительной ИБС, со средней продолжительностью заболевания около 10 лет на момент начала исследования; при этом пациенты с недавними коронарными событиями не были исключены. Возможно, результаты могли бы отличаться, если бы исследование проводилось на более остром контингенте пациентов.
Заключение.
Роль ингибирования ксантиноксидазы остается важной для снижения уровня мочевой кислоты в сыворотке, что позволяет предотвратить обострения подагры, но потенциальные преимущества этого подхода для сердечно-сосудистой системы не были подтверждены. Учитывая сложность окислительно-восстановительных процессов in vivo, в будущих исследованиях рекомендовано рассмотреть измерение других видов активных форм кислорода и активность различных ферментных источников, чтобы выявить более специфические мишени для фармакологического вмешательства, снижающего сердечно-сосудистые риски.
Источник: Источник: Европейский кардиологический журнал, European Heart Journal, том 44, выпуск 12, 21 марта 2023 г.
Дополнительные полезные материалы доступны на нашем канале в Телеграме.
Дизайн исследования
В рандомизированное контролируемое исследование были включены взрослые пациенты со стадией 3-4 хронической болезни почек и без подагры в анамнезе. Уровень альбумина/креатинина в моче превышал 265, или наблюдалось снижение скорости клубочковой фильтрации по меньшей мере на 3 мл/мин/1,73 м2 за последний год.
Пациенты получали аллопуринол (100-300 мг в день) или плацебо.
Первоначальной конечной точкой исследования было изменение скорости клубочковой фильтрации на 104 неделе. Скорость клубочковой фильтрации рассчитывалась по формуле CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration creatinine equation).
Результаты
- В исследование вошли 369 участников из Австралии и Новой Зеландии: 185 пациентов на аллопуриноле и 184 на плацебо. Трое пациентов из каждой группы исключены сразу после начала исследования.
- Средняя скорость клубочковой фильтрации составляла 31,7 мл/мин/1.73 м2. Средний уровень альбумина/креатинина в моче составил 716,9. Уровень мочевой кислоты был равен 8,2 мг/дл.
- Различия в изменении скорости клубочковой фильтрации между группами не выявлены (−3,33 мл/мин/1,73 м2 в год [95% ДИ, −4,11 — −2,55] в группе аллопуринола и −3,23 мл/мин/1,73 м2 в год [95% ДИ, −3,98 — −2,47] в группе плацебо). Среднее разница между группами составила −0,10 мл/мин/1,73 м2 в год [95% ДИ, −1,18 — 0,97]; P=0,85).
- Анализ безопасности показал, что нежелательные явления наблюдались у 46% пациентов из группы аллопуринола и у 44% из группы плацебо.
По данным исследования у пациентов с хронической болезнью почек и высоким риском прогрессии заболевания, терапия, направленная на снижение уровня мочевой кислоты (аллопуринол), не приводит к замедлению снижения скорости клубочковой фильтрации, по сравнению с плацебо.
Источник: Sunil V. Badve, Elaine M. Pascoe, Anushree Tiku и др. N Engl J Med 2020; 382:2504-2513.

Причины замедления выведения мочевой кислоты почками
Клинические формы и синдромы:
- хроническая почечная недостаточность;
- заболевания почек с предрасположенностью к интерстициальным и канальцевым повреждениям (поликистоз почек, анальгетическая нефропатия, гидронефроз);
- свинцовая нефропатия;
- обезвоживание;
- диабетический кетоацидоз;
- гиперпродукция молочной кислоты;
- преэклампсия;
- ожирение;
- гиперпаратиреоз;
- гипотиреоз;
- саркоидоз;
- хроническая бериллиозная интоксикация.
Лекарства и хронические интоксикации:
- тиазидные диуретики;
- циклоспорин;
- низкие дозы салицилатов;
- противотуберкулезные препараты (пиразинамид);
- этанол;
- леводопа.
Существует также первичная и вторичная подагра. Первичная подагра сопровождается отсутствием какого-либо основного заболевания, которое предшествует ее развитию. Она обусловлена генетическими недостатками пуринового обмена, связанными с несколькими генами, то есть представляет собой так называемый «конституциональный диспуризм».
Исследования уратного гомеостаза показали аутосомно-доминантный тип наследования таких аномалий. В частности, это наблюдается при врожденных нарушениях в содержании энзимов, занимающих ключевое положение в метаболизме пуринов.
При снижении активности гипоксантин-гуанин-фосфорибозилтрансферазы наблюдается увеличение ресинтеза пуринов из нуклеотидов, что может привести к синдрому Леша-Найхана. Этот синдром встречается исключительно у детей и молодых людей, и зачастую заканчивается уратной нефропатией с летальным исходом. В случае высокого содержания фосфорибозилпирофосфата наблюдается метаболический вариант гиперурикемии, поскольку этот фермент участвует в образовании предшественников мочевой кислоты. Вторичная подагра является одним из проявлений другого заболевания, возникающего при различных патологических процесса, чаще всего при хронической почечной недостаточности.
Для своевременного распознавания подагры, особенно на начальных стадиях, ключевым является клиническая картина острого подагрического артрита. Она хорошо известна, однако частота диагностических ошибок в первый год заболевания может достигать 90%, а через 5–7 лет правильный диагноз ставится лишь в 50% случаев. Причины позднего диагноза заключаются в недооценке характерных ранних симптомов заболевания и многообразии клинических проявлений подагры. Диагностика основывается на специфике клинической картины, повышении уровня мочевой кислоты в крови и обнаружении кристаллов урата натрия в тканях. В практике используются Римские диагностические критерии подагры:
- острый приступ артрита с поражением плюснефалангового сустава большого пальца ноги;
- подагрические узлы (тофусы);
- гиперурикемия (уровень мочевой кислоты в сыворотке выше физиологической нормы);
- выявление кристаллов уратов в синовиальной жидкости или мягких тканях.
Диагноз подагры считается достоверным при наличии любых двух из четырех критериев.
Существуют также менее распространенные критерии для диагностики подагры, предложенные Американской коллегией ревматологов (АСК) в 1977 году. Они скорее касаются острого воспалительного артрита или его рецидивов, чем самой подагры в целом. По этим критериям диагноз считается достоверным, если присутствуют 6 из 12 признаков:
- более одной атаки острого артрита;
- развитие наибольшей остроты воспалительного процесса в течение первого суток;
- моноартрит;
- покраснение кожи над болезненным суставом;
- боль или отек первого плюснефалангового сустава;
- асимметричное поражение первого плюснефалангового сустава;
- асимметричное поражение суставов предплюсны;
- наличие образований, напоминающих тофусы;
- асимметричное увеличение в пределах сустава (рентгенологический признак);
- субкортикальные кисты без эрозий;
- гиперурикемия;
- стерильная суставная жидкость.
В первые 3–4 года подагра протекает по типу рецидивирующего острого воспалительного моноартрита с полным обратным развитием и восстановлением функции суставов, при этом межприступный период продолжается от нескольких месяцев до 1–2 лет. В дальнейшем этот период укорачивается, в процесс вовлекаются все новые и новые суставы и воспалительные явления локализуются не только в суставах стоп, но распространяются на суставы верхних конечностей, что обычно совпадает с образованием тофусов.
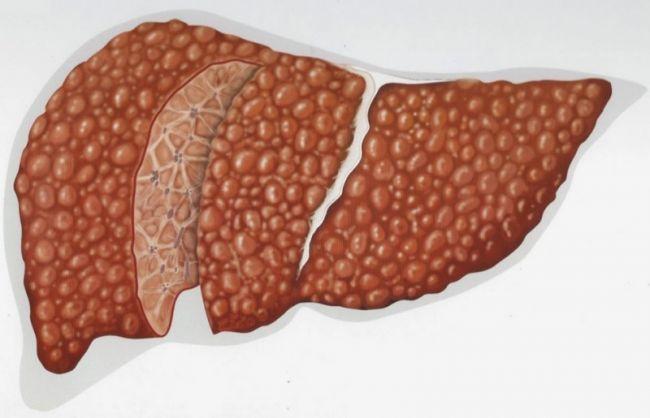
Тофусы представляют собой отложения кристаллов мочевой кислоты. Они обычно возникают в среднем через 6 лет после первого приступа подагры, хотя могут появиться и через 2–3 года. Ураты чаще всего осаждаются на поверхности суставного хряща, в синовиальной оболочке, в синовиальных влагалищах, сухожилиях, а В субкортикальных областях эпифизов костей.
Наиболее часто они локализуются на ушных раковинах и на задней поверхности локтевых суставов. Тофусы могут быть как единичными, так и множественными, и классифицируются по размеру: мелкие (до 1 см в диаметре), средние (от 1 до 2,5 см) и крупные (более 2,5 см). Подагрические узлы, локализующиеся в опорно-двигательном аппарате, являются ключевыми для формирования хронического подагрического артрита. Тофусы могут также образовываться в почках и других внутренних органах.
Хроническое течение подагры не ограничивается только вовлеченностью суставов и формированием тофусов, но и характеризуется поражением внутренних органов. Подагрическая нефропатия является наиболее важным с прогностической точки зрения проявлением подагры и самой распространенной причиной летальных исходов при этом заболевании.
Среди различных форм подагрической нефропатии можно выделить несколько типов: острая мочекислая блокада почечных канальцев, мочекислый нефролитиаз, возникающий из-за накопления солей мочевой кислоты в чашечках и лоханках почек, хроническую уратную нефропатию и диффузный гломерулонефрит. Острая мочекислая блокада возникает, например, при распаде опухолей вследствие интенсивного медикаментозного или рентгенотерапевтического лечения. Хроническая уратная нефропатия связана с отложением уратов в интерстиции почек, а развитие диффузного гломерулонефрита связано с иммунными расстройствами у пациентов с нарушенным пуриновым обменом. Иммуноморфологически, такой гломерулонефрит чаще всего классифицируется как мезангиопролиферативный, при котором обнаруживаются депозиты IgG и комплемента. Важно отметить, что подагра часто сопутствует другим патологиям, включая артериальную гипертонию, ожирение, гиперлипидемию, жировую дистрофию печени, атеросклероз и нарушения мозгового кровообращения, а также зависит от алкогольной зависимости.
Течение подагры характеризуется разнообразием темпов развития болезни. Возможно относительно доброкачественное течение с редкими приступами, небольшой гиперурикемией и урикозурией и длительным сохранением функциональной недостаточности опорно-двигательного аппарата. В других случаях, напротив, с самого начала заболевания наблюдаются частые атаки острого артрита с сильными болями или непрерывные атаки с множественным поражением суставов на протяжении нескольких недель или месяцев (подагрический статус). Рефрактерное к проводимой терапии течение подагры приводит к быстрому развитию функциональной недостаточности суставов и почек.
Критерии, по которым классифицируются формы подагры, включают: частоту приступов артрита в течение года, число вовлеченных суставов, степень разрушения костно-хрящевой ткани, наличие тофусов, а также поражение почек и его характер.
Варианты течения подагры
Легкая форма: артритные приступы происходят 1–2 раза в год, затрагивая не более двух суставов; почки не поражены, признаков деструкции суставов нет, тофусы либо отсутствуют, либо составляют лишь единичные образования до 1 см в диаметре.
Средней тяжести: 3–5 приступов в год, поражение 2–4 суставов, умеренно выраженная костно-суставная деструкция, множественные мелкие тофусы, поражение почек ограничено почечно-каменной болезнью.
Тяжелая форма: приступы возникают более 5 раз в год с множественным поражением суставов, наличием крупных тофусов и выраженной нефропатией.
Основными задачами терапии подагрического артрита являются:
- купирование острых приступов заболевания;
- снижение уровня уратов в организме;
- лечение хронического полиартрита;
- влияние на сопутствующую патологию.
Для купирования острого подагрического артрита применяются противовоспалительные средства. Среди них: колхицин (колхицин, колхикум-дисперт), нестероидные противовоспалительные препараты (НПВП) — вольтарен, дикловит, диклоран, целебрекс, мовалис, а также кортикостероиды — полькортолон, преднизолон, метилпреднизолон; или их комбинация — амбене.
Как колхицин, так и НПВП способны значительно уменьшить симптомы острого артрита в течение нескольких часов, в то время как у пациентов, не получающих лечение, приступ может продолжаться несколько недель. Ранее считалось, что наиболее эффективным средством для лечения приступов острого артрита при подагре является колхицин.
Ярко выраженный и быстрый (в течение 48 ч) эффект колхицина рассматривался как один из диагностических признаков этого заболевания. Колхицин способен предупредить дальнейшее развитие острого приступа подагры при его назначении в первые 30–60 мин атаки. Его лечебное действие обусловлено угнетением фагоцитарной активности нейтрофилов. При остром приступе подагры мононатриевые соли уратов, фагоцитированные нейтрофилами, приводят вследствие мембранолитического их действия к гибели этих клеток и высвобождению лизосомальных ферментов, которые отвечают за развитие острого воспаления.
Среди НПВП предпочтение отдается индометацину (индотард, метиндол) и диклофенаку (вольтарен, диклоран, диклофен). Дозировка составляют 200–250 мг/сут, при этом большую часть суточной дозы применяют в первые часы приступа.
Проведенные контролированные исследования не выявили более высокой эффективности традиционных НПВП по сравнению с селективными ингибиторами ЦОГ-2 (нимесил, нимулид, целебрекс), например целекоксибами (коксиб, целебрекс). Однако окончательное суждение о сравнительной эффективности этих препаратов можно вынести только в ходе дальнейших исследований.
Суточная доза колхицина составляет 4–6 мг/сут, причем 2/3 этой дозы пациент должен принять до 12 часов дня в первый день приступа. Обычно разовая доза равна 0,6 мг, ее применяют каждый час до значительного снижения воспаления. После уменьшения воспаления дозу следует постепенно снижать до полной отмены, уменьшая на 0,6 мг дважды в день.
Часто пациенты не могут достигнуть оптимальной суточной дозы из-за побочных эффектов. К основным побочным реакциям колхицина относятся тошнота, рвота, понос, возможны также геморрагический гастроэнтерит, лейкопения и нейропатия. В случаях подагрического статуса с непрекращающимися атаками острого артрита, не поддающимися лечению НПВП, возможно внутривенное введение колхицина.
Противоподагрическая терапия (базисная, модифицирующая болезнь) направлена на профилактику рецидивов острого артрита, снижение содержания мочевой кислоты в крови, предупреждение дальнейшего формирования тофусов и их обратное развитие. Все противоподагрические препараты делятся на две большие группы: урикодепрессоры (урикостатики) и урикозурики. Урикодепрессоры тормозят синтез мочевой кислоты путем ингибирования фермента ксантиноксидазы, превращающего гипоксантин в ксантин, а ксантин в мочевую кислоту. Урикозурики повышают экскрецию мочевой кислоты, подавляя обратную реабсорбцию уратов почечными канальцами.
К препаратам первой группы относится аллопуринол (аллопуринол, аллопуринол-эгис, аллупол, пуринол, ремид, тиопуринол, милурит), который занимает ведущее место среди других средств для лечения подагры. Показаниями для назначения аллопуринола являются метаболическая подагра, стойкая гиперурикемия, частые острые атаки артрита, мочекислая болезнь и генетически обусловленный дефицит гипоксантин-гуанин-фосфорибозилтрансферазы.
Применение аллопуринола возможно и у больных с подагрической нефропатией с начальными проявлениями хронической почечной недостаточности и небольшой азотемии. Начальная доза аллопуринола составляет 300 мг/сут. В случае неэффективности такой дозы ее увеличивают до 400–600 мг/сут, а при достижении клинического эффекта постепенно снижают. Поддерживающая доза определяется уровнем гиперурикемии и обычно составляет 100–300 мг/сут.
Аллопуринол способствует исчезновению острых артритных атак или их значительному облегчению, уменьшению размеров тофусов и их размягчению, снижению уровня мочевой кислоты до нормальных значений, нормализации показателей мочевого синдрома, уменьшению частоты почечных колик и улучшению функции почек. У некоторых пациентов на первом этапе может проявляться увеличение уровня мочевой кислоты и обострение подагрического артрита, поэтому в начале терапии его рекомендуется комбинировать с противовоспалительными средствами, такими как низкие дозы колхицина или НПВП. По этой причине не стоит принимать аллопуринол в период обострения подагрического артрита. При назначении аллопуринола могут появляться побочные эффекты, проявляющиеся желудочно-кишечной токсичностью, аллергическими реакциями (высыпания на коже, эозинофилия), а также гепатотоксичностью с повышением уровня сывороточных аминотрансфераз.
Урикозурические препараты, являющиеся слабыми органическими кислотами, менее значимы в терапии подагры по сравнению с урикостатиками. Их не следует назначать при высоком уровне мочевой кислоты в крови, а также при наличии нефропатии, даже на начальных стадиях.
Из урикозурических препаратов сульфинпиразон и пробенецид особенно широко используются в США. Сульфинпиразон (сульфинпиразон, апо-сульфинпиразон, антуран) назначают по 200–400 мг/сут в два приема. Его, как и другие урикозурические средства, принимают с большим количеством жидкости, которую для профилактики нефролитиаза следует ощелачивать. Побочные реакции встречаются относительно часто и проявляются желудочной и кишечной диспепсией, лейкопенией, аллергическими реакциями. Противопоказанием к назначению сульфинпиразона является язвенная болезнь желудка и, конечно, подагрическая нефропатия.
Пробенецид (бенемид) является производным бензойной кислоты, его прописывают в дозировке 1,5–2,0 г/сут. Бензойная кислота содержится в клюкве и ягодах, а В листьях брусники.
Поэтому отвары и морсы из ягод и листьев этих растений показаны больным подагрой и в большей степени больным с подагрической нефропатией, тем более что помимо бензойной кислоты они содержат гиппуровую кислоту, обладающую урикосептическими свойствами. Урикозурическая активность присуща блокатору рецептора ангиотензина II и фенофибрату (грофибрат, нофибал).
Наиболее эффективны производные бензбромарона, которые обладают не только урикозурическим эффектом, но и урикодепрессорным. Их используют как в монотерапии, так и в комбинации с аллопуринолом. Одним из комбинированных средств является алломарон, который включает 20 мг бензбромарона и 100 мг аллопуринола, его обычно принимают по 1 таблетке дважды в день.
Применение ощелачивающих препаратов и растворов является важной частью комплексной терапии подагры; они помогают снизить риск развития нефропатии, в частности — мочекаменной болезни. К ним относятся магурлит, блемарен и уралит. Перед приемом этих средств необходимо контролировать уровень рН мочи. Также к этим средствам можно отнести питьевую соду в дозировке 2–4 г в день или щелочные минеральные воды.
При выраженных симптомах артрита необходимо также проводить местное лечение (долобене, финалгон, диклоран плюс, долгит крем, немулид гель, бишофит-гель).
Диетотерапия занимает центральное место в лечении подагры по сравнению с другими ревматическими заболеваниями. Рекомендуется снизить общую калорийность питания, особенно поскольку при подагре часто наблюдается избыточный вес. Нужно уменьшить поступление экзогенных пуринов и животных жиров, которые снижают выведение мочевой кислоты почками.
Крайне осторожно следует подходить к употреблению любых алкогольных напитков, включая пиво и красное вино. Исключают из пищевого рациона печенку, почки, жирные сорта мяса, мясные бульоны, копчености, горох, бобы, чечевицу, шпинат, цветную капусту, шпроты, сельдь. Следует ограничить потребление мяса до 2–3 раз в неделю, при этом лучше употреблять его в отварном виде.
В. В. Бадокин, доктор медицинских наук, профессор РМАПО, Москва